 |
Glob Reg Health Technol Assess 2024; 11: 175-190 ISSN 2283-5733 | DOI: 10.33393/grhta.2024.3062 ORIGINAL RESEARCH ARTICLE |
 |
Analisi di impatto sul budget sanitario italiano di roxadustat per il trattamento dell’anemia da malattia renale cronica
Budget impact analysis on the Italian healthcare system of roxadustat for the treatment of anemia due to chronic kidney disease
Objective: The aim of this study was to evaluate the economic consequences of the introduction of roxadustat on the market as treatment for chronic kidney disease (CKD)-related anaemia in Italy.
Method: A budget impact model was developed to assess the economic impact of the introduction of roxadustat for the management of patient with CKD-related anaemia. The analysis was conducted considering National Health Service (NHS) perspective and three years’ time horizon. Eligible population for the treatment with roxadustat was estimated through published literature and clinicians’ support. Direct healthcare costs included drug acquisition (list prices for base case) and administration costs, monitoring costs, cost per blood transfusion, costs related to the management of adverse events and dialysis costs.
Results: The model estimated a three years expenditure associated with the management of patients with CKD-related incident anaemia in Italy of about € 260 and € 44.6 million for non-dialysis dependent (NDD) and dialysis-dependent (DD) patients respectively. The introduction of roxadustat on the market could generate a reduction in the expenditure related to the iron supplementation both for NDD and for DD patients (−€ 397,305 and −€ 50,135 over three years of the analysis, respectively) and a reduction in the pharmaceutical expenditure for NDD patients (−€ 2.3 million, −€ 7.5 million and −€ 13 million at first, second and third year of the analysis). Overall, the introduction of roxadustat could generate a saving for NHS approximately equal to € 2.3, € 7.5 and € 13 million at first, second and third year of the analysis.
Conclusion: The introduction of roxadustat could generate a reduction in the expenditure for the management of patients with CKD anaemia. A scenario analysis which used tender prices for ESAs and hypothesis of confidential discount for roxadustat showed that the saving for NHS will be kept if roxadustat’s discount is greater than 60.3%.
Keywords: Anaemia, Chronic kidney disease, Economic evaluation, Roxadustat
Received: March 7, 2024
Accepted: June 1, 2024
Published online: September 10, 2024
Global & Regional Health Technology Assessment - ISSN 2283-5733 - www.aboutscience.eu/grhta
© 2024 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
L’anemia rappresenta una complicanza comune della malattia renale cronica (MRC) e la sua prevalenza aumenta progressivamente con il peggioramento della funzione renale. L’Organizzazione Mondiale della Sanità definisce il livello di severità dell’anemia a seconda dei livelli di emoglobina (Hb) (1). L’anemia coinvolge una quota molto ampia di pazienti con malattia renale cronica: tra i pazienti seguiti all’interno delle Unità Operative di Nefrologia, quelli con anemia risultano pari al 60% in Svezia (2), al 58% in Spagna (3) e al 45-62% in Italia (4,5). Questa evidenza risulta confermata dallo studio CKDopps (Chronic Kidney Disease Outcomes and Practice Patterns), uno studio di coorte internazionale, prospettico, condotto in pazienti con MRC avanzata. Tale studio ha stimato come il 28-52% di 6.766 pazienti con MRC allo stadio III-V non in dialisi (Not Dialysis-Dependent, NDD), seguiti in Francia, Germania, Brasile e USA avesse valori di Hb < 12 g/dL (6). In uno studio prospettico spagnolo, condotto da Portolés et al., su 439 pazienti con MRC allo stadio 3, dopo 36 mesi di osservazione circa il 35% dei pazienti aveva sviluppato anemia (7). Secondo i dati USA del DOPPS Practice Monitor, circa l’80% dei pazienti in dialisi (Dialysis Dependent, DD) ha valori di Hb < 12 g/dL; la maggior parte di questi è in terapia con agenti stimolanti l’eritropoiesi (ESA) (8).
Numerosi studi osservazionali hanno messo in relazione la presenza di anemia con una prognosi negativa, sia in termini di progressione della MRC che di sviluppo di eventi cardiovascolari, aumentato rischio di ospedalizzazione o morte. Uno studio prospettico danese, condotto su 16.972 pazienti (di cui il 14% non risultava affetto da anemia), ha fatto emergere come, tra i pazienti NDD, il rischio di iniziare la dialisi per i pazienti con anemia severa (Hb < 8 g/dL) fosse marcatamente più elevato (HR 1,91, 95% IC 1,61-2,26) rispetto ai pazienti senza anemia; inoltre, sempre rispetto ai pazienti senza anemia, i pazienti NDD avevano un rischio maggiore di ospedalizzazione per qualsiasi causa maggiore (HR 1,74, IC 95% 1,57-1,93), di mortalità per tutte le cause (HR 1,82, 95% IC 1,70-1,94) e di eventi cardiovascolari maggiori (Major Acute Cardiovascular Events, MACE) (HR 1,14, IC 95% 1,02-1,26) (9). Per i pazienti DD sono state stimate associazioni simili rispetto a quanto emerso per la popolazione NDD; in particolare, ai pazienti DD sono risultati associati un aumentato rischio di ospedalizzazione (HR 1,51, 95% IC 1,20-1,90), un aumentato rischio di morte per tutte le cause (HR 1,91, 95% IC 1,50-2,43) e un aumentato rischio di eventi cardiovascolari maggiori (HR 1,16, 95% IC 0,84-1,61) rispetto ai pazienti senza anemia (9).
A livello nazionale, lo studio prospettico condotto da Minutolo et al. (10) in pazienti con MRC da lieve ad avanzata, arruolati in 40 Unità Operative di nefrologia in Italia (5,11,12), ha stimato come il 25,8% e il 12,7% dei pazienti abbia sviluppato rispettivamente anemia lieve (Hb < 11-12 g/dL per le donne o < 11-13 g/dL per gli uomini) e moderata (Hb < 11 g/dL o necessità di terapia con ESA).
Da tale studio è emerso come, ai pazienti con anemia lieve, rispetto ai pazienti non anemici, risultino associati un rischio più elevato di MRC terminale (end stage kidney disease, ESKD) (HR=1,42, IC 95% 1,02-1,98) e un maggior rischio di morte per tutte le cause (HR=1,55, IC 95% 1,04-2,32), mentre ai pazienti con anemia moderata risultino associati un ancor più elevato rischio di ESKD (HR= 1,73 IC 95% 1,20-2,51) e un ancor più elevato rischio di morte (HR=1,83, IC 95% 1,05-3,19).
Prima della disponibilità degli agenti stimolanti l’eritropoiesi (Erythropoiesis-Stimulating Agents, ESAs) nella pratica clinica, i pazienti con MRC e anemia grave spesso venivano gestiti con trasfusioni di globuli rossi; tali trasfusioni risultavano però spesso associate a un elevato rischio di malattia virale e di sovraccarico di ferro (13,14). In mancanza di terapie efficaci, i pazienti venivano mantenuti severamente anemici, con conseguente scarsa qualità della vita. A oggi gli ESA, associati alla terapia marziale, rappresentano lo standard di cura per l’anemia correlata alla malattia renale cronica. Pur rappresentando una strategia terapeutica efficace, una percentuale di pazienti ha una risposta insufficiente al trattamento con ESA (iporesponsivi) e necessitano di dosaggi elevati per correggere l’anemia. Questa sottopopolazione di pazienti sembrerebbe avere un rischio aumentato di eventi cardiovascolari o trombotici, forse in relazione all’uso di ESA ad alto dosaggio (15-17).
Gli inibitori del dominio della prolil-idrossilasi (HIF-PHI) rappresentano una nuova classe di farmaci, in grado di stimolare la produzione di eritropoietina endogena, simulando una condizione di ipossia (18). Questi farmaci, favorendo anche l’assorbimento intestinale e la mobilizzazione del ferro dal sistema reticoloendoteliale, offrono nuove opportunità di trattamento dell’anemia, specialmente nei pazienti infiammati con insufficiente risposta agli ESA (19). A differenza degli ESA, gli HIF-PHI vengono somministrati per via orale.
Roxadustat rappresenta il primo inibitore orale di HIF-PH per il trattamento di pazienti adulti con anemia sintomatica associata a MRC in dialisi e non in dialisi ad essere stato approvato in Europa.
In Italia, roxadustat può essere prescritto dietro piano terapeutico. In particolare, per i pazienti che sono già in trattamento con ESA, tale piano terapeutico prevede 12 settimane di sospensione di un’eventuale terapia con ESA prima dell’inizio del trattamento con roxadustat, così come era previsto dai criteri di inclusione dello studio clinico di confronto di roxadustat rispetto agli ESA in pazienti incidenti al trattamento dialitico (HIMALAYAS (20)).
L’obiettivo di questo studio è valutare la sostenibilità economica da parte del Servizio Sanitario Nazionale (SSN) dell’introduzione di roxadustat per il trattamento dei pazienti con anemia da MRC in Italia mediante la conduzione di un’analisi di impatto sul budget. Tale analisi si propone di esplorare l’impatto monetario dell’introduzione di roxadustat sul mercato, sia per la popolazione DD, sia per la popolazione NDD, fornendo una stima dei differenziali di costo tra lo scenario in cui si assume un’introduzione sul mercato di roxadustat e lo scenario in cui roxadustat non risulta presente.
Metodi
L’analisi di impatto sul budget è stata condotta secondo la prospettiva del SSN e seguendo le Linee Guida suggerite dall’International Society of Pharmacoeconomics and Outcome Research (ISPOR) (21,22).
In particolare, l’analisi è stata condotta mediante l’impiego di un modello economico sviluppato in excel tale da stimare i costi associati alla gestione e al trattamento dei pazienti con anemia correlata a MRC, sia per lo scenario in assenza di roxadustat, sia per lo scenario in cui si prevede l’introduzione di roxadustat sul mercato. In relazione alla dipendenza o meno dalla dialisi e in relazione al trattamento ricevuto (ESA o roxadustat), l’utilizzo delle risorse sanitarie da parte del paziente con anemia correlata alla MRC risulta differente; il modello economico ha tentato di registrare e valorizzare le risorse sanitarie erogate dal SSN per la cura e la gestione dei pazienti con anemia correlata a MRC in Italia, distinguendo tra pazienti NDD e pazienti DD, al fine di ottenere una stima del costo medio annuo associato alla gestione del paziente in trattamento con ESA o con roxadustat. Successivamente, tali costi medi annui, stratificati in base alla dipendenza dalla dialisi e in base al trattamento ricevuto (ESA o roxadustat), sono stati moltiplicati per il numero di pazienti NDD e DD che, in corrispondenza di ciascuno scenario e di ciascun anno di analisi, si assume siano trattati con ESA o roxadustat, al fine di ottenere un costo complessivo di gestione e trattamento dei pazienti con anemia correlata alla MRC per entrambi gli scenari di analisi. L’impatto dell’introduzione di roxadustat sulla spesa totale sostenuta dal SSN per la gestione e il trattamento di questi pazienti viene valutato come differenziale di costo tra i due scenari.
Per lo scenario senza roxadustat sono state considerate le terapie maggiormente utilizzate per il trattamento dell’anemia da MRC, quali gli ESA (epoetina alfa, darbepoetina alfa, epoetina beta, epoetina zeta e metossipolietilenglicole-epoetina beta) in concomitanza con la supplementazione del ferro sia per via orale, sia per via endovenosa o anche nessun trattamento.
L’analisi è stata condotta considerando un orizzonte temporale di 3 anni e considerando distintamente i pazienti NDD e i pazienti DD.
Nella Figura 1 è riportata la struttura del modello in forma grafica
Popolazione eleggibile e scenari di analisi
Roxadustat è indicato per il trattamento di pazienti adulti con anemia sintomatica associata a MRC (23); il piano terapeutico di AIFA ne individua la rimborsabilità per i pazienti che presentano anemia sintomatica (Hb < 11 g/dL) e che sono naïve alla terapia con ESA oppure che non sono stati trattati con ESA nelle 12 settimane precedenti. Quest’ultimo criterio rende di fatto molto raro il cambio di trattamento da ESA a roxadustat, in quanto non viene garantita la continuità terapeutica; per questo motivo, ai soli fini della valutazione economica, si è considerata questa porzione di pazienti trascurabile e si sono considerati come eleggibili al trattamento con roxadustat esclusivamente i pazienti incidenti alla terapia per l’anemia con ESA o HIF-PHI.
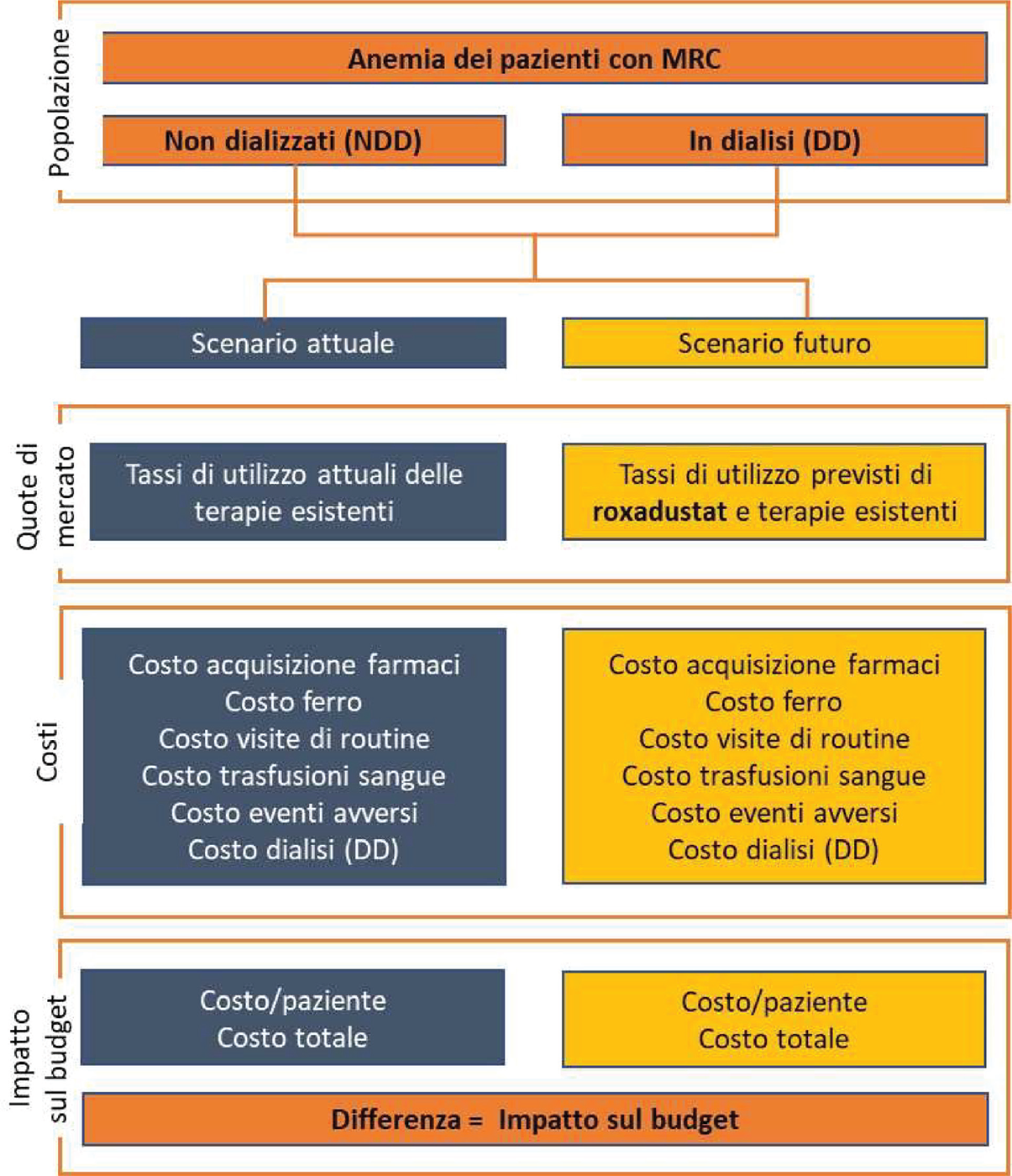
FIGURA 1 - Struttura del modello di impatto sul budget in forma grafica.
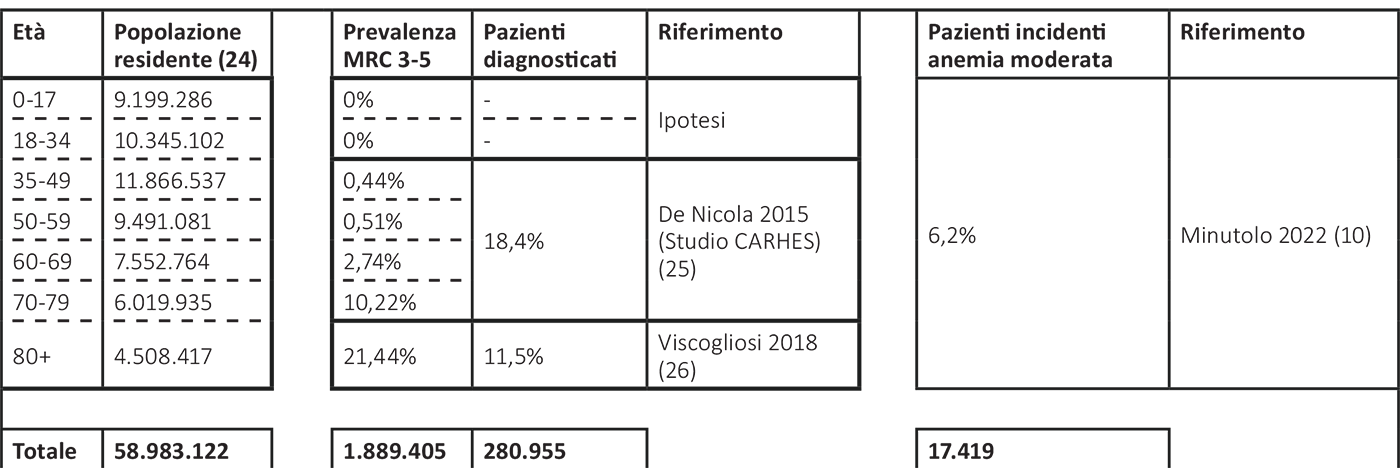
La popolazione eleggibile al trattamento con roxadustat è riportata nella Figura 2 e nella cascata epidemiologica rappresentata nella Tabella 1. In particolare, applicando alla popolazione residente in Italia al 2022 (ISTAT (24)) la stima di prevalenza della MRC allo stadio 3-5 divisa per fasce d’età come riportato nello studio CARHES (Cardiovascular risk profile in Renal patients of the Italian Health Examination Survey) (25) e in quello di Viscogliosi (26), si ottiene un numero di pazienti con MRC allo stadio 3-5 pari a circa 1,89 milioni; di questi solo una parte è correttamente diagnosticata ed è consapevole di essere affetta da MRC (18,4% se sotto gli 80 anni e 11,5% dagli 80 anni in su) (25,26), arrivando a circa 290.000 pazienti diagnosticati con MRC allo stadio 3-5. Considerando che il 6,2% di questi pazienti risulta incidente per anemia ogni anno con valori di Hb < 11 g/dL (anemia moderata), il numero di pazienti eleggibili al trattamento con roxadustat è risultato pari a 17.419 pazienti. Di questi, grazie a una rielaborazione da studi di Real World (27,28), è stato stimato che solo il 3% dei pazienti incidenti per anemia è sottoposto a dialisi, pari a 523 pazienti eleggibili, mentre i restanti 16.896 sono in terapia conservativa.
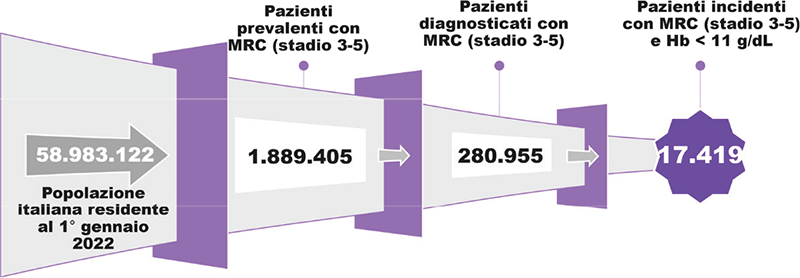
FIGURA 2 - Stima della popolazione eleggibile al trattamento con roxadustat.
Attualmente gli ESA e/o la supplementazione marziale rappresentano lo standard di cura dei pazienti affetti da anemia da MRC.
Nella Tabella 2 sono riportate le percentuali di utilizzo delle diverse molecole di ESA in commercio in Italia durante i tre anni di analisi per lo scenario attuale, quindi senza la presenza di roxadustat sul mercato, e per lo scenario in cui se ne assume l’introduzione. In particolare, per entrambi gli scenari, su parere del clinico esperto coinvolto nello sviluppo dell’analisi economica, è stato considerato che il 5% della popolazione eleggibile in realtà non venga trattata per cause esterne (p. es., accesso e inerzia alle cure, comorbilità…). All’interno di ciascuno scenario, la popolazione eleggibile è stata suddivisa in due sottopopolazioni, vale a dire la popolazione di pazienti NDD e la popolazione di pazienti DD.
È stato assunto che, nello scenario in cui si prevede l’introduzione di roxadustat sul mercato, il numero di pazienti trattati con roxadustat sia crescente nel corso degli anni in analisi, fino ad arrivare a una quota di pazienti trattata con roxadustat al terzo anno pari al 57%. Le quote di pazienti trattati con roxadustat in corrispondenza di ciascun anno di analisi sono state stimate a partire da dati di mercato basati su una popolazione estremamente selezionata (solo pazienti incidenti) rispetto al totale degli eleggibili. Per questo motivo, soprattutto la quota di pazienti trattata con roxadustat al terzo anno di analisi risulta piuttosto elevata.
Con riferimento alla popolazione NDD si è considerato un numero di pazienti trattati con roxadustat pari a 1.690, 5.576 e 9.631 pazienti rispettivamente al primo, al secondo e al terzo anno dalla sua introduzione, mentre, con riferimento alla popolazione DD, si è assunto un numero di pazienti trattati con roxadustat pari a 52, 173 e 298 pazienti rispettivamente al primo, al secondo e al terzo anno di analisi.
Parametri di costo
All’interno dell’analisi sono stati considerati il costo di acquisizione e somministrazione dei trattamenti in analisi e del ferro per via endovenosa e per via orale, delle visite di routine, delle trasfusioni di sangue, della gestione degli eventi avversi e della dialisi.
| Pazienti NDD (27) | Pazienti DD (28) | |||||
|---|---|---|---|---|---|---|
| Scenario senza roxadustat | Anno 1 | Anno 2 | Anno 3 | Anno 1 | Anno 2 | Anno 3 |
| Roxadustat | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% | 0,0% |
| Non in terapia | 5,0% | 5,0% | 5,0% | 5,0% | 5,0% | 5,0% |
| Epoetina alfa | 34,6% | 34,6% | 34,6% | 31,8% | 31,8% | 31,8% |
| Darbepoetina alfa | 33,4% | 33,4% | 33,4% | 30,0% | 30,0% | 30,0% |
| Epoetina beta | 6,4% | 6,4% | 6,4% | 12,6% | 12,6% | 12,6% |
| Epoetina zeta | 14,1% | 14,1% | 14,1% | 16,3% | 16,3% | 16,3% |
| Metossipolietilenglicole-epoetina beta | 6,5% | 6,5% | 6,5% | 4,3% | 4,3% | 4,3% |
| Scenario con roxadustat | Anno 1 | Anno 2 | Anno 3 | Anno 1 | Anno 2 | Anno 3 |
| Roxadustat | 10,0% | 33,0% | 57,0% | 10,0% | 33,0% | 57,0% |
| Non in terapia | 5,0% | 5,0% | 5,0% | 5,0% | 5,0% | 5,0% |
| Epoetina alfa | 30,9% | 22,5% | 13,8% | 28,4% | 20,7% | 12,7% |
| Darbepoetina alfa | 29,9% | 21,8% | 13,4% | 26,9% | 19,6% | 12,0% |
| Epoetina beta | 5,7% | 4,2% | 2,6% | 11,3% | 8,2% | 5,0% |
| Epoetina zeta | 12,6% | 9,2% | 5,6% | 14,6% | 10,7% | 6,5% |
| Metossipolietilenglicole-epoetina beta | 5,8% | 4,2% | 2,6% | 3,8% | 2,8% | 1,7% |
Il costo di acquisizione dei trattamenti è stato stimato combinando il prezzo dei singoli farmaci (Tab. 3) con il rispettivo dosaggio medio rilevato da studi clinici o da analisi di dati Real World (Tab. 4).
Il costo del ferro per via endovenosa nei pazienti con MRC non dializzati tiene conto anche del personale e del materiale impiegato durante la somministrazione in ospedale.
Per il costo di acquisizione del farmaco è stato considerato il prezzo ex-factory al netto dei due sconti obbligatori del 5% per il caso-base. Come scelta conservativa, per gli ESA per i quali sono disponibili i biosimilari, solo i prezzi di questi ultimi sono stati considerati nell’analisi.
Gli ESA necessitano della catena del freddo per il trasporto e la corretta conservazione. Un’indagine condotta da Purcom Procurement ha identificato uno spreco medio del 14% per questo tipo di farmaco, dovuto all’interruzione della catena del freddo; tale spreco è stato considerato nel modello economico. Per roxadustat non è stato preso in considerazione alcun tipo di spreco, dato che la composizione farmaceutica è stabile a temperatura ambiente e non necessita quindi di condizioni particolari per la sua conservazione.
Con riferimento al costo relativo alla supplementazione di ferro, all’interno dell’analisi sono stati considerati sia il costo del ferro orale, sia il costo del ferro somministrato per via endovenosa. Le frequenze e i costi di acquisizione del ferro sono riportati nella Tabella 5. In particolare, mediante il supporto di clinici esperti nel campo della MRC, è stato assunto che il 25% e l’8,5% rispettivamente dei pazienti NDD e DD assumano ferro orale. Con riferimento al consumo di ferro per via endovenosa, per la popolazione NDD dello studio DOLOMITES (29), è risultato che il 6,2% dei pazienti in trattamento con roxadustat e il 12,7% dei pazienti in trattamento con ESA consumano mediamente ferro per via endovenosa rispettivamente per 34,7 mg/mese e 69,6 mg/mese. Per i pazienti DD, all’interno dello studio HIMALAYAS non risulta presente l’informazione circa la proporzione di pazienti DD in trattamento con roxadustat ed ESA che utilizza il ferro per via endovenosa. Al fine di acquisire tale informazione, sono state effettuate delle assunzioni a partire dal consumo medio e mediano mensile di ferro per via endovenosa osservato per i pazienti in trattamento con roxadustat (media = 58,2 mg; mediana = 0 mg) ed ESA (media = 88,7 mg; mediana = 42,9 mg) all’interno dello studio clinico HIMALAYAS; in particolare, sapendo che nel braccio roxadustat meno del 50% dei pazienti utilizzava ferro per via endovenosa (mediana nulla) e che nel braccio ESA più del 50% dei pazienti utilizzava ferro per via endovenosa (mediana non nulla) e assumendo per i pazienti che effettivamente assumono ferro per via endovenosa un consumo medio mensile di ferro pari ad almeno il doppio di quello osservato all’interno dello studio clinico e riferito a tutti i pazienti (a prescindere dal fatto che assumano ferro per via endovenosa o meno), il consumo medio annuo di ferro per via endovenosa tra i pazienti in trattamento con roxadustat ed ESA che effettivamente ricevono ferro per via endovenosa risulterebbe rispettivamente pari a 1.395,4 mg (dose media annua pari a 697,7 mg × 2) e pari a 2.128,1 mg (dose media annua pari a 1.064.1 mg × 2). A questo punto, assumendo un consumo medio annuo di ferro per via endovenosa per tutti i pazienti che effettivamente ricevono ferro pari a circa 1.500 mg (dunque senza effettuare alcuna distinzione di dosaggio tra i pazienti in trattamento con roxadustat ed ESA), risulterebbe che circa il 46,5% dei pazienti in trattamento con roxadustat (697,7 mg/1.500 mg) e che circa il 70,9% dei pazienti in trattamento con ESA (1.064,1 mg/1.500 mg) assumono ferro per via endovenosa.
| Molecola | Prodotto | Confezione | Prezzo | Riferimento |
|---|---|---|---|---|
| Roxadustat | Evrenzo | 12 tab da 70 mg | € 246,68 | Gazzetta Ufficiale n.48 del 25/02/2023 (43) |
| Epoetina alfa | Binocrit | 6 siringhe 4.000 UI | € 204,48 | Farmadati (44) |
| Darbepoetina alfa | Aranesp | 1 siringa 30 mcg | € 58,73 | Farmadati (44) |
| Epoetina beta | Neorecormon | 6 siringhe 4.000 UI | € 206,88 | Farmadati (44) |
| Epoetina zeta | Retacrit | 6 siringhe 4.000 UI | € 204,24 | Farmadati (44) |
| Metossipolietilenglicole-epoetina beta | Mircera | 1 siringa 75 mcg | € 152,30 | Farmadati (44) |
| Popolazione NDD | |||
| Molecola | Posologia media | Costo annuo | Fonte posologia |
| Roxadustat | 218,2 mg somministrati ogni settimana | € 3.344 | Studio DOLOMITES (29) |
| Epoetina alfa | 3.950 UI somministrati 13 volte al mese | € 5.985 | Studio RW CAPRI (27) |
| Darbepoetina alfa | 35 mg somministrati 4 volte al mese | € 3.749 | Studio DOLOMITES (29) |
| Epoetina beta | 2.308 UI somministrati 13 volte al mese | € 3.538 | Studio RW CAPRI (27) |
| Epoetina zeta | 3.462 UI somministrati 13 volte al mese | € 5.239 | Studio RW CAPRI (27) |
| Metossipolietilenglicole-epoetina beta | 96 mg somministrati una volta al mese | € 2.667 | Studio RW CAPRI (27) |
| Popolazione DD | |||
| Molecola | Posologia media | Costo annuo | Fonte posologia |
| Roxadustat | 276,2 mg somministrati ogni settimana | € 4.232 | Pooled analysis on DD patients (45) |
| Epoetina alfa | 2.662 UI somministrati 13 volte al mese | € 4.034 | Pooled analysis on DD patients (45) |
| Darbepoetina alfa | 31,6 mg somministrati 4 volte al mese | € 3.385 | Studio PYRENEES (46) |
| Epoetina beta | 2.588 UI somministrati 13 volte al mese | € 3.967 | RCP – NEORECORMON (47) |
| Epoetina zeta | 2.662 UI somministrati 13 volte al mese | € 4.029 | Ipotesi: uguale a epoetina alfa |
| Metossipolietilenglicole-epoetina beta | 84 mg somministrati una volta al mese | € 2.333 | RCP – MIRCERA (48) |
| Popolazione NDD | |||
| Costo ferro | Roxadustat | ESA | Fonte |
| Costo annuo ferro orale | € 41,0 | € 41,0 | Rielaborazione da informazioni sottostanti e Farmadati (44) |
| Costo annuo ferro per via endovenosa | € 7,6 | € 31,1 | Rielaborazione da informazioni sottostanti e Farmadati (44) |
| Utilizzo ferro orale | Roxadustat | ESA | Fonte |
| Quota di pazienti utilizzatori | 25% | 25% | Roxadustat: Expert opinion
ESA: RIKAS study (32) |
| Posologia | 85 mg al giorno | ||
| Utilizzo ferro per via endovenosa | Roxadustat | ESA | Fonte |
| Quota di pazienti utilizzatori | 6,2% | 12,7% | Studio DOLOMITES (29) |
| Dose mensile (annuale) ferro, calcolata solo per pazienti utilizzatori di ferro | 34,74 mg
(416,88 mg) |
69,59 mg
(835,08 mg) |
Studio DOLOMITES (29) |
| Quota ferro carbossimaltosio | 99% | 99% | Expert opinion |
| Quota ferro saccarato | 0% | 0% | |
| Quota ferro gluconato | 1% | 1% | |
| Posologia ferro carbossimaltosio e frequenza media | 500 mg somministrati 0,83 volte l’anno | 500 mg somministrati 1,67 volte l’anno | Rielaborazione da Studio DOLOMITES (29) |
| Posologia ferro saccarato e frequenza media | 200 mg somministrati 2,08 volte l’anno | 200 mg somministrati 4,18 volte l’anno | |
| Posologia ferro gluconato e frequenza media | 62,5 mg somministrati 6,67 volte l’anno | 62,5 mg somministrati 13,36 volte l’anno | |
| Popolazione DD | |||
| Costo ferro | Roxadustat | ESA | Fonte |
| Costo annuo ferro orale | € 15,4 | € 15,4 | Rielaborazione da informazioni sottostanti e Farmadati (44) |
| Costo annuo ferro per via endovenosa | € 182,6 | € 278,4 | Rielaborazione da informazioni sottostanti e Farmadati (44) |
| Utilizzo ferro orale | Roxadustat | ESA | Fonte |
| Quota di pazienti utilizzatori | 9% | 9% | Roxadustat: Expert opinion
ESA: RIKAS study (32) |
| Posologia | 94 mg al giorno | ||
| Utilizzo ferro per via endovenosa | Roxadustat | ESA | Fonte |
| Quota di pazienti utilizzatori | 46,5% | 70,9% | Rielaborazione e ipotesi da studio HIMALAYAS |
| Dose mensile (annuale) ferro, calcolata solo su pazienti utilizzatori di ferro | 125 mg
(1.500 mg) |
125 mg
(1.500 mg) |
Rielaborazione e ipotesi da studio HIMALAYAS |
| Quota ferro carbossimaltosio | 95% | 95% | Expert opinion |
| Quota ferro saccarato | 0% | 0% | |
| Quota ferro gluconato | 5% | 5% | |
| Posologia ferro carbossimaltosio e frequenza media | 500 mg somministrati 3 volte l’anno | 500 mg somministrati 3 volte l’anno | Rielaborazione e ipotesi da studio HIMALAYAS |
| Posologia ferro saccarato e frequenza media | 200 mg somministrati 7,5 volte l’anno | 200 mg somministrati 7,5 volte l’anno | |
| Posologia ferro gluconato e frequenza media | 62,5 mg somministrati 24 volte l’anno | 62,5 mg somministrati 24 volte l’anno | |
Il costo di acquisizione del ferro somministrato per via endovenosa è stato stimato considerando tre tipologie di ferro per via endovenosa (ferro carbossimaltosio, saccarato e gluconato); tale costo è stato dunque stimato come costo ponderato per le quote di mercato associate a ciascun trattamento. Mediante le informazioni riportate nella Tabella 4 è stato possibile stimare un costo annuo per la supplementazione di ferro orale (ferro solfato) pari a € 41,0 e pari a € 15,4 rispettivamente per il paziente NDD e DD, mentre il costo annuo associato alla supplementazione del ferro per via endovenosa è risultato pari a € 7,6 e a € 31,1 per il paziente NDD rispettivamente in trattamento con roxadustat e con ESA e pari a € 182,6 e a € 278,4 per il paziente DD rispettivamente in trattamento con roxadustat ed ESA. I costi annui stimati per il ferro somministrato per via endovenosa comprendono anche il costo di somministrazione; tale costo è stato stimato attraverso le tariffe nazionali relative alla specialistica ambulatoriale (codici 99.14.1 – Infusione di immunoglobuline per via endovenosa; 99.24.1 – Infusione di sostanze ormonali) (30) ed è stato considerato solamente per i pazienti NDD in quanto per i pazienti DD è stato assunto che il ferro per via endovenosa venga somministrato durante la dialisi, per cui tale costo risulta già coperto dal costo associato alla dialisi.
Nella Tabella 6 sono riportati le frequenze di utilizzo e i costi associati alle visite di routine, alle trasfusioni di sangue, alla gestione degli eventi avversi e alla dialisi.
Con riferimento alle visite di routine, la frequenza con cui queste vengono effettuate per i pazienti in trattamento con ESA è stata ottenuta dalla letteratura (TUNE study per i pazienti NDD (31), RIKAS study per i pazienti DD (32), mentre, per i pazienti in trattamento con roxadustat, dal momento che non si considera che il nuovo farmaco porti cambiamenti nella gestione generale del paziente, sono state assunte le stesse frequenze emerse per gli ESA; in particolare, sono state considerate cinque visite annuali per i pazienti NDD e visite mensili per i pazienti DD. Il costo unitario di una visita è stato ottenuto dal tariffario nazionale delle prestazioni di assistenza specialistica (codice 89.7 – Visita generale) (30).
Gli eventi avversi considerati per questa analisi sono l’ictus, l’infarto del miocardio e la trombosi dell’accesso vascolare. Il costo associato alla gestione di ciascun evento avverso è stato stimato associando alle probabilità di sperimentare ciascun evento avverso ottenute dalla letteratura (33,34), il costo di gestione specifico per quell’evento avverso. Il costo unitario associato alla gestione di ciascun evento avverso è stato stimato utilizzando il tariffario nazionale delle prestazioni di assistenza ospedaliera (35), il rapporto annuale sull’attività di ricovero ospedaliero 2019 (36) e dati provenienti da studi pubblicati (37). In particolare, il costo associato alla gestione dell’ictus e il costo di gestione dell’infarto miocardico sono stati stimati considerando sia il costo dell’evento acuto, dunque il costo associato alla gestione ospedaliera dell’evento (calcolato come costo medio delle tariffe delle prestazioni di assistenza ospedaliera per acuti maggiormente utilizzate per questa tipologia di evento ponderato per il numero di dimissioni effettuate in un anno), sia il costo del follow-up pari a un anno dall’evento acuto (37). Il costo di gestione della trombosi dell’accesso vascolare è stato stimato considerando il solo costo dell’evento acuto; tale costo è stato stimato mediante la stessa metodologia adottata per l’ictus e per l’infarto miocardico.
| Costi di monitoraggio | Costo unitario | Fonte | |
| Visita di routine | € 20,66 | Tariffe delle prestazioni di assistenza specialistica ambulatoriale (30) | |
| Visita specialistica | € 20,66 | ||
| Trasfusione di sangue | € 25,82 | ||
| Costo dialisi | Costo annuo | Fonte | |
| Emodialisi | € 27.724 | Tariffe delle prestazioni di assistenza specialistica ambulatoriale (30), Registro Dialisi e Trapianto Lazio (39) | |
| Dialisi peritoneale | € 18.566 | ||
| Costi di gestione degli eventi avversi | Costo per evento | Fonte | |
| Ictus | € 11.155 | Tariffario nazionale delle prestazioni di assistenza ospedaliera (35), rapporto SDO 2019 (36), Sciattella et al. 2019 (37) | |
| Infarto del miocardio | € 10.568 | ||
| Trombosi dell’accesso vascolare | € 6.479 | ||
| Utilizzo della dialisi | Quota di utilizzo | Fonte | |
| Emodialisi | 90% | Rielaborazione da Registro italiano dialisi e trapianto (39) | |
| Dialisi peritoneale | 10% | ||
| Probabilità annua eventi avversi | Roxadustat | ESA | Fonte |
| Ictus | 1,2% | 1,2% | Theidel et al. 2013 (33) |
| Infarto del miocardio | 2,9% | 2,9% | Theidel et al. 2013 (33) |
| Trombosi dell’accesso vascolare | 7,2% | 5,2% | Lok et al. 2003 (34) |
| Popolazione NDD | |||
| Frequenza monitoraggio | Roxadustat | ESA | Fonte |
| Visite di controllo | 5 | 5 | Roxadustat: assunto uguale a ESA
ESA: TUNE study (31) |
| Visite specialistiche | 5 | 5 | |
| Quota di pazienti che effettuano trasfusioni | 9,6% | 11,8% | Studio DOLOMITES (29) |
| Frequenza annua di utilizzo delle trasfusioni | 1 | 1 | Expert opinion |
| Popolazione DD | |||
| Frequenza monitoraggio | Roxadustat | ESA | Fonte |
| Visite di controllo | 12 | 12 | Expert opinion |
| Visite specialistiche | 12 | 12 | |
| Quota di pazienti che effettuano trasfusioni | 9,6% | 12,9% | Rielaborazione da studi clinici PYRENEES (46), HIMALAYAS (20), SIERRA, ROCKIES |
| Frequenza annua di utilizzo delle trasfusioni | 1 | 1 | Expert opinion |
Il costo associato alle trasfusioni è stato stimato tenendo conto della proporzione di pazienti che ricevono una trasfusione (distinguendo tra i pazienti DD e NDD in trattamento con ESA o con roxadustat) e assumendo una trasfusione all’anno per tutti i pazienti. Il costo unitario relativo alla trasfusione è stato stimato mediante il tariffario nazionale delle prestazioni di assistenza specialistica (99.07.1 – Trasfusione di sangue o emocomponenti) (30).
Il costo associato alla dialisi è stato stimato assumendo una quota di pazienti che si sottopone a emodialisi pari al 90% e una quota di pazienti che si sottopone a dialisi peritoneale pari al 10% (Registro italiano dialisi e trapianto del 2019 (38). La frequenza con cui i pazienti si sottopongono a ciascuna tipologia di dialisi è stata ottenuta dal Registro Dialisi e Trapianti della Regione Lazio (2019) (39); in particolare sono state considerate tre e sette sedute a settimana rispettivamente per l’emodialisi e per la dialisi peritoneale. Il costo associato all’emodialisi è stato stimato ponderando le tariffe associate alle procedure 39.95.1 (Emodialisi in acetato o in bicarbonato) e 39.95.9 (Emodialisi – Emofiltrazione) per il numero di pazienti sottoposti a emodialisi registrati all’interno del Registro Dialisi e Trapianti della Regione Lazio, mentre il costo associato alla dialisi peritoneale è stato stimato ponderando le tariffe associate ai codici 54.98.1 (Dialisi peritoneale automatizzata, CCPD) e 54.98.2 (Dialisi peritoneale continua, CAPD) per il numero di pazienti sottoposti a dialisi peritoneale registrati all’interno del Registro Dialisi e Trapianti della Regione Lazio. Mediante l’impiego di queste informazioni è stato possibile stimare un costo annuo per l’emodialisi pari a € 27.724 e un costo annuo per la dialisi peritoneale pari a € 18.566.
Analisi di sensibilità
Al fine di valutare la robustezza dei risultati a seguito della variazione del valore assoluto dei parametri all’interno del loro range di scostamento, è stata condotta un’analisi di sensibilità deterministica. In particolare, per questa analisi, è stata assunta una variabilità del ±20% in relazione a ciascun parametro incluso nel modello. I risultati derivanti da tale analisi sono mostrati attraverso il grafico tornado.
È stata inoltre condotta un’analisi di scenario per approfondire meglio la sensibilità del modello rispetto all’utilizzo di ciascuna tipologia di ferro per via endovenosa (ferro carbossimaltosio, ferro saccarato, ferro gluconato) da parte dei pazienti DD e NDD. In particolare, rispetto al caso-base che vedeva un uso quasi esclusivo del ferro carbossimaltosio, sono stati simulati i seguenti scenari alternativi: 1) tutti i pazienti assumono solo ferro saccarato; 2) tutti i pazienti assumono solo ferro gluconato. I risultati di tale simulazione sono riportati nella Tabella 10
Infine, è stata condotta una seconda analisi di scenario che considera i prezzi gara degli ESA e alcune ipotesi di sconto confidenziale per roxadustat. Questa analisi di scenario è motivata dal fatto che i prezzi degli ESA sono fortemente influenzati dalle gare di appalto e il prezzo di aggiudicazione può risultare sensibilmente diverso da quello pubblicato in Gazzetta Ufficiale. Analogamente, è noto che sia presente uno sconto confidenziale per roxadustat, perché riportato in Gazzetta Ufficiale, con entità dello sconto non pubblica; per questo motivo, nella stessa analisi di scenario sono state valutate diverse ipotesi di sconto di roxadustat.
I prezzi gara degli ESA utilizzati per tale analisi di scenario sono riportati nella Tabella 7 e derivano da un’analisi sui prezzi medi delle gare eseguite fra ottobre 2019 e settembre 2022 e pubblicate sul portale CONSIP. Per roxadustat sono state considerate ipotesi di sconto dal 10% al 90%, con intervalli del 10%.
Risultati
Il modello economico ha permesso di stimare un costo medio annuo per paziente NDD in trattamento con roxadustat o con ESA rispettivamente pari a € 3.941 e a € 5.307, mentre il costo medio annuo per il paziente DD in trattamento con roxadustat o con ESA è risultato rispettivamente pari a € 30.239 e a € 29.659; in particolare, con riferimento al paziente DD, circa l’80% del costo è risultato associato alla dialisi. La Tabella 8 riporta il dettaglio dei costi medi dei pazienti NDD e DD stratificati per trattamento e per singola voce di costo.
Nelle Tabelle 9 e 10 sono riportati i risultati dell’analisi di impatto sul budget nel caso base rispettivamente per la popolazione NDD e DD. Con riferimento alla popolazione NDD, il modello ha stimato come, in assenza di roxadustat, la spesa annua associata alla gestione ed al trattamento dei pazienti con anemia da MRC in Italia sia pari a circa € 86,8 milioni; l’introduzione di roxadustat sul mercato comporterebbe una riduzione della spesa complessiva per il SSN di € 2,3, € 7,5 e 13,0 milioni rispettivamente al primo, al secondo e al terzo anno di commercializzazione.
| Molecola | Prodotto | Confezione | Prezzo | Fonte |
|---|---|---|---|---|
| Epoetina alfa | Binocrit | 6 siringhe 4.000 UI | € 24,54 | Analisi prezzi medi gara (49) |
| Darbepoetina alfa | Aranesp | 1 siringa 30 mcg | € 35,83 | |
| Epoetina beta | Neorecormon | 6 siringhe 4.000 UI | € 66,20 | |
| Epoetina zeta | Retacrit | 6 siringhe 4.000 UI | € 24,51 | |
| Metossipolietilenglicole-epoetina beta | Mircera | 1 siringa 75 mcg | € 79,20 |
| NDD | DD | |||
|---|---|---|---|---|
| Roxadustat | ESA | Roxadustat | ESA | |
| Farmaco | € 3.344 | € 4.695 | € 4.232 | € 3.684 |
| Supplementazione ferro | € 49 | € 72 | € 198 | € 294 |
| Eventi avversi | € 443 | € 433 | € 905 | € 776 |
| Monitoraggio | € 103 | € 103 | € 248 | € 248 |
| Trasfusioni | € 2 | € 3 | € 2 | € 3 |
| Dialisi | € 0 | € 0 | € 24.654 | € 24.654 |
| Totale | € 3.941 | € 5.307 | € 30.239 | € 29.659 |
| Anno 1 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
|---|---|---|---|
| Costo del farmaco | € 75.364.469 | € 73.080.548 | −€ 2.283.921 |
| Costo supplementazione di ferro | € 1.156.650 | € 1.116.919 | −€ 39.730 |
| Costo eventi avversi | € 6.950.120 | € 6.966.759 | € 16.640 |
| Costo di monitoraggio | € 3.316.178 | € 3.316.178 | € 0 |
| Costo delle trasfusioni | € 48.904 | € 47.944 | −€ 960 |
| Costo totale | € 86.836.320 | € 84.528.348 | −€ 2.307.972 |
| Anno 2 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
| Costo del farmaco | € 75.364.469 | € 67.827.529 | −€ 7.536.939 |
| Costo supplementazione di ferro | € 1.156.650 | € 1.025.539 | −€ 131.111 |
| Costo eventi avversi | € 6.950.120 | € 7.005.030 | € 54.911 |
| Costo di monitoraggio | € 3.316.178 | € 3.316.178 | € 0 |
| Costo delle trasfusioni | € 48.904 | € 45.737 | −€ 3.167 |
| Costo totale | € 86.836.320 | € 79.220.014 | −€ 7.616.307 |
| Anno 3 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
| Costo del farmaco | € 75.364.469 | € 62.346.119 | −€ 13.018.350 |
| Costo supplementazione di ferro | € 1.156.650 | € 930.186 | −€ 226.464 |
| Costo eventi avversi | € 6.950.120 | € 7.044.965 | € 94.846 |
| Costo di monitoraggio | € 3.316.178 | € 3.316.178 | € 0 |
| Costo delle trasfusioni | € 48.904 | € 43.434 | −€ 5.471 |
| Costo totale | € 86.836.320 | € 73.680.881 | −€ 13.155.439 |
| Anno 1 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
|---|---|---|---|
| Costo del farmaco | € 1.859.369 | € 1.884.992 | € 25.623 |
| Costo supplementazione di ferro | € 145.986 | € 140.973 | −€ 5.014 |
| Costo eventi avversi | € 385.452 | € 392.191 | € 6.739 |
| Costo di monitoraggio | € 246.358 | € 246.358 | € 0 |
| Costo delle trasfusioni | € 1.655 | € 1.610 | −€ 45 |
| Costo dialisi | € 12.249.454 | € 12.249.454 | € 0 |
| Costo totale | € 14.888.274 | € 14.915.578 | € 27.304 |
| Anno 2 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
| Costo del farmaco | € 1.859.369 | € 1.943.925 | € 84.557 |
| Costo supplementazione di ferro | € 145.986 | € 129.442 | −€ 16.545 |
| Costo eventi avversi | € 385.452 | € 407.689 | € 22.238 |
| Costo di monitoraggio | € 246.358 | € 246.358 | € 0 |
| Costo delle trasfusioni | € 1.655 | € 1.508 | −€ 147 |
| Costo dialisi | € 12.249.454 | € 12.249.454 | € 0 |
| Costo totale | € 14.888.274 | € 14.978.376 | € 90.103 |
| Anno 3 | Scenario senza roxadustat | Scenario con roxadustat | Impatto sul budget |
| Costo del farmaco | € 1.859.369 | € 2.005.421 | € 146.053 |
| Costo supplementazione di ferro | € 145.986 | € 117.409 | −€ 28.577 |
| Costo eventi avversi | € 385.452 | € 423.862 | € 38.410 |
| Costo di monitoraggio | € 246.358 | € 246.358 | € 0 |
| Costo delle trasfusioni | € 1.655 | € 1.401 | −€ 254 |
| Costo dialisi | € 12.249.454 | € 12.249.454 | € 0 |
| Costo totale | € 14.888.274 | € 15.043.906 | € 155.632 |
L’entità del risparmio è guidata per la maggior parte dal costo del farmaco, ma ci sono anche risparmi associati alla supplementazione del ferro (−€ 39.730, −€ 131.111 e −€ 226.464 rispettivamente al primo, al secondo e al terzo anno) e alle trasfusioni (−€ 960, −€ 3.167 e −€ 5.471 rispettivamente al primo, al secondo e al terzo anno di analisi). Si riscontra invece un leggero aumento della spesa dovuto alla gestione degli eventi avversi (+€ 16.640, +€ 54.911 e +€ 94.846 rispettivamente al primo, al secondo e al terzo anno di analisi). In particolare, dagli studi clinici non risulta una differenza statisticamente significativa in termini di incidenza degli eventi avversi tra i pazienti in trattamento con roxadustat e i pazienti in trattamento con ESA; tale incremento marginale dei costi di gestione degli eventi avversi per i pazienti in trattamento con roxadustat non risulta dunque attribuibile a un rischio aumentato di eventi avversi per questi pazienti ma rappresenta bensì la mera conseguenza di un calcolo economico dipendente in gran parte dalla stima del costo dei singoli eventi avversi considerati nell’analisi.
La spesa annua sostenuta dal SSN per la gestione e il trattamento dei pazienti incidenti con anemia da MRC in dialisi è risultata pari a circa € 14,9 milioni; anche in questo caso l’introduzione di roxadustat sul mercato comporterebbe una riduzione della spesa associata alla supplementazione di ferro (−€ 5.014, −€ 16.545 e −€ 28.577 rispettivamente al primo, al secondo e al terzo anno di analisi) e una riduzione della spesa associata alle trasfusioni (−€ 45, −€ 147 e −€ 254 rispettivamente al primo, al secondo e al terzo anno di analisi); tali riduzioni di spesa non risultano però sufficienti a compensare l’incremento della spesa farmaceutica (+€ 25.623, +€ 84.557 e +€ 146.053 rispettivamente al primo, al secondo e al terzo anno di analisi) e dei costi di gestione degli eventi avversi (+€ 6.739, +€ 22.238 e +€ 38.410 rispettivamente al primo, al secondo e al terzo anno di analisi), per cui complessivamente si avrebbe un incremento della spesa totale a carico del SSN pari a circa € 27.304, € 90.103 e € 155.632 rispettivamente al primo, al secondo e al terzo anno di analisi.
Nella Figura 3 sono riportate le stime di spesa totali per anno e scenario di analisi e le stime di impatto sul budget sia per la popolazione NDD (Fig. 3A) sia per la popolazione DD (Fig. 3B).
Il diverso impatto economico di roxadustat tra i pazienti NDD e DD deriva principalmente dal differente consumo medio di roxadustat tra le due popolazioni, così come osservato negli studi clinici (Tab. 4). Ovviamente nella pratica clinica il consumo medio di roxadustat potrebbe risultare diverso rispetto a quanto osservato negli studi clinici; l’analisi di sensibilità deterministica ha fatto emergere come, per la popolazione NDD, una riduzione del costo di roxadustat pari al 20% (dunque un consumo medio di roxadustat ridotto del 20%) comporterebbe un’ulteriore riduzione dell’impatto sul budget a tre anni pari a circa il 49% (−€ 34,4 milioni) rispetto al caso-base (−€ 23,1 milioni), mentre, per la popolazione DD, una riduzione del costo di roxadustat pari al 20% comporterebbe una riduzione della spesa a carico del SSN a tre anni di analisi pari a −€ 169.654 (rispetto a un incremento di spesa stimato nell’analisi del caso-base pari a € 273.038) (Fig. 4). Il costo di roxadustat e il costo dell’epoetina alfa sono risultati i parametri a cui è corrisposto il maggior impatto sui risultati cumulati a tre anni, sia per i pazienti NDD (Fig. 4A) che per i pazienti DD (Fig. 4B).
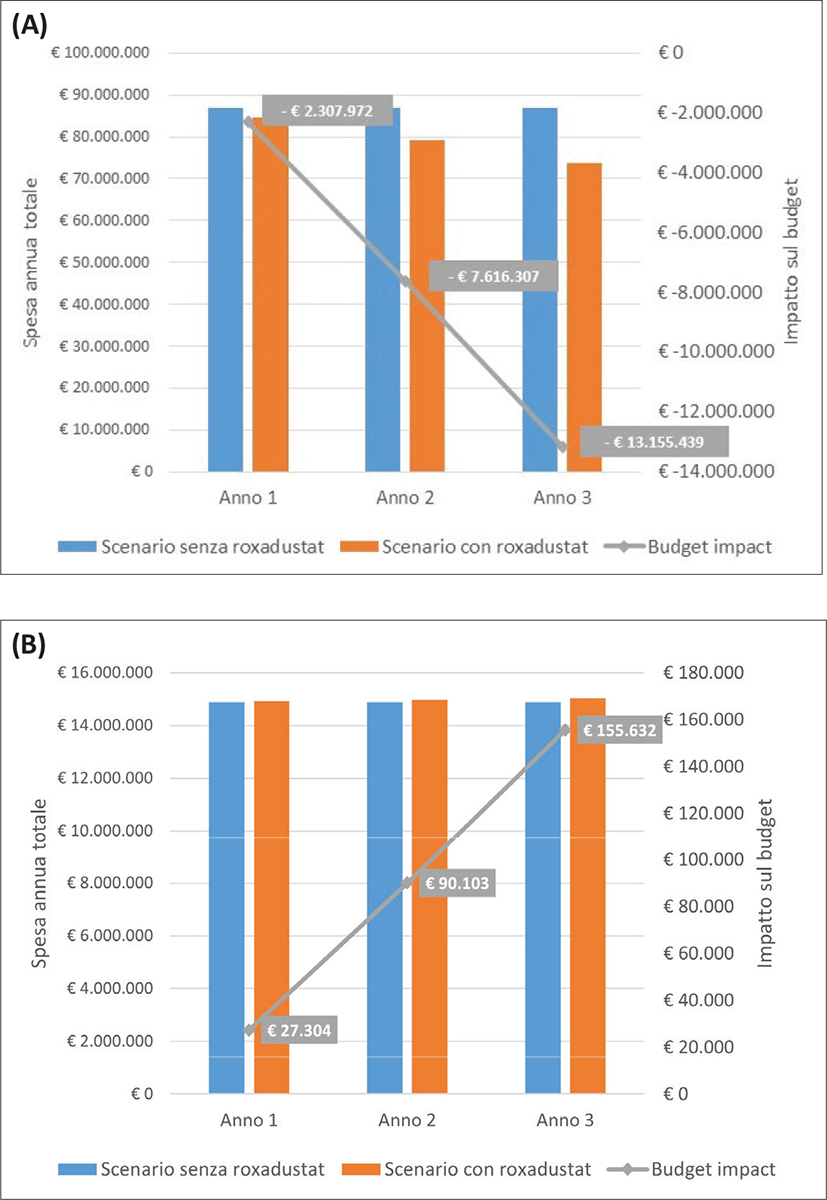
FIGURA 3 - Spesa totale per anno e scenario di analisi e impatto sul budget: popolazione NDD (3A), popolazione DD (3B).
L’analisi di scenario sui prezzi dei farmaci mostra come variano i risultati di impatto sul budget a tre anni utilizzando il prezzo di aggiudicazione gara per gli ESA e al variare dello sconto non trasparente di roxadustat (Tab. 11). Lo sconto di roxadustat non è un’informazione pubblica, per questo motivo le ipotesi di sconto coprono tutto l’arco possibile. Si nota come i risultati siano fortemente influenzati dallo sconto di roxadustat e per sconti superiori al 60% il modello prevede un risparmio complessivo per il Sistema Sanitario Nazionale. Nello specifico il punto di pareggio (impatto sul budget nullo) è stato individuato per uno sconto di roxadustat pari al 60,3%.
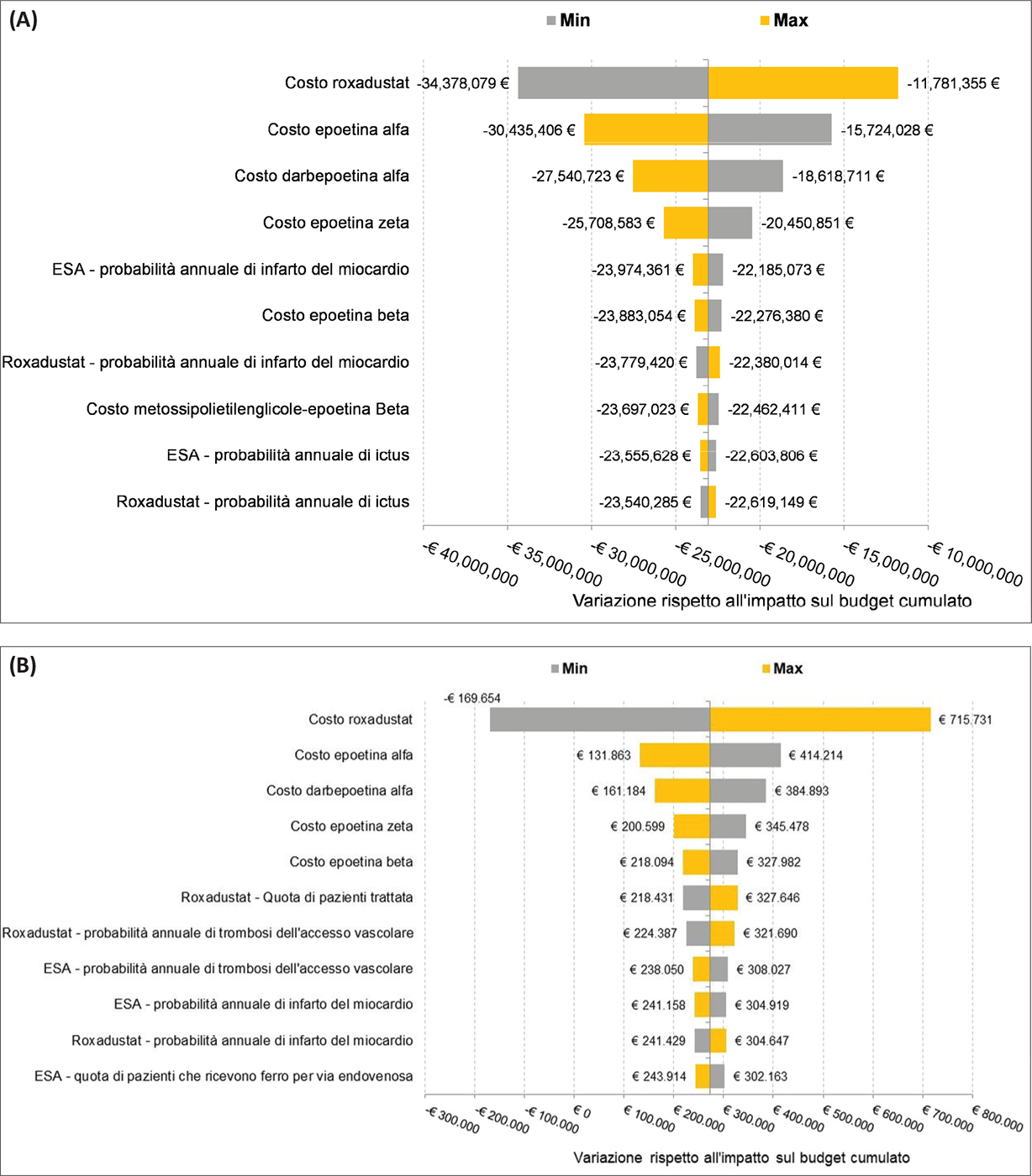
FIGURA 4 - Risultati dell’analisi di sensibilità deterministica: popolazione NDD (4A), popolazione DD (4B).
| Impatto sul budget | |||
|---|---|---|---|
| Ipotesi sconto roxadustat | NDD | DD | NDD e DD |
| 0% | € 33.764.167 | € 1.644.348 | € 35.408.515 |
| 10% | € 28.114.986 | € 1.423.002 | € 29.537.988 |
| 20% | € 22.465.805 | € 1.201.656 | € 23.667.461 |
| 30% | € 16.816.624 | € 980.310 | € 17.796.934 |
| 40% | € 11.167.443 | € 758.963 | € 11.926.406 |
| 50% | € 5.518.262 | € 537.617 | € 6.055.879 |
| 60% | −€ 130.919 | € 316.271 | € 185.352 |
| 70% | −€ 5.780.100 | € 94.924 | −€ 5.685.175 |
| 80% | −€ 11.429.281 | −€ 126.422 | −€ 11.555.702 |
| 90% | −€ 17.078.462 | −€ 347.768 | −€ 17.426.230 |
Nella Tabella 12 sono riportati i risultati dell’analisi di scenario condotta rispetto all’utilizzo delle tre tipologie di ferro per via endovenosa da parte dei pazienti DD e NDD. Assumendo un utilizzo del solo ferro saccarato o del solo ferro gluconato, i risultati dell’analisi di impatto sul budget non si discosterebbero molto dai risultati emersi per il caso-base. Infatti, le variazioni assolute sono contenute in −€ 182.821 per la popolazione NDD e in +€ 66.212 per la popolazione DD.
Discussione
Roxadustat rappresenta il primo della nuova classe degli inibitori di HIF-PH a essere stato approvato in Europa per il trattamento dell’anemia sintomatica associata alla MRC nell’agosto 2021. A livello nazionale, roxadustat è rimborsato da marzo 2023 e sottoposto a prescrizione con piano terapeutico. L’obiettivo di questa analisi è stato quello di valutare l’impatto economico dell’introduzione di roxadustat rispetto alla spesa attualmente sostenuta dal SSN per la gestione e il trattamento dei pazienti con anemia da MRC. Dato l’obiettivo puramente economico dello studio, aspetti quali la valutazione degli outcome di lungo termine e la prospettiva del paziente in termini di qualità della vita, di preferenze di trattamento, di aderenza e di soddisfazione circa il trattamento ricevuto non sono stati valutati nell’ambito di questa analisi. In linea con l’obiettivo dello studio, attraverso lo sviluppo di un modello economico si è tentato di fornire una stima dei costi associati ai pazienti NDD e DD sia per lo scenario in cui roxadustat risulta assente sul mercato che per lo scenario in cui roxadustat risulta presente. In assenza di roxadustat, la spesa annua associata alla gestione e al trattamento dei pazienti con anemia da MRC in Italia per i tre anni di analisi è risultata pari a circa € 86,8 e € 14,9 milioni rispettivamente per i pazienti NDD e DD; per lo scenario in cui roxadustat risulta presente sul mercato, per i pazienti NDD tale spesa annua è risultata pari a € 84,5 milioni, a € 79,2 milioni e a € 73,7 milioni in corrispondenza del primo, del secondo e del terzo anno di analisi, mentre, per i pazienti DD, è risultata pari a € 14,9 milioni in corrispondenza del primo anno di analisi e pari a circa € 15 milioni per il secondo e il terzo anno di analisi. Il differenziale di spesa tra questi due scenari mostra come la presenza di roxadustat sul mercato potrebbe generare un risparmio della spesa a carico del SSN pari a circa € 2,3 milioni, € 7,6 milioni e € 13,2 milioni rispettivamente al primo, al secondo e al terzo anno di analisi per i pazienti NDD e un incremento pari a circa € 27.304, € 90.103 e € 155.632 rispettivamente al primo, al secondo e al terzo anno di analisi per i pazienti DD.
| DD | NDD | |||||
|---|---|---|---|---|---|---|
| Caso base | Scenario 1 | Scenario 2 | Caso base | Scenario 1 | Scenario 2 | |
| Utilizzo del ferro saccarato | 0% | 100% | 0% | 0% | 100% | 0% |
| Utilizzo del ferro carbossimaltosio | 95% | 0% | 0% | 99% | 0% | 0% |
| Utilizzo del ferro gluconato | 5% | 0% | 100% | 1% | 0% | 100% |
| Impatto sul budget cumulato a tre anni | € 237.038 | € 252.291 | € 303.250 | −€ 23.079.717 | −€ 23.262.538 | −€ 23.075.265 |
| ∆ vs caso-base
(%) |
– | € 15.253
(+6,4%) |
€ 66.212
(+29,9%) |
– | −€ 182.821
(−0,8%) |
€ 4.452
(+0,01%) |
L’analisi di scenario che ha utilizzato i prezzi gara per gli ESA mostra che il risparmio per il SSN permane per sconti di roxadustat pari almeno al 60,3%.
Una recente revisione sistematica della letteratura, condotta al fine di valutare i costi e la qualità della vita associati al trattamento dell’anemia da MRC in pazienti DD, ha mostrato come ai pazienti trattati con ESA risultino associati costi inferiori e un minore utilizzo di risorse sanitarie rispetto ai pazienti non trattati con ESA (40). Tra gli studi inclusi, lo studio di Moyneur et al. (41), condotto al fine di quantificare i costi incrementali diretti e indiretti associati alla terapia con ESA in pazienti con anemia da MRC nella fase prima della dialisi, ha fatto emergere come il costo mensile per paziente trattato con ESA sia risultato inferiore rispetto a quello stimato per il paziente non trattato con ESA, sia in termini di costi diretti (-$ 852) che in termini di costi indiretti (-$ 308) (analisi di regressione multivariata, p < 0,001). Inoltre, i costi diretti stimati nei primi 6 mesi di dialisi per i pazienti in trattamento con ESA sono risultati inferiori rispetto a quelli stimati per i pazienti non in trattamento; in particolare, per il paziente trattato è stata osservata una riduzione mensile dei costi diretti pari a $ 1.515 (analisi di regressione multivariata, p = 0,0267).
Pur utilizzando un target di Hb diverso da quello raccomandato dalle Linee Guida internazionali, lo studio di Liu et al. (42) ha inoltre mostrato come il mancato raggiungimento di un target di Hb pari a 11 g/dL possa avere implicazioni negative dal punto di vista economico: all’aumentare del tempo trascorso con un livello di Hb < 11 g/dL aumentano le spese mediche e l’impiego di risorse sanitarie ($ 5.461 con Hb < 11 g/dL+L a 0 mesi, $ 6.276 con Hb < 11 g/dL+L per un periodo pari a 1-2 mesi, $ 8.070 con Hb < 11 g/dL+L per un periodo ≥ 3 mesi).
La presente analisi ha mostrato come l’introduzione di roxadustat sul mercato possa generare un risparmio della spesa a carico del SSN per i pazienti con anemia da MRC; tale risparmio risulta attribuibile principalmente alla riduzione della spesa farmaceutica per i pazienti NDD e alla riduzione dei costi associati alla supplementazione del ferro e alle trasfusioni per i pazienti sia NDD che DD. È importante sottolineare che i risultati di questo studio non sono generalizzabili ad altri Paesi in quanto il numero di pazienti in trattamento e i costi considerati all’interno dell’analisi fanno riferimento al contesto nazionale e potrebbero dunque differire tra i diversi Paesi.
Dalla letteratura emerge come il mancato raggiungimento di target adeguati di Hb comporti costi superiori per la gestione dei pazienti con anemia da MRC.
Tale modello economico tenta di ripercorrere in maniera sintetica e semplificata il percorso di gestione e trattamento dei pazienti con anemia da MRC in Italia, al fine di stimare l’impatto che l’introduzione sul mercato di roxadustat avrebbe sulla spesa a carico del SSN. Tale modellizzazione, come ogni tentativo di rappresentazione sintetica della realtà, risulta caratterizzata da alcuni limiti. In primo luogo, con riferimento alla stima dei costi di acquisizione dei trattamenti in analisi, sono stati impiegati i prezzi da Gazzetta Ufficiale; per tale ragione, è stata condotta un’analisi di scenario per avvicinarsi maggiormente alla spesa reale sostenuta dal SSN per l’acquisizione dei farmaci, che ha utilizzato una stima della media dei prezzi gara di appalto per gli ESA e diverse ipotesi di sconto non trasparente per roxadustat. Tale analisi di scenario ha a sua volta dei limiti, che derivano dalla variabilità intrinseca dei prezzi gara, poiché questi per loro natura possono variare nel tempo e nei vari territori.
Un ulteriore limite dell’analisi potrebbe riguardare la posologia considerata per l’epoetina alfa. I dati utilizzati potrebbero non rappresentare la reale pratica clinica dato che la posologia utilizzata in fase conservativa usualmente è inferiore rispetto a quella dei pazienti in dialisi e questo potrebbe generare delle distorsioni nelle stime. Tuttavia, tali stime sono state testate mediante l’analisi di sensibilità, la quale ha fatto emergere come, assumendo una riduzione del 20% della posologia dell’epoetina alfa per la popolazione in conservativa si otterrebbe una riduzione di spesa a 3 anni di analisi pari a −€ 15,7 milioni (vs −€23,1 milioni del caso-base). Viceversa, assumendo un aumento del 20% della posologia dell’epoetina alfa per la popolazione in dialisi, si otterrebbe un incremento di spesa a 3 anni di analisi pari a € 131.863 (vs € 273.038 del caso-base).
Con riferimento alla stima dei costi di gestione della malattia, all’interno dell’analisi non si è tenuto conto dei costi associati alla quota di pazienti non in trattamento; tali costi risulteranno dunque sottostimati in termini di burden economico complessivo associato alla malattia, senza però creare variazioni a livello di impatto sul budget. Inoltre, in assenza di informazioni pubblicate rispetto al contesto nazionale circa la frequenza con cui i pazienti si sottopongono all’emodialisi e alla dialisi peritoneale, all’interno del modello economico è stata utilizzata la frequenza di utilizzo settimanale riportata dal Registro Dialisi e Trapianti della Regione Lazio (39); va però sottolineato come i dati provenienti dalla Regione Lazio potrebbero non essere necessariamente rappresentativi della realtà di altre Regioni italiane. Un ulteriore limite dell’analisi consiste nelle assunzioni effettuate per i pazienti in trattamento con roxadustat laddove non fossero disponibili informazioni; in particolare, in assenza di informazioni per roxadustat circa la somministrazione del ferro orale, la quota di pazienti a cui viene somministrato il ferro orale tra i pazienti in trattamento con ESA è stata assunta anche per i pazienti in trattamento con roxadustat. Inoltre, con riferimento alla frequenza con cui i pazienti si sottopongono a visite di routine o specialistiche, per i pazienti in trattamento con roxadustat tale frequenza è stata assunta pari a quella osservata per i pazienti in trattamento con ESA. Con riferimento ai pazienti DD, la quota di pazienti in trattamento con roxadustat e con ESA che assumono ferro per via endovenosa e la dose media annua di ferro per via endovenosa assunta dai pazienti che effettivamente assumono ferro per via endovenosa, in assenza di informazioni, sono state stimate effettuando delle assunzioni a partire dai dati dello studio clinico HIMALAYAS; tali variazioni sono state testate all’interno dell’analisi di sensibilità deterministica, la quale non ha fatto emergere un impatto importante di tali stime sui risultati del modello. Infine, sempre in riferimento ai pazienti DD, non è stato possibile quantificare il numero di pazienti sottoposti a dialisi bisettimanale e si è assunto che tutti i pazienti ricevano emodialisi trisettimanale; questa assunzione influisce sui risultati dei singoli scenari, ma in egual modo fra scenario senza e con roxadustat, e quindi non incide sui risultati di impatto sul budget.
L’utilizzo della terapia con roxadustat in pazienti iporesponsivi agli ESA e che quindi necessitano di un alto dosaggio con conseguenti alti costi per le eritropoietine potrebbe essere una scelta teoricamente vantaggiosa dal punto di vista economico. Tuttavia, i dati scientifici a supporto sono ancora solo preliminari e l’attuale piano terapeutico, impedendo il passaggio a roxadustat per i pazienti già in terapia con ESA, rende tale scenario al momento non rappresentativo del mondo reale.
Un ulteriore limite dell’analisi consiste nel fatto che, con riferimento alla dialisi, la percentuale di pazienti che iniziano la dialisi (circa il 7%) e la distribuzione dei pazienti tra coloro che effettuano l’emodialisi e la dialisi peritoneale sono state assunte uguali tra i pazienti in trattamento con roxadustat e con ESA. Inoltre, le quote di mercato potrebbero non essere rappresentative dei singoli territori regionali, in quanto queste sono state definite sulla base di fonti che descrivono il comportamento nazionale.
Infine, un ulteriore limite importante è che non esistono dati nazionali completi di epidemiologia della MRC e dell’anemia della MRC e del suo trattamento; lo stesso Registro Italiano di Dialisi e Trapianto non raccoglie i dati di tutte le Regioni.
I risultati ottenuti da questo studio risentono ovviamente dei dati di ingresso e delle assunzioni che sono state effettuate e che sono alla base del modello economico. Tuttavia, tali parametri sono stati testati tramite l’analisi di sensibilità che mostra la variazione dei risultati dell’analisi in funzione della variazione degli input.
Conclusioni
L’anemia rappresenta una delle complicanze clinicamente più rilevanti della MRC. Il mancato trattamento o bassi livelli di Hb sono associati, oltre al peggioramento della situazione clinica del paziente, a un aumento dei costi sanitari. L’introduzione del trattamento con roxadustat comporta una riduzione della spesa associata alla supplementazione di ferro, della spesa associata alle trasfusioni e della spesa per l’acquisizione dei farmaci anti-anemici. L’analisi di scenario mostra che, anche considerando i prezzi gara per gli ESA, il risparmio per il SSN permane per sconti di roxadustat maggiori del 60,3%.
Disclosures
Conflict of interest: LDV received honoraria for lectures indirectly supported by Vifor Pharma and Astellas Pharma. LDV is member of the council of the Italian Society of Nephrology. PDR is an employee of Astellas Pharma Italia SpA. CB and AM declare that they have no conflicts of interest.
Financial support: This study was initiated and funded by Astellas Pharma Italia SpA. No honoraria were given for the publication.
Authors’ contributions: CB and AM: Conceptualization; Data Curation; Methodology; Formal Analysis; Investigation; Writing – Original Draft. PDR: Conceptualization; Resources; Funding acquisition; Writing – review & editing. LDV: Resources; Validation; Writing – review & editing.
Bibliografia
- 1. WHO. Haemoglobin concentrations for the diagnosis of anaemia and assessment of severity Vitamin and Mineral Nutrition Information System. Geneva, World Health Organization, 2011 (WHO/NMH/NHD/MNM/11.1). Online (Accessed March 2024)
- 2. Mennini FS. M.A., Viti R, Bini C, Maffei P, Pivonello R, Analisi di impatto di budget di pasireotide in pazienti con acromegalia nella prospettiva del Sistema Sanitario Nazionale. IN PUBBLICATION; 2016.
- 3. Cases-Amenós A, Martínez-Castelao A, Fort-Ros J, et al; Investigadores del Estudio Micenas I. Prevalence of anaemia and its clinical management in patients with stages 3-5 chronic kidney disease not on dialysis in Catalonia: MICENAS I study. Nefrologia. 2014;34(2):189-198. PubMed
- 4. De Nicola L, Minutolo R, Chiodini P, et al; SIN-TABLE CDK Study Group. Prevalence and prognosis of mild anemia in non-dialysis chronic kidney disease: a prospective cohort study in outpatient renal clinics. Am J Nephrol. 2010;32(6):533-540. CrossRef PubMed
- 5. Minutolo R, Locatelli F, Gallieni M, et al; REport of COmorbidities in non-Dialysis Renal Disease Population in Italy (RECORD-IT) Study Group. Anaemia management in non-dialysis chronic kidney disease (CKD) patients: a multicentre prospective study in renal clinics. Nephrol Dial Transplant. 2013;28(12):3035-3045. CrossRef PubMed
- 6. Wong MMY, Tu C, Li Y, et al; CKDopps Investigators. Anemia and iron deficiency among chronic kidney disease Stages 3-5ND patients in the Chronic Kidney Disease Outcomes and Practice Patterns Study: often unmeasured, variably treated. Clin Kidney J. 2019;13(4):613-624. CrossRef PubMed
- 7. Portolés J, Gorriz JL, Rubio E, et al; NADIR-3 Study Group. The development of anemia is associated to poor prognosis in NKF/KDOQI stage 3 chronic kidney disease. BMC Nephrol. 2013;14(2):2. CrossRef PubMed
- 8. DOPPS Practice Monitor-Hemodialysis DPM. Online. (Accessed March 2024)
- 9. Toft G, Heide-Jørgensen U, van Haalen H, et al. Anemia and clinical outcomes in patients with non-dialysis dependent or dialysis dependent severe chronic kidney disease: a Danish population-based study. J Nephrol. 2020;33(1):147-156. CrossRef PubMed
- 10. Minutolo R, Provenzano M, Chiodini P, et al; Collaborative Study Group on the Conservative Treatment of CKD of the Italian Society of Nephrology. New-onset anemia and associated risk of ESKD and death in non-dialysis CKD patients: a multicohort observational study. Clin Kidney J. 2022;15(6):1120-1128. CrossRef PubMed
- 11. De Nicola L, Chiodini P, Zoccali C, et al; SIN-TABLE CKD Study Group. Prognosis of CKD patients receiving outpatient nephrology care in Italy. Clin J Am Soc Nephrol. 2011;6(10):2421-2428. CrossRef PubMed
- 12. Cianciaruso B, Pota A, Bellizzi V, et al. Effect of a low- versus moderate-protein diet on progression of CKD: follow-up of a randomized controlled trial. Am J Kidney Dis. 2009;54(6):1052-1061. CrossRef PubMed
- 13. Coyne DW, Goldsmith D, Macdougall IC. New options for the anemia of chronic kidney disease. Kidney Int Suppl (2011). 2017 Dec;7(3):157-163. doi: CrossRef PubMed
- 14. Kidney Disease: Improving Global Outcomes (KDIGO), KDIGO Clinical Practice Guideline for Anemia in Chronic Kidney Disease. Kidney Int Suppl. 2012;2:279-335. Online (Accessed March 2024)
- 15. Szczech LA, Barnhart HX, Inrig JK, et al. Secondary analysis of the CHOIR trial epoetin-alpha dose and achieved hemoglobin outcomes. Kidney Int. 2008;74(6):791-798. CrossRef PubMed
- 16. Bae MN, Kim SH, Kim YO, et al. Association of Erythropoietin-Stimulating Agent Responsiveness with Mortality in Hemodialysis and Peritoneal Dialysis Patients. PLoS One. 2015;10(11):e0143348. CrossRef PubMed
- 17. Fujii H, Hamano T, Tsuchiya K, et al; PARAMOUNT Study Investigators. Not baseline but time-dependent erythropoiesis-stimulating agent responsiveness predicts cardiovascular disease in hemodialysis patients receiving epoetin beta pegol: A multicenter prospective PARAMOUNT-HD Study. Int J Cardiol. 2023;375:110 118. CrossRef PubMed
- 18. Locatelli F, et al. Il trattamento dell’anemia del paziente con malattia renale cronica: dopo un viaggio lungo oltre 30 anni quali evidenze supportano la scelta motivata di un ESA? G Ital Nefrol. 2020;4(5).
- 19. Locatelli F, Del Vecchio L. Hypoxia-Inducible Factor-Prolyl Hydroxyl Domain Inhibitors: From Theoretical Superiority to Clinical Noninferiority Compared with Current ESAs? J Am Soc Nephrol. 2022;33(11):1966-1979. CrossRef PubMed
- 20. Provenzano R, Shutov E, Eremeeva L, et al. Roxadustat for anemia in patients with end-stage renal disease incident to dialysis. Nephrol Dial Transplant. 2021;36(9):1717-1730. CrossRef PubMed
- 21. Mauskopf JA, Sullivan SD, Annemans L, et al. Principles of good practice for budget impact analysis: report of the ISPOR Task Force on good research practices--budget impact analysis. Value Health. 2007;10(5):336-347. CrossRef PubMed
- 22. Sullivan SD, Mauskopf JA, Augustovski F, et al. Budget impact analysis-principles of good practice: report of the ISPOR 2012 Budget Impact Analysis Good Practice II Task Force. Value Health. 2014;17(1):5-14. CrossRef PubMed
- 23. European Medicines Agency (EMA). RCP Roxadustat. Online. (Accessed March 2024)
- 24. ISTAT. Popolazione residente per sesso, età e stato civile al 1° Gennaio 2022. Online. (Accessed March 2024)
- 25. De Nicola L, Donfrancesco C, Minutolo R, et al; ANMCO-SIN Research Group. Prevalence and cardiovascular risk profile of chronic kidney disease in Italy: results of the 2008-12 National Health Examination Survey. Nephrol Dial Transplant. 2015;30(5):806-814. CrossRef PubMed
- 26. Viscogliosi G, De Nicola L, Vanuzzo D, Giampaoli S, Palmieri L, Donfrancesco C; HES Research Group. Mild to moderate chronic kidney disease and functional disability in community-dwelling older adults. The Cardiovascular risk profile in Renal patients of the Italian Health Examination Survey (CARHES) study. Arch Gerontol Geriatr. 2019;80:46-52. CrossRef PubMed
- 27. The CAPRI study: CKD Anemia Prevalence, Incidence, treatment patterns and healthcare resource utilization in non dialysis patients in Italy. A retrospective study of electronic medical records.”. 2021.(Astellas Data on File)
- 28. Real World Analysis on administrative database – Anemia in dialysis dependent CKD patients. 2021.(Astellas Data on File)
- 29. Barratt J, Andric B, Tataradze A, et al. Roxadustat for the treatment of anaemia in chronic kidney disease patients not on dialysis: a Phase 3, randomized, open-label, active-controlled study (DOLOMITES). Nephrol Dial Transplant. 2021;36(9):1616-1628. CrossRef PubMed
- 30. Decreto del Ministero della Salute 18 ottobre 2012. Tariffe delle prestazioni di assistenza specialistica ambulatoriale. Online. (Accessed March 2024)
- 31. Fliser D, Mata Lorenzo M, Houghton K, et al. Real-Life Anemia Management Among Patients with Non-Dialysis-Dependent Chronic Kidney Disease in Three European Countries. Int J Nephrol Renovasc Dis. 2023;16:115-129. CrossRef PubMed
- 32. Cases A, Sánchez EGA, Cadeddu G, Lorenzo MM. Epidemiology and treatment of renal anaemia in Spain: RIKAS retrospective study. Nefrologia (Engl Ed). 2023;43(5):562-574. CrossRef PubMed
- 33. Theidel U, Asseburg C, Giannitsis E, Katus H. Cost-effectiveness of ticagrelor versus clopidogrel for the prevention of atherothrombotic events in adult patients with acute coronary syndrome in Germany. Clin Res Cardiol. 2013;102(6):447-458. CrossRef PubMed
- 34. Lok CE, Bhola C, Croxford R, Richardson RM. Reducing vascular access morbidity: a comparative trial of two vascular access monitoring strategies. Nephrol Dial Transplant. 2003;18(6):1174-1180. CrossRef PubMed
- 35. Decreto del Ministero della Salute 18 ottobre 2012. Tariffe delle prestazioni di assistenza ospedaliera per acuti, per tipo di ricovero. Online. (Accessed March 2024)
- 36. Ministero della Salute. Rapporto annuale sull’attività di ricovero ospedaliero. Dati SDO 2019. Online. (Accessed March 2024)
- 37. Sciattella P, et al. Rehospitalization due to subsequent cardiovascular events in secondary prevention patients treated with lipid lowering therapies in Italy. Poster PCV84. 2019; Online. (Accessed March 2024)
- 38. Registro Italiano di Dialisi e Trapianto. Report 2017. Online. (Accessed March 2024)
- 39. Dipartimento di Epidemiologia Lazio. Registro Dialisi e Trapianto Lazio. Rapporto 2019. Online. (Accessed March 2024)
- 40. Spinowitz B, Pecoits-Filho R, Winkelmayer WC, et al. Economic and quality of life burden of anemia on patients with CKD on dialysis: a systematic review. J Med Econ. 2019;22(6):593-604. CrossRef PubMed
- 41. Moyneur E, Bookhart BK, Mody SH, Fournier AA, Mallett D, Duh MS. The economic impact of pre-dialysis epoetin alpha on health care and work loss costs in chronic kidney disease: an employer’s perspective. Dis Manag. 2008;11(1):49-58. CrossRef PubMed
- 42. Liu J, Guo H, Gilbertson D, Foley R, Collins A. Associations of anemia persistency with medical expenditures in Medicare ESRD patients on dialysis. Ther Clin Risk Manag. 2009;5(4):319-330. CrossRef PubMed
- 43. Gazzetta Ufficiale n.48 del 25/02/2023. Online. (Accessed March 2024)
- 44. Farmadati. Last Access Date: 30/09/2023. Online.
- 45. Roxadustat Vs ESAs in Dialysis-Dependent Chronic Kidney Disease: pooled analysis of four Phase 3 studies. 2021. (Astellas Data on File)
- 46. Csiky B, Schömig M, Esposito C, et al. Roxadustat for the Maintenance Treatment of Anemia in Patients with End-Stage Kidney Disease on Stable Dialysis: A European Phase 3, Randomized, Open-Label, Active-Controlled Study (PYRENEES). Adv Ther. 2021;38(10):5361-5380. CrossRef PubMed
- 47. Agenzia Italiana del Farmaco (AIFA). Riassunto delle caratteristiche del prodotto NeoRecormon. Online. (Accessed March 2024)
- 48. Agenzia Italiana del Farmaco (AIFA). Riassunto delle caratteristiche del prodotto Mircera. Online. (Accessed March 2024)
- 49. Analisi prezzi medi gare ospedaliere su dato IHS (Information Hospital Service).(Astellas Data on File)