 |
Glob Reg Health Technol Assess 2024; 11: 94-100 ISSN 2283-5733 | DOI: 10.33393/grhta.2024.3013 ORIGINAL RESEARCH ARTICLE |
 |
Scompenso cardiaco e impatto economico: un’analisi nella reale pratica clinica in Italia
Heart failure and economic impact: an analysis in real clinical practice in Italy
Introduction: Heart failure (HF) affects 1% of subjects aged 45-55 and over 10% of subjects aged ≥ 80 and in Italy represents the third leading cause of hospitalization.
Objective: To analyse the clinical and economic burden of HF in the Italian real clinical practice.
Methods: A retrospective analysis was conducted on the administrative databases of healthcare institutions for 4.2 million health-assisted residents. Between January 2012 and March 2021, patients with a hospital discharge diagnosis for HF were included. Among healthcare utilization and costs, treatments, hospitalizations, and specialist services were evaluated. The HF group was compared with a population without HF (no-HF) similar for age, sex distribution, and cardiovascular risk factors.
Results: The same number of patients with (N = 74,085) and without HF (N = 74,085) was included. A profile of cardiovascular comorbidities emerged in the HF group, mainly hypertension (88.6%), cardiovascular disease (61.3%) and diabetes (32.1%). Hospitalizations from any cause were 635.6 vs 429.8/1,000 person-year in the HF vs no-HF group. At one-year follow-up, all-cause mortality was 24.9% in HF patients and 8.4% in no-HF. Resource utilization/patient was respectively 26.8 ± 15.9 vs 17.1 ± 12.5 for medications, 0.8 ± 1.2 vs 0.3 ± 0.8 for hospitalizations, and 9.4 ± 12.6 vs 6.5 ± 9.8 for specialist services. This resource utilization resulted in significantly higher total healthcare costs in the HF group vs no-HF group (€ 5,910 vs € 3,574, p < 0.001), mainly related to hospitalizations (€ 3,702 vs € 1,958).
Conclusions: HF patients show a significantly higher clinical and economic burden than no-HF, with total healthcare costs being about 1.7 times the costs of the no-HF group.
Keywords: Cardiovascular comorbidities, Healthcare costs, Heart failure, Hospitalizations
Received: December 22, 2023
Accepted: February 28, 2024
Published online: April 22, 2024
This article includes supplementary materials.
Global & Regional Health Technology Assessment - ISSN 2283-5733 - www.aboutscience.eu/grhta
© 2024 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
Lo scompenso cardiaco (SC) è caratterizzato da una disfunzione ventricolare che porta a una ridotta gittata cardiaca e alla comparsa di manifestazioni cliniche quali dispnea, edema degli arti inferiori, astenia, affaticamento e debolezza (1). A livello mondiale, tale patologia colpisce il 2-3% della popolazione, con numeri sensibilmente maggiori negli anziani e un’incidenza che raddoppia per ogni decade a partire dai 45 anni (2).
In Italia lo SC rappresenta la terza causa di ospedalizzazione nella popolazione generale, ma è la prima nei soggetti di oltre 65 anni; inoltre, lo SC si associa a una mortalità intraospedaliera del 5-7% (3). Le recenti Linee Guida dell’Istituto Superiore di Sanità (ISS) raccomandano che il percorso diagnostico e terapeutico del paziente con SC debba prevedere un approccio multidisciplinare con il contributo di figure quali cardiologo, infermiere con competenze avanzate in SC, medico internista/geriatra, medico di medicina generale, specialista di cure palliative e medicina riabilitativa, psicologo e caregiver per assistenza sociale/domiciliare (4).
Lo SC rappresenta un’importante emergenza di salute a livello mondiale e una sfida aperta per i sistemi sanitari in ragione dell’elevato impegno di risorse e dei relativi costi (5-9). Come sottolineato dalle più recenti Linee Guida pubblicate nel 2021 dalla Società Europea di Cardiologia (ESC) (10) e dal successivo aggiornamento del 2023 (11), i pazienti con SC vanno spesso incontro a episodi di esacerbazione e presentano con elevata frequenza diverse comorbilità cardiovascolari e non cardiovascolari. Tra le prime, quelle più frequenti sono ipertensione arteriosa, malattia coronarica, malattia ischemica periferica e cerebrovascolare, aritmie e cardiopatia valvolare, mentre tra le patologie non cardiovascolari spesso associate a SC rientrano quelle respiratorie come la broncopneumopatia cronica ostruttiva (BPCO), quelle endocrine (disfunzioni tiroidee, diabete mellito) e quelle emopoietiche e l’insufficienza renale (12-15). Questo complesso stato clinico comporta la necessità di ricoveri ospedalieri multipli, soprattutto oltre i 65 anni d’età (16,17). Inoltre, lo SC è una condizione clinica caratterizzata da un alto tasso di mortalità che, come stimato dal registro dell’European Society of Cardiology Heart Failure, risulterebbe del 23,6% per i pazienti ospedalizzati e durante il primo anno di follow-up (18).
Lo SC si ripercuote significativamente anche sullo stato psicologico dell’individuo, che si traduce in una compromissione significativa della qualità della vita e nella necessità di assistenza di operatori sanitari o caregiver. Diverse evidenze hanno indicato come l’ottimizzazione della terapia per lo SC, l’educazione all’aderenza ai farmaci e la gestione domiciliare dei trattamenti quotidiani senza il supporto continuo dei caregiver possano rappresentare degli obiettivi cardine da conseguire per ridurre il numero di ospedalizzazioni con i relativi costi per il SSN e auspicabilmente anche la mortalità.
La presente analisi condotta in un contesto di reale pratica clinica ha la finalità di analizzare le caratteristiche demografiche e cliniche della popolazione con SC in Italia e il tasso di ospedalizzazioni e mortalità con il relativo burden economico a carico del Servizio Sanitario Nazionale (SSN).
Metodi
Fonte dei dati
È stata condotta un’analisi retrospettiva integrando i database amministrativi di un pool di enti sanitari italiani geograficamente distribuiti sul territorio nazionale equivalenti a quasi 4,2 milioni di residenti. I dati sono stati estratti dai seguenti database: (i) archivio anagrafe assistibili, per le caratteristiche demografiche (sesso, età) e l’eventuale data di decesso; (ii) database dell’assistenza farmaceutica territoriale, per le informazioni sui medicinali in regime di rimborsabilità da parte del SSN, identificati mediante il codice Anatomico Terapeutico Chimico (ATC), sul numero di confezioni, sul numero di unità per confezione, sul costo unitario per confezione e sulla data di prescrizione; (iii) database delle “schede di dimissione ospedaliera”, per le ricerca delle diagnosi principali e accessorie, codificate secondo il codice ICD-9-CM (International Classification of Diseases, IX Revisione, Clinical Modification) e la data di diagnosi; (iv) database delle prestazioni specialistiche ambulatoriali, per i dati sull’erogazione di visite specialistiche ed esami diagnostici (data, tipo, costo dell’attività); (v) archivio delle esenzioni per patologia, che riporta i codici delle esenzioni assegnate ai pazienti sulla base di patologie diagnosticate e la data di esenzione.
In ottemperanza alla normativa sulla privacy (GDPR 2016/679), ai soggetti incaricati del trattamento dei dati non è stata fornita alcuna informazione che consentisse di risalire in modo diretto o indiretto all’identità del paziente. Tutti i risultati comprendono solo ed esclusivamente dati aggregati mai riconducibili al singolo assistito. Ad ogni paziente incluso è stato assegnato un codice univoco anonimo al fine di collegare le informazioni contenute nei diversi database mediante data-linkage. Sulla base dell’attuale normativa vigente in materia di conduzione di analisi osservazionali, il protocollo dell’analisi è stato sottomesso ai comitati etici locali degli enti sanitari coinvolti e approvato da essi.
Identificazione della popolazione con scompenso cardiaco
Criteri di inclusione e di esclusione. Tra gennaio 2012 e marzo 2021, sono stati inclusi pazienti adulti (≥ 18 anni) con almeno una diagnosi di dimissione ospedaliera di primo e secondo livello per SC identificata mediante codice ICD-9-CM 428. La data del primo ricovero ospedaliero per SC è stata considerata come data-indice e l’analisi ha compreso tutto l’intervallo di dati disponibili precedente e successivo alla data-indice, purché non inferiore a un anno, vale a dire periodo di caratterizzazione e di follow-up, rispettivamente. I pazienti senza inclusione continua nel corso del periodo di osservazione (per esempio, per trasferimento a un’altra regione) sono stati esclusi dall’analisi.
Caratteristiche demografiche e cliniche. Per la popolazione inclusa nello studio, sono state raccolte le caratteristiche al baseline. Le variabili demografiche erano l’età alla data-indice, le fasce d’età (18-24 anni, 25-34 anni, 35-44 anni, 45-54 anni, 55-64 anni, 65-74 anni, 75-84 anni, ≥85 anni) e la distribuzione dei sessi, espressa come percentuale di maschi. Il profilo clinico dei pazienti è stato esaminato mediante il Charlson Comorbidity Index (CCI), uno score aspecifico per valutare la mortalità a 10 anni sulla base del “peso” di 19 malattie concomitanti (19). Nella presente analisi, tuttavia, è stata utilizzata una versione adattata del CCI, escludendo dal calcolo le patologie cardiovascolari, vale a dire infarto miocardico, insufficienza cardiaca, malattia cerebrovascolare e malattia vascolare periferica. Inoltre, per descrivere lo status clinico del paziente sulla base delle comorbilità più frequentemente associate allo SC (13,14), durante tutto il periodo di caratterizzazione sono state ricercate le seguenti diagnosi: ipertensione, diabete mellito, malattie cardiovascolari, iperlipidemia, BPCO, apnea ostruttiva del sonno e apnea centrale del sonno, malattia renale cronica (MRC), anemia, malattie della tiroide, depressione, osteoartrite e osteoporosi. L’elenco dettagliato delle comorbilità analizzate nei pazienti con SC durante il periodo di caratterizzazione e i codici utilizzati come proxy di diagnosi sono riportati nella Tabella S1 del materiale supplementare. Durante il follow-up, i tassi di ospedalizzazione sono stati stimati per anno per persona, in termini di ricoveri da tutte le cause (ordinari e in day hospital) e di ricoveri da causa cardiovascolare (ordinari e in day hospital). Inoltre, il tasso di mortalità è stato stimato durante il ricovero indice e durante il primo anno di follow-up e riportato come percentuale di pazienti deceduti.
Consumi di risorse sanitarie e costi diretti per il SSN
L’utilizzo di risorse sanitarie per paziente vivo al primo anno di follow-up ha preso in esame il numero di prescrizioni di farmaci, il numero di ricoveri ospedalieri (ordinari e in day hospital) e il numero di prestazioni specialistiche ambulatoriali (esami di laboratorio, visite specialistiche, procedure diagnostiche). I costi diretti totali medi sostenuti dal SSN sono stati calcolati tenendo conto delle voci di spesa citate sopra.
Analisi statistica
È stata condotta un’analisi statistica descrittiva. Le variabili continue sono presentate come media ± deviazione standard (DS), mentre quelle categoriche come numeri e percentuali.
Al fine di avere un gruppo di controllo, sono stati selezionati pazienti senza SC, comparabili per età, sesso e patologie cardiovascolari, metaboliche e renali (in termini di frequenza di ipertensione, diabete, malattie cardiovascolari, iperlipidemia e MRC). Su tale coorte sono state esaminate, per l’anno 2019, le stesse variabili della popolazione con SC, vale a dire i tassi di ospedalizzazione e di mortalità, l’utilizzo complessivo delle risorse sanitarie e i costi. Per l’analisi dei costi, i valori anomali (quelli che superavano di 3 volte la deviazione standard rispetto alla media) sono stati esclusi. Le variabili categoriche sono state analizzate con il test chi-quadrato. Un valore di p < 0,05 è stato considerato statisticamente significativo e tutte le analisi sono state eseguite utilizzando STATA SE, versione 17.0 (StataCorp LLC, College Station, TX, USA).
Risultati
Caratteristiche demografiche e cliniche nei pazienti con e senza SC
Il campione di 4.166.287 assistiti afferenti agli enti partecipanti all’analisi presentava caratteristiche demografiche in termini di distribuzione dei sessi e delle fasce d’età del tutto comparabili con i dati nazionali dell’ISTAT riferiti allo stesso periodo, vale a dire al 1° gennaio 2019 (Tab. S2 del materiale supplementare); pertanto, la rappresentatività del campione in analisi può considerarsi adeguata.
Da tale campione, sono stati poi identificati 99.933 pazienti (2,4%) con un ricovero per SC; di questi, sono stati inclusi 74.085 pazienti con almeno 12 mesi di dati disponibili. La popolazione di controllo è stata selezionata per avere la stessa numerosità, vale a dire 74.085 soggetti senza SC comparabili per variabili demografiche e comorbilità cardiovascolari.
La Tabella 1 riporta le caratteristiche demografiche e cliniche delle coorti con SC e senza SC. Lo SC è stato identificato come diagnosi primaria o secondaria nel 48,4% e nel 51,6% dei pazienti, rispettivamente. Si sono osservate una distribuzione similare dei sessi, un’età tendenzialmente avanzata, in media di 79 anni e una netta preponderanza di anziani, con l’89,6% dei pazienti con SC nelle fasce over 65 anni. Il profilo clinico era gravato da un importante tasso di comorbilità associate al rischio cardiovascolare, soprattutto ipertensione (88,6% dei pazienti con SC), diabete (32,1%) e insufficienza renale cronica (30,4%).
Tassi di ospedalizzazione e mortalità nei pazienti con e senza SC
I tassi di ospedalizzazione osservati nei pazienti con SC nel follow-up, data-indice esclusa, erano circa 1,5 volte superiori rispetto ai controlli (Tab. 2). Di 74.085 pazienti inclusi, 7.562 (10,2%) erano deceduti durante il ricovero indice e, dei restanti sopravviventi, circa un quarto (16.549 su 66.523, corrispondenti al 24,9%) decedeva entro il primo anno di follow-up.
| SC (N = 74.085) | No-SC (N = 74.085) | |
|---|---|---|
| Sesso maschile, n (%) | 36.800 (49,7%) | 36,800 (49,7%) |
| Età (anni), media ± DS | 79,3 ± 11,3 | 78,9 ± 11,4 |
| Gruppi d’età, n (%) | ||
| 18-24 anni | 57 (0,1%) | 57 (0,1%) |
| 25-34 anni | 142 (0,2%) | 142 (0,2%) |
| 35-44 anni | 472 (0,6%) | 472 (0,6%) |
| 45-54 anni | 1.969 (2,7%) | 1.969 (2,7%) |
| 55-64 anni | 5.247 (7,1%) | 5.247 (7,1%) |
| 65-74 anni | 12.560 (17,0%) | 12.560 (17,0%) |
| 75-84 anni | 26.259 (35,4%) | 26.259 (35,4%) |
| ≥ 85 anni | 27.379 (37,0%) | 27.379 (37,0%) |
| CCI*, media ± DS | 1,5 ± 1,5 | 0,9 ± 1,1 |
| CCI = 0, n (%) | 16.664 (22,5%) | 31.778 (42,9%) |
| CCI = 1, n (%) | 25.912 (35,0%) | 25.635 (34,6%) |
| CCI ≥ 2, n (%) | 31.509 (42,5%) | 16.672 (22,5%) |
| Follow-up (anni), media ± DS | 2,3 ± 2,4 | – |
| Diagnosi primaria di SC, n (%) | 35.878 (48,8%) | – |
| Diagnosi secondaria di SC, n (%) | 38.207 (51,6%) | – |
| Profilo di comorbilità, n (%) | ||
| Comorbilità cardiovascolari | ||
| Ipertensione | 65.672 (88,6%) | 65.672 (88,6%) |
| Diabete mellito | 23.797 (32,1%) | 23.797 (32,1%) |
| Malattie cardiovascolari | 45.425 (61,3%) | 45.425 (61,3%) |
| Iperlipidemia | 28.503 (38,5%) | 28.503 (38,5%) |
| MRC | 22.498 (30,4%) | 22.498 (30,4%) |
| BPCO | 25.600 (34,6%) | 13.411 (18,1%) |
| Apnea ostruttiva del sonno e apnea centrale del sonno | 295 (0,4%) | 223 (0,3%) |
| Anemia | 10.466 (14,1%) | 7.768 (10,5%) |
| Malattie della tiroide | 8.968 (12,1%) | 8.750 (11,8%) |
| Depressione | 13.660 (18,4%) | 12.509 (16,9%) |
| Osteoartrite e osteoporosi | 3.493 (4,7%) | 4.684 (6,3%) |
*Nota: per il calcolo del CCI sono state escluse le seguenti comorbilità cardiovascolari: infarto miocardico, insufficienza cardiaca, malattia cerebrovascolare, malattia vascolare periferica.
Abbreviazioni: BPCO, broncopneumopatia cronica ostruttiva; CCI, Charlson Comorbidity Index; MRC, malattia renale cronica.
Analisi dei consumi e dei costi sanitari
Al primo anno di follow-up nella coorte con SC, i consumi medi erano di 26,8 prescrizioni di farmaci, 0,8 ricoveri e 9,4 servizi specialistici per paziente vivo. Per ciascuna delle voci i consumi medi annui per paziente vivo erano più elevati nei pazienti con SC che in quelli senza SC (Tab. 3).
| Pazienti con SC | Pazienti senza SC | ||
|---|---|---|---|
| Periodo di caratterizzazione | Periodo di follow-up | Anno 2019 | |
| Ricoveri ospedalieri | |||
| Tasso di ricoveri ospedalieri da tutte le cause (per 1.000 persone/anno) | 342,8 [340,8-344,9] | 635,6 [631,8-639,3] | 429,8 [425,0-434,6] |
| Tasso di ricoveri ospedalieri da cause cardiovascolari (per 1.000 persone/anno) | 135,9 [134,6-137,2] | 309,3 [306,7-312,0] | 217,0 [213,6-220,5] |
| Tasso di ricoveri ospedalieri per SC (per 1.000 persone/anno) | – | 206,5 [204,3-208,6] | – |
| Mortalità | |||
| Mortalità per tutte le cause (%, durante il ricovero indice per SC) | – | 10,2% | – |
| Mortalità per tutte le cause (%, nei primi 12 mesi di follow-up) | – | 24,9% | 8,4% |
| Numero per anno per paziente (media ± DS) | Pazienti con SC | Pazienti senza SC | |
|---|---|---|---|
| Primo anno del periodo di caratterizzazione | Primo anno di follow-up (N = 49.974) | Anno 2019 (N = 67.916) | |
| Prescrizioni di farmaci | 21,5 ± 14,8 | 26,8 ± 15,9 | 17,1 ± 12,5 |
| Ricoveri ospedalieri (ordinari e day hospital) | 0,5 ± 1,0 | 0,8 ± 1,2 | 0,3 ± 0,8 |
| Prestazioni specialistiche | 7,4 ± 11,1 | 9,4 ± 12,6 | 6,5 ± 9,8 |
Come mostrato nella Figura 1, i costi sanitari totali erano significativamente maggiori nei pazienti con SC rispetto a quelli senza SC (SC vs no-SC: 5.910 € vs 3.574 €, p < 0,001); i ricoveri ospedalieri rappresentavano la voce di spesa più impattante (SC vs no-SC: 3.702 € vs 1.958 €, p < 0,001).
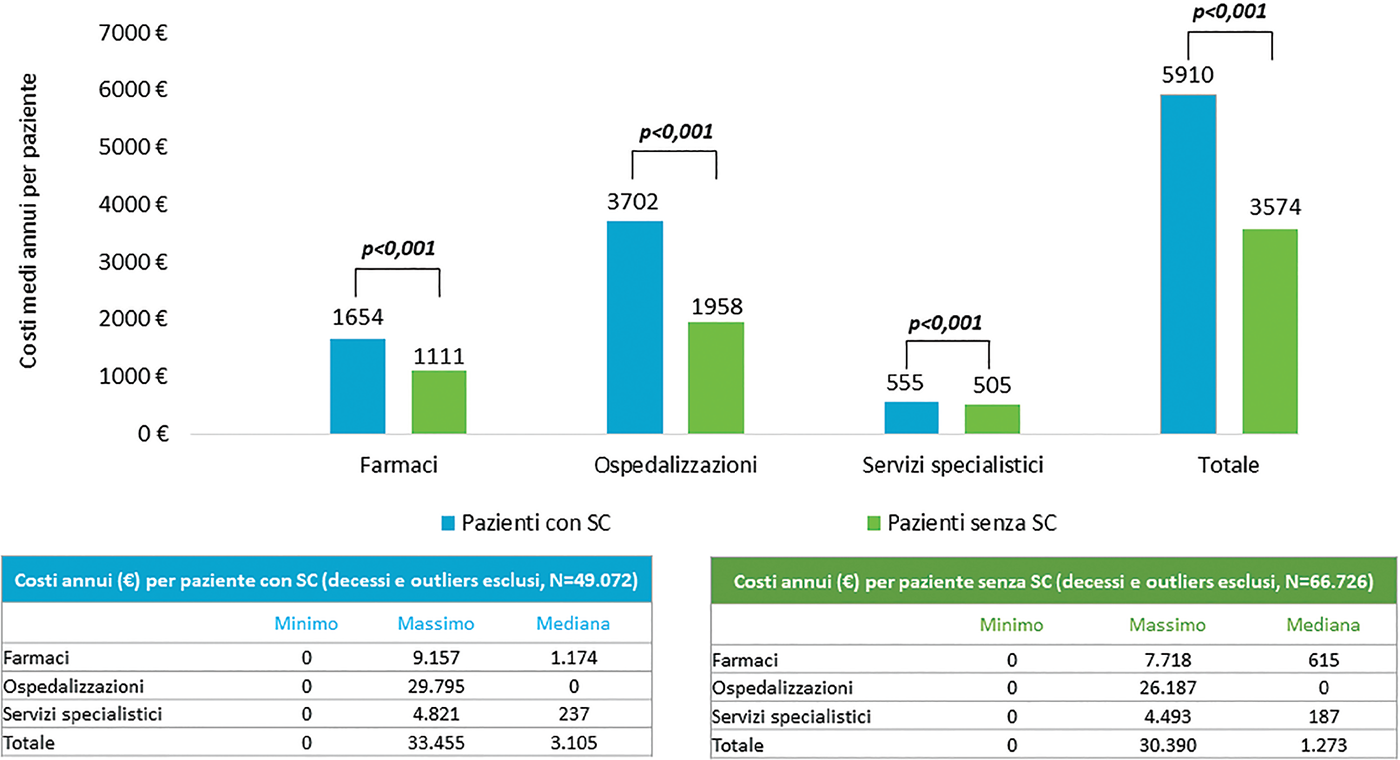
FIGURE 1 - Costi sanitari annui per paziente vivo per anno nei pazienti con SC e senza SC, riportati come medie (grafico), mediane, valore minimo e massimo (Tabelle in calce).
Anche se con costi globali e per singole voci di spesa tendenzialmente ridotti, l’analisi comparativa tra i pazienti con e senza SC nel secondo e nel terzo anno di follow-up ha mostrato un andamento paragonabile a quella del primo anno di follow-up (Fig. 2).
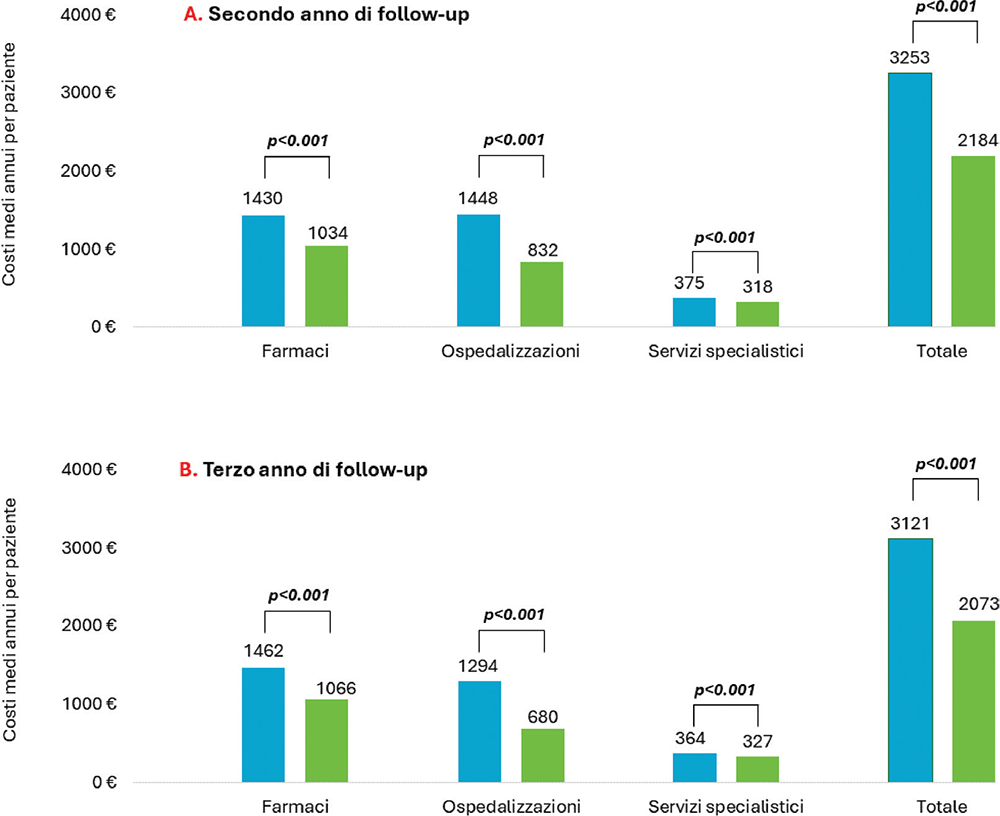
FIGURE 2 - Costi sanitari annui per paziente vivo per anno nei pazienti con SC e senza SC, al secondo (A) e al terzo anno di follow-up (B).
La Figura 3 riporta l’analisi dei costi medi per paziente vivo al primo anno di follow-up nel gruppo SC, dopo stratificazione dei farmaci tra cardiovascolari e non cardiovascolari, e dei costi per le ospedalizzazioni da causa cardiovascolare e non cardiovascolare. Dall’analisi si evince che le spese per farmaci non cardiovascolari erano superiori a quelle per farmaci cardiovascolari (rispettivamente: 997 € vs 657 €, p < 0,001); analogamente, le spese per i ricoveri da cause non cardiovascolari erano superiori a quelle per i ricoveri da causa cardiovascolare (rispettivamente: 2.303 € vs 1.399 €, p < 0,001).
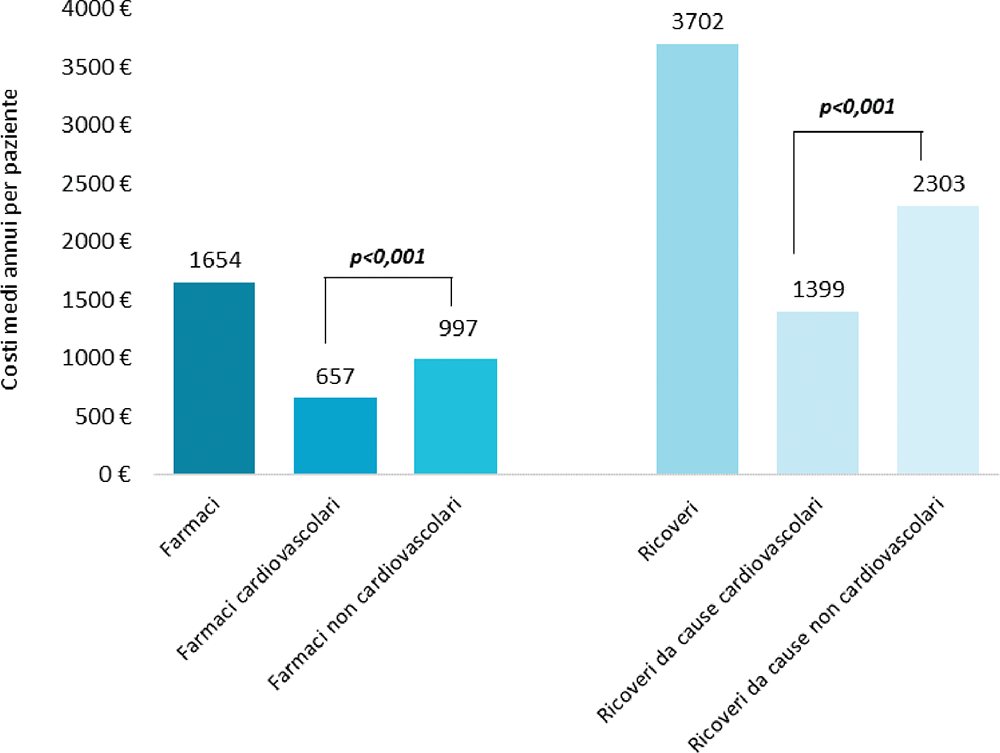
FIGURE 3 - Costi sanitari medi per paziente vivo relativi ai farmaci (totali e stratificati per cardiovascolari e non cardiovascolari) e ai ricoveri ospedalieri (da tutte le cause e stratificati per cause cardiovascolari e cause non cardiovascolari).
Discussione
Lo SC è una patologia fortemente dipendente dall’età, i cui numeri sono destinati a crescere, soprattutto nel mondo occidentale, di pari passo con il progressivo invecchiamento della popolazione (20). La presente analisi si proponeva di caratterizzare in termini demografici e clinici i pazienti con SC in un setting di reale pratica clinica italiana, focalizzandosi in particolare sui tassi di ospedalizzazione e sulla mortalità con le relative ricadute in termini di sostenibilità da parte del SSN. Da un campione rappresentativo di oltre 4 milioni di assistiti, pari a circa il 7% della popolazione italiana, 74.085 pazienti con diagnosi primaria o secondaria di SC e almeno un anno di disponibilità dei dati prima di tale diagnosi e dopo sono risultati eleggibili per lo studio. Nella popolazione campione, la frequenza dello SC si attestava intorno al 2%, dato del tutto comparabile con quanto riportato a livello mondiale (2). È stato quindi costruito un gruppo di controllo della stessa numerosità con le stesse caratteristiche demografiche e con la presenza di ipertensione, diabete, malattia cardiovascolare, dislipidemia e insufficienza renale cronica. In linea con i dati nazionali (8,21) e internazionali (2,22), la popolazione era costituita prevalentemente da anziani, con circa 9 pazienti su 10 oltre i 65 anni e un’età media vicina agli 80 anni. Tale osservazione non è sorprendente, dal momento che la prevalenza dello SC aumenta con l’età e che pazienti anziani con SC presentano molteplici comorbilità oltre allo SC di per sé (23-26).
Nella popolazione con SC inclusa, lo status clinico è stato esaminato mediante due approcci. Dapprima è stato applicato un adattamento dell’indice di Charlson (19) con l’esclusione delle malattie cardiovascolari e cerebrovascolari per valutare in maniera aspecifica il profilo di comorbilità che è risultato comunque più severo nei pazienti con SC rispetto al gruppo di controllo senza SC. Successivamente, è stato considerato il pattern delle condizioni concomitanti più comunemente descritte in letteratura nei soggetti con SC, vale a dire patologie cardiovascolari, respiratorie, renali, metaboliche, ematiche e psicologiche. Come atteso e concordemente con le evidenze esistenti, la popolazione con SC mostrava un profilo gravato da importanti comorbilità soprattutto cardiovascolari, quali ipertensione, diabete e insufficienza renale cronica (1,13-15).
Da tali dati emerge per i pazienti con SC un quadro di multicronicità che implica un marcato incremento dei tassi di ospedalizzazione e mortalità, come riportato anche dalle più recenti Linee Guida europee ESC (10,11). Infatti, nella presente analisi risultava come circa il 10% e il 25% dei pazienti ospedalizzati per SC decedevano durante il ricovero indice o entro il primo anno post-ricovero, rispettivamente. Questi dati erano in linea con quanto riportato dall’analisi del registro dell’European Society of Cardiology Heart Failure sui pazienti inclusi da 211 centri cardiologici distribuiti su 21 paesi europei, nel periodo 2011-2014, e che metteva in evidenza un tasso di mortalità del 23,6% nei pazienti SC ospedalizzati. Inoltre, una recente analisi monocentrica condotta in Italia su 728 pazienti ricoverati in Pronto Soccorso con una diagnosi di SC acuto ha mostrato che il tasso di mortalità era del 20% entro il primo anno di follow-up e dell’8% durante il ricovero indice (27).
La nostra analisi ha evidenziato un sensibile aumento dei costi e dei consumi sanitari a un anno dalla diagnosi di SC rispetto all’anno prima della diagnosi stessa e rispetto al gruppo di controllo senza SC. Anche escludendo l’ospedalizzazione indice, vale a dire quella per SC in cui veniva identificata la malattia, i costi dei ricoveri erano la voce maggiormente impattante sul burden globale dello SC. Analogamente, una recente ampia revisione sistematica della letteratura condotta su 4 database elettronici (incluso MEDLINE) per la ricerca di pubblicazioni tra gennaio 2014 e marzo 2020 inerenti analisi economiche sullo SC negli Stati Uniti, ha mostrato come i costi fossero molto variabili in base alle caratteristiche del singolo paziente (profilo di comorbilità, età, frazione di eiezione), ma, in ogni caso, condizionati in massima parte dalle spese per i ricoveri ospedalieri (28).
Nell’analisi dei costi sanitari sui soli pazienti con SC dopo stratificazione tra farmaci cardiovascolari e non cardiovascolari e delle ospedalizzazioni tra causa cardiovascolare e causa non cardiovascolare, è emerso come il contesto non cardiovascolare assorbisse spese superiori per quanto riguarda sia i farmaci che le ospedalizzazioni. Tale dato, oltre a confermare la complessità clinica e il profilo di comorbilità del paziente con SC, indica come la gestione della patologia debba necessariamente fare riferimento ad approcci terapeutici e interventistici di tipo multidisciplinare, non solo cardiovascolari.
L’interpretazione dei dati della presente analisi deve tenere conto di alcune limitazioni. A fronte dei vantaggi dell’utilizzo dei database amministrativi nel fornire una “fotografia” di setting di reale pratica clinica, tali database possono risultare sprovvisti di alcune particolari informazioni cliniche sul paziente, come la severità della malattia, l’attitudine del paziente verso la terapia domiciliare o altri dati utili per identificare possibili fattori confondenti. In particolare, si deve riconoscere tra le limitazioni dell’analisi la mancanza dei dati sulla frazione di eiezione che è un paramento rilevante per stabilire tipologia e severità dello SC. Inoltre, sia le patologie concomitanti che quelle utilizzate per il calcolo del CCI sono state identificate mediante i codici per tracciare nei database la presenza di prescrizioni di farmaci e ospedalizzazioni; pertanto, non sono state rilevate le condizioni che non implicassero terapie o ricoveri. Infine, dal momento che il periodo di inclusione arrivava fino a marzo 2021, non si può escludere che i dati raccolti a partire da marzo 2020 possano essere stati condizionati dall’effetto della pandemia COVID-19, ma questo aspetto non è stato valutato nella presente analisi. È noto dalla letteratura come vi sia un link patogenetico tra SC e infezione da SARS-CoV-2 (29). Infatti, biomarcatori cardiaci anormali sono comuni nel paziente con COVID-19, probabilmente a causa del fatto che l’ingresso del virus attraverso i recettori ACE2 e che lo storm citochinico risultante dall’infezione potrebbero rappresentare un trigger per il danno cardiaco diretto, l’aumento dell’attività trombotica e la cardiomiopatia da stress (29).
Conclusioni
Dalla presente analisi real-world in Italia, il paziente con SC emerge come un soggetto anziano e gravato da un profilo di multicronicità severo. A causa dell’invecchiamento generale della popolazione e delle previsioni di crescita dell’incidenza dello SC nei prossimi anni, la gestione di tali pazienti si presenta come un’importante emergenza sanitaria, sociale e finanziaria. L’elevato burden clinico ed economico associato allo SC deriva in massima parte dalla necessità di ricoveri ospedalieri, spesso multipli, non solo per la malattia stessa, ma anche per le complicazioni cardiovascolari, respiratorie, renali e metaboliche concomitanti, suggerendo come interventi mirati potrebbero portare a un sensibile contenimento dei costi e dei consumi sanitari sostenuti dal SSN.
Disclosures
Conflict of interest: The Authors declare no conflict of interest.
Financial support: The study report was commissioned by Boehringer Ingelheim and Eli Lilly. The Authors did not receive payment related to the development of the manuscript. Boehringer Ingelheim was given the opportunity to review the manuscript for medical and scientific accuracy as well as intellectual property considerations. Maria Cappuccilli PhD of CliCon provided writing and editorial support, and formatting assistance, which was contracted by Boehringer Ingelheim.
Authors contribution: MD: study design, conceptualization, manuscript preparation; ML: data analysis, statistical analysis; LDE: study design, conceptualization, manuscript supervision.
Data availability statement: All data used for the current analysis are available upon reasonable request next to CliCon S.r.l. which is the body entitled of data treatment and analysis by healthcare entities involved.
Bibliografia
- 1. Watson RD, Gibbs CR, Lip GY. ABC of heart failure. Clinical features and complications. BMJ. 2000;320(7229):236-239. CrossRef PubMed
- 2. Coats AJS. Ageing, demographics, and heart failure. Eur Heart J Suppl. 2019;21(suppl L):L4-L7. CrossRef PubMed
- 3. Ministero della Salute. Alleanza Italiana per le Malattie Celebro-Cardiovascolari. Scompenso Cardiaco. Online. (Accessed June 2023)
- 4. Istituto Superiore di Sanità. Scompenso cardiaco. Online (Accessed March 2024)
- 5. Leventhal ME, Denhaerynck K, Brunner-La Rocca HP, et al. Swiss Interdisciplinary Management Programme for Heart Failure (SWIM-HF): a randomised controlled trial study of an outpatient inter-professional management programme for heart failure patients in Switzerland. Swiss Med Wkly. 2011;141:w13171. CrossRef PubMed
- 6. Klein S, Jiang S, Morey JR, et al. Estimated Health Care Utilization and Expenditures in Individuals With Heart Failure From the Medical Expenditure Panel Survey. Circ Heart Fail. 2021;14(5):e007763. CrossRef PubMed
- 7. Ong SC, Low JZ, Yew WY, et al. Cost analysis of chronic heart failure management in Malaysia: A multi-centred retrospective study. Front Cardiovasc Med. 2022;9:971592. CrossRef PubMed
- 8. Maggioni AP, Orso F, Calabria S, et al; ARNO Observatory. The real-world evidence of heart failure: findings from 41 413 patients of the ARNO database. Eur J Heart Fail. 2016;18(4):402-410. CrossRef PubMed
- 9. Perrone V, Sangiorgi D, Degli Esposti L, et al. Lo scompenso cardiaco nella ASL Barletta-Andria-Trani (BT): analisi dei trattamenti farmacologici, del consumo di risorse e relativo costo per il Servizio Sanitario Nazionale. [Heart failure in Apulia Region - Italy (Local Health Unit Barletta-Andria-Trani): analysis of the therapeutic pathways, healthcare resource consumption and related costs.]. Recenti Prog Med. 2019;110(1):23-32. CrossRef PubMed
- 10. McDonagh TA, Metra M, Adamo M, et al; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-3726. CrossRef PubMed
- 11. McDonagh TA, Metra M, Adamo M, et al; ESC Scientific Document Group. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023;44(37):3627-3639. CrossRef PubMed
- 12. Harrington J, Sun JL, Fonarow GC, et al. Clinical Profile, Health Care Costs, and Outcomes of Patients Hospitalized for Heart Failure With Severely Reduced Ejection Fraction. J Am Heart Assoc. 2023;12(10):e028820. CrossRef PubMed
- 13. van der Wal HH, van Deursen VM, van der Meer P, Voors AA. Comorbidities in Heart Failure. Handb Exp Pharmacol. 2017;243:35-66. CrossRef PubMed
- 14. Metra M, Zacà V, Parati G, et al; Heart Failure Study Group of the Italian Society of Cardiology. Cardiovascular and noncardiovascular comorbidities in patients with chronic heart failure. J Cardiovasc Med (Hagerstown). 2011;12(2):76-84. CrossRef PubMed
- 15. Damman K, Valente MA, Voors AA, O’Connor CM, van Veldhuisen DJ, Hillege HL. Renal impairment, worsening renal function, and outcome in patients with heart failure: an updated meta-analysis. Eur Heart J. 2014;35(7):455-469. CrossRef PubMed
- 16. Chen J, Normand SL, Wang Y, Krumholz HM. National and regional trends in heart failure hospitalization and mortality rates for Medicare beneficiaries, 1998-2008. JAMA. 2011;306(15):1669-1678. CrossRef PubMed
- 17. Bytyçi I, Bajraktari G. Mortality in heart failure patients. Anatol J Cardiol. 2015;15(1):63-68. CrossRef PubMed
- 18. Chioncel O, Mebazaa A, Maggioni AP, et al; ESC-EORP-HFA Heart Failure Long-Term Registry Investigators. Acute heart failure congestion and perfusion status - impact of the clinical classification on in-hospital and long-term outcomes; insights from the ESC-EORP-HFA Heart Failure Long-Term Registry. Eur J Heart Fail. 2019;21(11):1338-1352. CrossRef PubMed
- 19. Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-383. CrossRef PubMed
- 20. The Lancet. Heart failure in an ageing population. Lancet. 2017 Nov 22:S0140-6736(17)33039-8. CrossRef PubMed
- 21. Maggioni A, Spandonaro F. Lo scompenso cardiaco acuto in Italia. G Ital Cardiol (Rome). 2014;15(S2):3-4.
- 22. Norhammar A, Bodegard J, Vanderheyden M, et al. Prevalence, outcomes and costs of a contemporary, multinational population with heart failure. Heart. 2023;109(7):548-556. CrossRef PubMed
- 23. Chiao YA, Rabinovitch PS. The Aging Heart. Cold Spring Harb Perspect Med. 2015;5(9):a025148. CrossRef PubMed
- 24. Guo J, Huang X, Dou L, et al. Aging and aging-related diseases: from molecular mechanisms to interventions and treatments. Signal Transduct Target Ther. 2022;7(1):391. CrossRef PubMed
- 25. Curtis LH, Whellan DJ, Hammill BG, et al. Incidence and prevalence of heart failure in elderly persons, 1994-2003. Arch Intern Med. 2008;168(4):418-424. CrossRef PubMed
- 26. Nakai M, Iwanaga Y, Kanaoka K, et al. Age-dependent association of discharge heart-failure medications with clinical outcomes in a super-aged society. Biomed Pharmacother. 2022;155:113761. CrossRef PubMed
- 27. Lombardi C, Peveri G, Cani D, et al. In-hospital and long-term mortality for acute heart failure: analysis at the time of admission to the emergency department. ESC Heart Fail. 2020;7(5):2650-2661. CrossRef PubMed
- 28. Urbich M, Globe G, Pantiri K, et al. A Systematic Review of Medical Costs Associated with Heart Failure in the USA (2014-2020). PharmacoEconomics. 2020;38(11):1219-1236. CrossRef PubMed
- 29. Bader F, Manla Y, Atallah B, Starling RC. Heart failure and COVID-19. Heart Fail Rev. 2021;26(1):1-10. CrossRef PubMed