 |
Glob Reg Health Technol Assess 2022; 9: 138-145 ISSN 2283-5733 | DOI: 10.33393/grhta.2022.2474 ORIGINAL RESEARCH ARTICLE |
 |
Costo per responder del metotrexato rispetto ad altre terapie in pazienti con psoriasi a placche da moderata a grave in Italia
Cost per responder for methotrexate versus other therapies in patients with moderate-to-severe plaque psoriasis in Italy
Objective: Conventional synthetic disease modifying antirheumatic drugs (csDMARDs) were recommended in 2019 as first line therapy from Italian Medicines Agency (AIFA) for the treatment of moderate to severe psoriasis. Updated local guidelines recommended methotrexate (MTX) as the drug of first choice. Nevertheless, MTX is reported by AIFA to be underused. Since no study evaluated jointly the first-line efficacy and costs of the most widely used biologic drugs (adalimumab, etanercept, secukinumab and ustekinumab) and methotrexate in Italy, a cost per responder (CPR) analysis was performed.
Methods: A CPR model was developed based on efficacy data from a published Cochrane network meta-analysis. Drug costs included in the model were estimated based on average regional tender prices. The primary analysis assessed the CPR of both Psoriasis Area and Severity Index (PASI) 90 at weeks 12 and 52. A secondary analysis was conducted considering PASI 75. For methotrexate, both an average dosage of 13.4 mg, estimated by an expert panel, and a dosage of 15 mg reported in European guidelines were considered.
Results: At weeks 12 and 52, the costs per responder PASI 90 were lower for methotrexate 13.4 mg compared to the most widely used biologics in Italy, € 566.71 and € 2,455.72 respectively. Methotrexate also showed a lowest CPR both at 12 and 52 weeks, € 529.95 and € 2,296.47 respectively, in the secondary analysis.
Conclusions: The analysis showed a lower cost per responder for methotrexate than for adalimumab, etanercept, secukinumab and ustekinumab. For healthcare budget holders, this means using the saved resources to treat more patients.
Keywords: Cost per responder, csDMARDs, Methotrexate, Plaque psoriasis
Received: July 26, 2022
Accepted: October 11, 2022
Published online: November 10, 2022
This article includes supplementary material
Global & Regional Health Technology Assessment - ISSN 2283-5733 - www.aboutscience.eu/grhta
© 2021 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
La psoriasi è una comune malattia cronica immuno-mediata della pelle che colpisce l’1-4% della popolazione mondiale e circa 14 milioni di persone in Europa (1). La forma più comune della patologia è la psoriasi a placche, che colpisce circa l’80-90% dei pazienti (2), con circa il 25% dei pazienti con psoriasi da moderata a grave (3,4) candidata a trattamenti sistemici quali fototerapia, agenti sistemici convenzionali (acitretina, ciclosporina, metotrexato, fumarati) e terapie mirate (biologici e piccole molecole).
La prevalenza nella popolazione generale italiana (pari al 2,9%) presenta una certa variabilità tra le diverse regioni. L’incidenza media è pari a 2,75 casi per 1.000 persone-anno (5). In base ai dati di prevalenza e incidenza riportati in letteratura si stima che in Italia vi siano tra i 436.000 e i 524.000 pazienti con psoriasi moderata-severa, con circa 45.000 pazienti-anno incidenti. Tuttavia, circa il 50% dei pazienti con psoriasi moderata-grave non è trattato in modo appropriato, come evidenziato da un recente studio osservazionale retrospettivo condotto su 12 milioni di assistiti (6).
La psoriasi rappresenta una patologia comune, che può avere un notevole impatto sul sistema sanitario. Garantire una corretta gestione della patologia e un uso appropriato delle risorse terapeutiche risulta pertanto fondamentale. Il management della patologia a livello di pratica clinica è però attualmente molto variabile, in quanto alcuni punti risultano essere ancora dibattuti, come l’utilizzo in prima linea dei più costosi farmaci biologici, che, anche se molto efficaci, possono comportare un rilevante aumento della spesa farmaceutica per questa specifica patologia.
Alle terapie sistemiche tradizionali, si sono affiancati da ormai diversi anni i farmaci biologici, che hanno cambiato in modo significativo il decorso della patologia, consentendo ai pazienti di raggiungere livelli significativi di clearance cutanea, associati a un miglioramento della QoL (7-9).
Tuttavia, per il trattamento della psoriasi di grado da moderato a grave, il ricorso ai biologici è previsto in caso di impossibilità di utilizzo o di inefficacia dei farmaci sistemici. Infatti, secondo la determina AIFA n. 699 del 15 aprile 2019 pubblicata in G.U. n. 93 del 19 aprile 2019, e successivo aggiornamento pubblicato in G.U. n. 129 del 20 maggio 2020 (10), il trattamento con farmaci biologici a carico del SSN deve essere limitato a pazienti con psoriasi a placche di grado da moderato a severo (definita come: PASI > 10 o BSA > 10% oppure BSA < 10% o PASI < 10 in associazione con lesioni al viso o palmari/plantari, ungueali o genitali) in caso di mancata risposta o intolleranza (fallimento terapeutico) a un DMARD sintetico convenzionale, dove il PASI (Psoriasis Area and Severity Index) rappresenta un Indice che correla segni e sintomi con l’estensione della malattia.
Per la valutazione della risposta a un trattamento si è soliti considerare il PASI 75, vale a dire un miglioramento del 75% del PASI iniziale dopo un trattamento, come indicatore minimo da raggiungere per definire una terapia efficace.
La comparsa dei nuovi farmaci biologici ha portato a un considerevole progresso nel trattamento della psoriasi, tanto che le recenti Linee Guida europee sulla psoriasi mirano a obiettivi di trattamento più elevati (PASI 90 o PASI 100) rispetto al PASI 75 (11). Le Linee Guida del 2021 del gruppo di lavoro multidisciplinare sui Farmaci Biotecnologici in Dermatologia della Regione Emilia-Romagna relative al trattamento sistemico della psoriasi cronica a placche moderata-grave concordano nel proporre il metotrexato come farmaco di prima scelta, in assenza di controindicazioni specifiche (12), preferibilmente per via sottocutanea (11).
Nonostante la presenza di Linee Guida, il MTX risulterebbe essere sottoutilizzato come dimostrato dallo studio di real world di Clicon et al., riportato in Corazza et al. (13), in cui dei 495 pazienti inclusi con psoriasi e in trattamento con farmaci biologici solo il 43,2% (N = 214) era stato trattato con metotrexato o ciclosporina nell’anno precedente l’inizio della terapia biologica e di questi il 52,3% (N = 112) aveva ricevuto un trattamento convenzionale per un periodo di almeno 3 mesi. Considerando l’intera popolazione inclusa (N = 495), solo il 22,6% dei pazienti aveva ricevuto una terapia con metotrexato o ciclosporina per almeno 3 mesi nell’anno prima del trattamento biologico. Tale studio, anche se con una dimensione campionaria ridotta da cui non è possibile effettuare alcun processo inferenziale, presenta dei risultati in linea con quanto riportato nel rapporto “L’uso dei farmaci in Italia – Rapporto OsMed 2015 dell’Osservatorio Nazionale sull’impiego dei Medicinali”, in cui il 77,3% dei pazienti con psoriasi era stato avviato al trattamento con farmaci biologici senza pregresso utilizzo di MTX o ciclosporina per almeno tre mesi (14).
Nonostante la presenza di numerose analisi di valutazione economica per i farmaci biologici, per il contesto italiano non è presente alcuno studio che valuti congiuntamente l’efficacia in prima linea dei farmaci biologici più utilizzati in Italia e del metotrexato nel raggiungimento del nuovo target terapeutico PASI 90. La presente analisi costo per responder, sulla base del Number Needed to Treat (NNT) colma questa lacuna perché, combinando insieme efficacia e costo, fornisce un utile strumento per supportare in modo efficiente i processi decisionali per l’allocazione ottimale delle risorse.
Metodi
L’analisi di costo per responder è stata condotta sui principi attivi maggiormente utilizzati in Italia appartenenti alle classi farmacologiche più rappresentative in termini di quote di mercato. Nello specifico, per le classi di farmaci interleuchine 17, anti-TNF alfa, interleuchine 12/23 e csDMARD, sono stati selezionati i principi attivi con le quote di mercato, espresse in numero di unità elementari, più elevate: secukinumab, etanercept, adalimumab, ustekinumab e metotrexato (Tab. I).
| Principio attivo | Classe farmaceutica | Market share sul totale |
|---|---|---|
| Seculinumab | Interleuchina-17A | 17% |
| Adalimumab | Anti-TNFα | 12,2% |
| Etanercept | Anti-TNFα | 6,5% |
| Ustekinumab | Interleuchina-12/23 | 9,2% |
| Metotrexato | csDMARD | 1,1% |
Fonte: Dati IQVIA, MAT maggio 2022.
L’outcome primario, PASI 90, è stato valutato a 12 settimane per la fase di induzione, così come quello secondario, PASI 75, che ancora oggi rappresenta l’indicatore da raggiungere per definire una terapia efficace, come riportato nelle Linee Guida della psoriasi della regione Emilia-Romagna (12). Entrambi gli outcome sono stati esplorati nell’analisi di scenario a 52 settimane per la fase di induzione e mantenimento, assumendo per quest’ultima la stessa efficacia della fase di induzione riportata nella network meta-analisi (NMA) Cochrane di Sbidian et al. (15). Tale assunzione, validata da un panel di esperti, anche se non supportata da dati di comparazione indiretta, è in linea con i dati di efficacia clinica a 52 settimane del metotrexato e dei farmaci biologici riportati rispettivamente in Reich et al. (16) e Leonardi et al. (17). Ciascuna analisi è stata eseguita considerando, come caso base, il dosaggio di 13,4 mg utilizzato nella pratica clinica, mentre il dosaggio raccomandato dalle Linee Guida europee di 15 mg (11) è stato valutato nell’analisi di scenario.
Posologia e costo trattamenti
Lo schema posologico e il numero di somministrazioni dei farmaci biologici sono stati stimati dalle rispettive schede tecniche, mentre, per il metotrexato, è stato utilizzato un dosaggio medio, per la fase di induzione e mantenimento, pari a 13,4 mg, sulla base della valutazione di un panel di esperti e delle percentuali delle confezioni sottocutanee vendute pesate per le rispettive quote di mercato (Dati IQVIA, MAT maggio 2022, Data on file) (Tab. II). Considerando che le formulazioni sottocutanee rappresentavano il 75% del mercato e che del restante 25%, relativo alle formulazioni orali, non erano disponibili le quote di mercato delle confezioni in commercio, è stato assunto dal panel di esperti il medesimo dosaggio stimato per la formulazione sottocutanea (13,4 mg). ll dosaggio di 15 mg raccomandato dalle Linee Guida è stato utilizzato sia per l’induzione che per il mantenimento. Il costo di acquisizione dei principi attivi considerati, stimato dalla media dei prezzi netti di gara regionale aggiudicati (Tab. A Supplementare), è stato utilizzato insieme al dosaggio medio per determinare il costo medio per paziente nella fase di induzione a 12 settimane e di induzione e mantenimento del primo anno di trattamento (Tabb. III e IV).
| mg | Formulazione | Market share | Costo unità elementare | Costo per mg | Costo medio ponderato per mg |
|---|---|---|---|---|---|
| 2,5 | Orale | 25% | 0,199 | 0,079 | 0,53 |
| 7,5 | SC | 6,75 | 5,06 | 0,67 | |
| 10 | 22,50 | 6,75 | 0,67 | ||
| 12,5 | 6,75 | 8,44 | 0,67 | ||
| 15 | 28,50 | 10,13 | 0,67 | ||
| 17,5 | 2,25 | 11,81 | 0,67 | ||
| 20 | 5,62 | 13,50 | 0,67 | ||
| 25 | 2,62 | 16,87 | 0,67 |
SC: Sottocutaneo.
Fonte: Elaborazione degli Autori su dati IQVIA.
| Principio attivo | Posologia di trattamento (induzione e mantenimento) | Confezione | Prezzo medio per unità |
|---|---|---|---|
| Metotrexato | Dosaggio medio pari a 13,4 mg nella fase di induzione e di mantenimento | € 7,05 | |
| Etanercept biosimilare | Induzione: 50 mg/settimana
Mantenimento: 50 mg/settimana |
1 unità da 50 mg | € 51,29 |
| Adalimumab biosimilare | Induzione: 80 mg, seguiti da una dose di 40 mg somministrata a settimane alterne, a partire dalla settimana successiva alla somministrazione della dose iniziale
Mantenimento: 40 mg |
1 unità da 40 mg | € 47,04 |
| Ustekinumab | Induzione: 45 mg somministrati per via sottocutanea, seguiti da una dose di 45 mg dopo 4 settimane
Mantenimento: 45 mg ogni 12 settimane |
45 mg soluzione iniettiva | € 2.311,00 |
| Secukinumab | Induzione: 300 mg alle settimane 0, 1, 2, 3 e 4, seguiti da un dosaggio di 300 mg ogni 4 settimane
Mantenimento: 300 mg ogni 4 settimane |
1 unità da 150 mg | € 415,99 |
Fonte: Elaborazione degli Autori.
| Principio attivo | N. unità posologiche induzione | N. unità posologiche mantenimento | Costo induzione
(12 settimane) |
Costo medio primo anno (52 settimane) |
|---|---|---|---|---|
| Metotrexato | 12 | 40 | € 84,58 | € 366,52 |
| Etanercept biosimilare | 12 | 40 | € 615,44 | € 2.666,91 |
| Adalimumab biosimilare | 8 | 20 | € 376,36 | € 1.317,24 |
| Ustekinumab | 2 | 4 | € 4.622,00 | € 13.866,00 |
| Secukinumab | 12 | 22 | € 4.991,90 | € 14.143,72 |
Fonte: Elaborazione degli Autori.
Dati di efficacia
L’efficacia delle terapie considerate in questo studio per il trattamento della PsO moderata-grave è stata valutata a 8-24 settimane, sulla base della stima del rischio relativo (RR) di ciascun trattamento versus placebo di raggiungere il PASI 90 e il PASI 75 riportato nella network meta-analisi (NMA) Cochrane di Sbidian et al. (15) (Tab. IV). Il PASI 90 e il PASI 75 indicano rispettivamente una riduzione del 90% e del 75% del punteggio PASI rispetto al rispettivo valore iniziale (18). Il Number Needed to Treat (NNT), definito come il numero di pazienti che deve essere trattato per ottenere un beneficio terapeutico aggiuntivo rispetto al gruppo di controllo comune (placebo), è stato stimato sia per il PASI 90 che per il PASI 75 a partire dal rischio relativo (RR) di ciascun trattamento riportato nella NMA e dal rischio stimato del braccio di controllo (Assumed Control Risk, ACR) utilizzando la seguente formula: 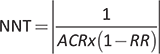 .
.
Per l’analisi primaria PASI 90 è stato utilizzato il rischio assoluto del placebo (ACR) riportato nella NMA, pari a 0,025, mentre l’ACR del PASI 75, pari a 0,06, è stato stimato come rischio assoluto calcolato come rapporto tra la somma del numero di eventi (risposta PASI 75) del placebo e la somma dei pazienti randomizzati nel braccio placebo degli studi inclusi nella NMA che avevano come braccio di controllo il placebo (Tab. V). Al fine di stimare il costo per responder, il NNT di ciascun trattamento (Tab. VI) è stato moltiplicato per il rispettivo costo annuo.
| Trattamento | Rischio Relativo PASI 90 (95% CrI) | Rischio Relativo PASI 75 (95% CrI) |
|---|---|---|
| Metotrexato | 6,97 (1,42-34,34) | 3,66 (1,81-7,37) |
| Secukinumab | 25,79 (21,61-30,78) | 12,71 (11,12-14,52) |
| Adalimumab_bs | 17,81 (14,82-21,40) | 10,05 (8,61-11,73) |
| Etanercept_bs | 10,76 (9,03-12,82) | 8,09 (7,22-9,06) |
| Ustekinumab | 18,46 (15,51-21,98) | 11,04 (9,83-12,40) |
Fonte: Sbidian et al. (15).
| Trattamento | NNT PASI 90 | NNT PASI 75 |
|---|---|---|
| Metotrexato | 6,70 | 6,27 |
| Secukinumab | 1,61 | 1,42 |
| Adalimumab_bs | 2,38 | 1,84 |
| Etanercept_bs | 4,10 | 2,35 |
| Ustekinumab | 2,29 | 1,66 |
Fonte: Elaborazione degli Autori sulla base di Sbidian et al. (15).
Risultati
L’analisi costo per responder a 12 settimane, effettuata su un dosaggio medio di 13,4 mg, ha evidenziato per l’outcome primario, PASI 90, e secondario, PASI 75, una notevole variabilità in termini di costo. Il metotrexato rappresenta, in entrambi i casi, il trattamento con il costo per responder più basso pari a € 566,71 e a € 529,95, seguito da adalimumab, con € 895,55/€ 693,10, etanercept, secukinumab e ustekinumab (Fig. 1).
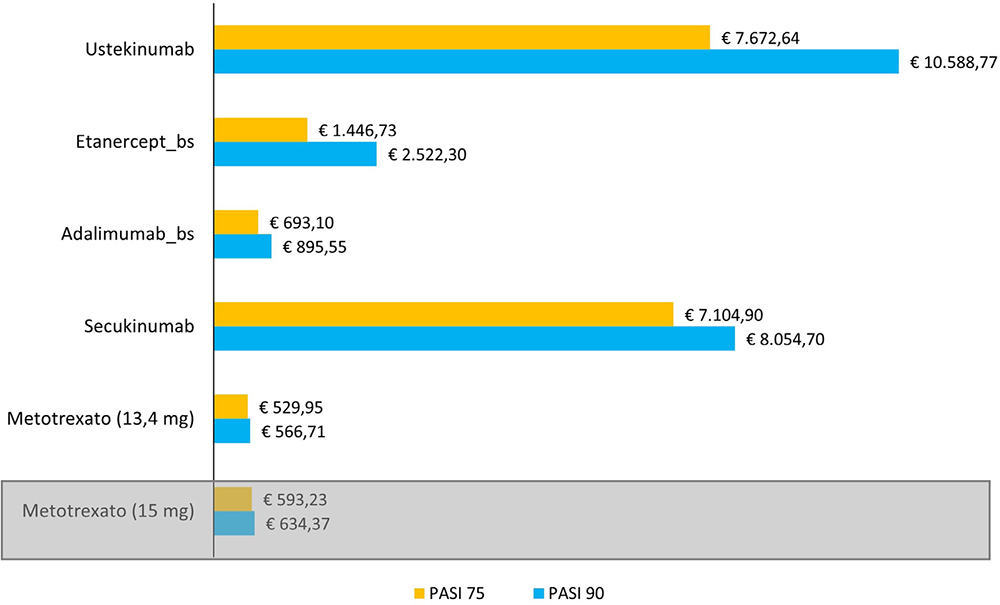
Fig. 1 - Analisi costo per responder PASI 90 e PASI 75 a 12 settimane.
Analisi di scenario
L’analisi di scenario del PASI 90 e del PASI 75 condotta a 52 settimane evidenzia come il metotrexato continui a essere il principio attivo con il costo per responder più basso, pari rispettivamente a € 2.455,72/€ 2.296,47 seguito da adalimumab, con € 3.134,43/€ 2.425,86, etanercept, secukinumab e ustekinumab (Fig. 2).
Per valutare l’impatto del dosaggio di 15 mg raccomandato dalle Linee Guida europee, è stata condotta sul PASI 90 e PASI 75 un’analisi di scenario, facendo variare il dosaggio utilizzato nel caso base da 13,4 mg a 15 mg. Come mostrato nella Figura 1 (box grigio), con il dosaggio di 15 mg il costo per responder PASI 90 e PASI 75 del metotrexato a 12 settimane continua a essere il più basso di tutti gli altri farmaci, pari a € 634,37/€ 593,23 mentre a 52 settimane risulta essere rispettivamente il più basso (€ 2.748,94) e il secondo più basso (€ 2.570,68) dopo adalimumab (€ 2.425,86) (Fig. 2, box grigio).
Analisi di sensibilità
La robustezza dell’analisi è stata esplorata per il PASI 90 e per il PASI 75 su un orizzonte temporale di 12 settimane con un’analisi di sensibilità univariata, facendo variare il rischio relativo dei principi attivi considerati secondo il limite inferiore e superiore dei rispettivi intervalli di confidenza (IC) e il costo del metotrexato ± 20%. Per facilitare la lettura della sensitivity analysis, il diagramma a tornado presenta la differenza in termini di aumento o diminuzione del valore del costo per responder, ottenuto dalla variazione di ciascun parametro in negativo (Lower) e in positivo (Higher), rispetto al risultato che si è ottenuto nel caso base. Pertanto, la linea verticale del grafico posta in corrispondenza dello zero rappresenta l’impatto nullo sul caso base. I risultati relativi al metotrexato mostrano come l’intervallo di confidenza del rischio relativo sia il parametro che più influenza il risultato del costo per responder PASI 90 e PASI 75, con un impatto maggiore nel primo caso (Figg. 3 e 4).
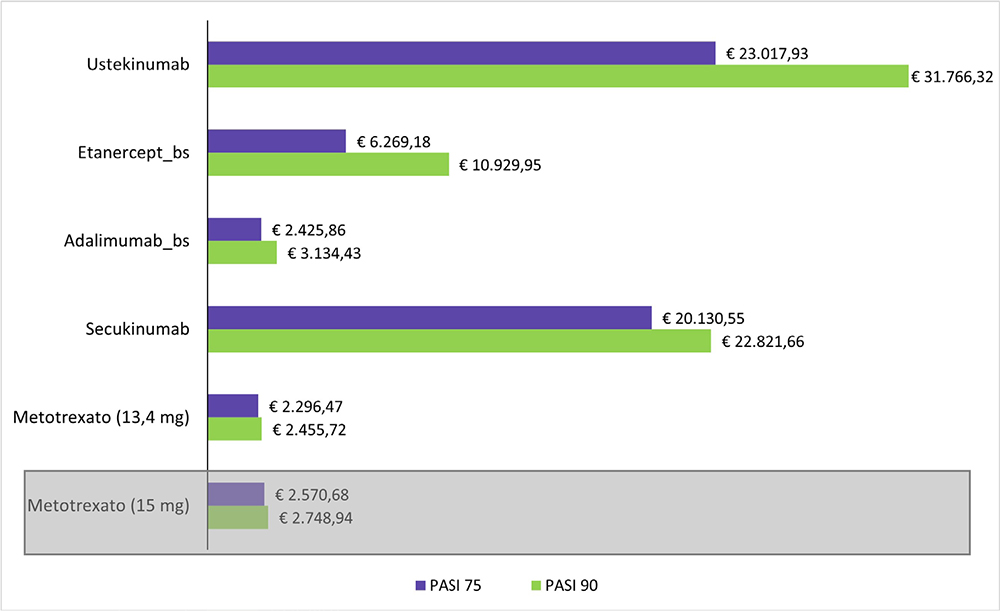
Fig. 2 - Analisi costo per responder PASI 90 e PASI 75 a 52 settimane.
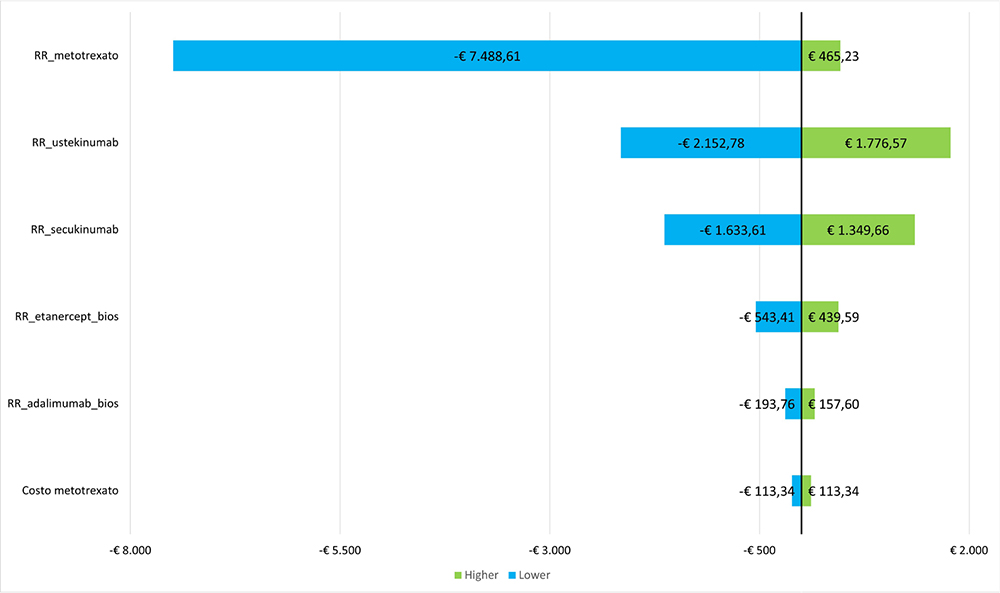
Fig. 3 - Analisi di sensibilità univariata costo per responder PASI 90 a 12 settimane.
Potenziale impatto sul SSN
I risultati dell’analisi costo per responder a 52 settimane sono stati utilizzati per stimare il potenziale impatto sul SSN dell’adozione della strategia terapeutica con il costo per responder più basso, rappresentata dal metotrexato. I costi aggiuntivi per responder PASI 90 e PASI 75 di ciascun trattamento versus il metotrexato sono stati calcolati dalla differenza tra i due costi per responder. Tale differenza consente di stimare (dividendo per il valore del costo per responder del metotrexato) il numero di pazienti potenzialmente trattabili con il metotrexato.
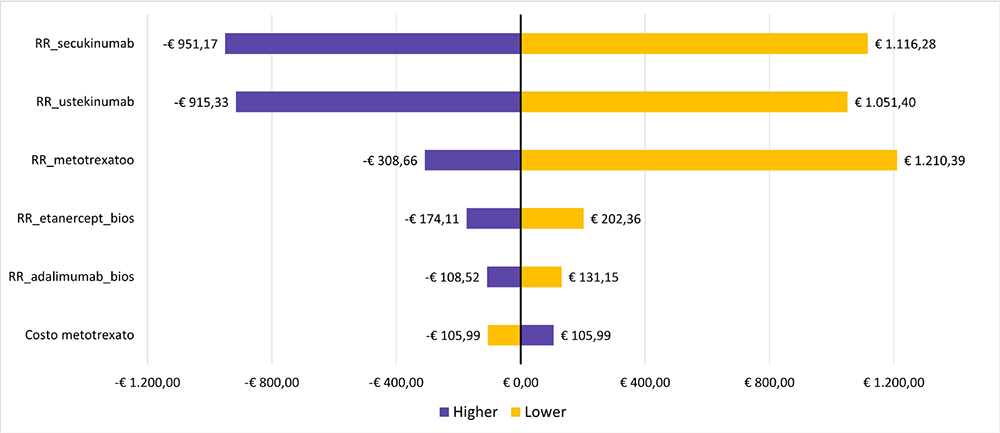
Fig. 4 - Analisi di sensibilità univariata costo per responder PASI 75 a 12 settimane.
La Tabella VII mostra come con un dosaggio medio di metotrexato di 13,4 mg, a parità di risorse, sia possibile trattare, considerando il PASI 90 e il PASI 75, rispettivamente fino a 12 e 9 pazienti in più rispetto a ustekinumab e fino a 8 pazienti in più rispetto a secukinumab. Ipotizzando un budget medio di un’Azienda Sanitaria Locale (ASL) di € 200.000, da allocare per la psoriasi moderata-severa, è possibile stimare sia il numero di pazienti che sarebbe possibile trattare per ciascun trattamento sia il numero di pazienti aggiuntivi potenzialmente trattabili con il metotrexato, la strategia terapeutica con il costo per responder più basso. La Tabella VIII evidenzia come con il metotrexato sia possibile trattare un numero di pazienti aggiuntivo responsivi al PASI 90 e al PASI 75, pari rispettivamente a un range di 17-75 e di 5-78 rispetto agli altri trattamenti.
| Trattamento | Costo per responder PASI 90 addizionale * | N. pazienti ** | Costo per responder PASI 75 addizionale * | N. pazienti ** |
|---|---|---|---|---|
| Secukinumab | € 20.365,94 | 8,29 | € 17.834,08 | 7,77 |
| Adalimumab_bs | € 678,70 | 0,28 | € 129,39 | 0,06 |
| Etanercept_bs | € 8.474,23 | 3,45 | € 3.972,71 | 1,73 |
| Ustekinumab | € 29.310,60 | 11,94 | € 20.721,46 | 9,02 |
* (versus metotrexato 13,4 mg)
** potenzialmente trattabili con metotrexato 13,4 mg
Fonte: Elaborazione degli Autori.
| Trattamento | N. pazienti costo per responder PASI 90 | Differenza versus metotrexato | N. pazienti costo per responder PASI 75 | Differenza versus metotrexato |
|---|---|---|---|---|
| Metotrexato 13,4 mg | 81,44 | 87,09 | ||
| Secukinumab | 8,76 | 72,68 | 9,94 | 77,15 |
| Adalimumab_bs | 63,81 | 17,63 | 82,44 | 4,65 |
| Etanercept_bs | 18,30 | 63,14 | 31,90 | 55,19 |
| Ustekinumab | 6,30 | 75,15 | 8,69 | 78,40 |
Fonte: Elaborazione degli Autori.
Limiti dell’analisi
L’analisi costo per responder presenta alcuni limiti, a partire dalla robustezza della stima del braccio placebo (ACR) per l’endpoint secondario PASI 75, utile per calcolare la riduzione dei rischi assoluti (ARR) di ciascun trattamento versus il placebo. Tale stima si è resa quindi necessaria a causa della mancanza, nella network meta-analisi di Sbidian et al., degli ARR. Inoltre, data l’assenza in tale studio di stime indirette a 52 settimane, è stata assunta un’efficacia (PASI 75 e PASI 90) sostenuta fino a 52 settimane, in coerenza con quanto riportato in letteratura (16,17), nelle Linee Guida della regione Emilia-Romagna (12) e dal panel di esperti. Tuttavia, l’impatto stimato sul SSN potrebbe essere affetto da errori proprio per la mancanza di stime a 52 settimane derivanti da una comparazione indiretta. Un altro limite è rappresentato dall’assunzione fatta, secondo quanto emerso da un panel di esperti, sul dosaggio della formulazione orale sulla base di quella sottocutanea. Da ultimo, l’assenza nella NMA degli intervalli di confidenza relativi al rischio assoluto e l’impossibilità di stimarli non hanno consentito di stimare il limite inferiore e superiore del NNT e di valutarne quindi l’impatto nell’analisi di sensibilità univariata.
Discussione
L’utilizzo in prima linea dei farmaci biologici per la psoriasi a placche di grado da moderato a severo se da un lato ha certamente migliorato gli outcome di salute dei pazienti che ne soffrono, dall’altro ha portato a un uso non sempre appropriato di questi farmaci, con conseguente sottoutilizzo dei csDMARD, in particolare stime di mercato riportato che soltanto il 22% dei pazienti con psoriasi a placche ha utilizzato il metotrexato in prima linea di trattamento. Questo fenomeno ha quindi generato inappropriatezza prescrittiva, come riportato nel Rapporto OsMed 2015, tanto che la stessa AIFA è dovuta intervenire con la determina n. 699. La presente analisi costo per responder è il primo studio che considera congiuntamente i farmaci più utilizzati nel contesto italiano, includendo quindi anche il metotrexato e non soltanto i farmaci biologici. La maggior parte delle evidenze disponibili per l’Italia riguarda analisi costo per responder che confrontano soltanto farmaci biologici/biosimilari (19,20). Comunque, un recente studio, in linea con la nostra analisi, ha evidenziato un più basso costo per responder del metotrexato rispetto ad adalimumab.
Per quanto riguarda il dosaggio di 15 mg di MTX, utilizzato nell’analisi di scenario, bisogna considerare che le Linee Guida europee raccomandano l’utilizzo di tale posologia per via iniettiva sin dall’inizio del trattamento e che, invece, le percentuali di risposta PASI 90 e PASI 75 del metotrexato stimate dalla NMA fanno riferimento a studi che valutavano formulazioni orali con un dosaggio iniziale inferiore a 15 mg. Ciò ha diverse implicazioni: 1) l’efficacia del metotrexato stimata nello studio Sbidian et al. potrebbe essere sottostimata rispetto a quella riscontrata nella pratica clinica; 2) i risultati delle analisi costo per responder potrebbero essere ancora più favorevoli per il metotrexato di quanto già non lo siano. In aggiunta a quanto riportato, recenti studi di confronto tra le due modalità di somministrazione hanno dimostrato che la forma orale è sia meno efficace che meno tollerata della forma sottocutanea e soprattutto che ha un effetto plateau a 15 mg che invece non ha la formulazione iniettiva (21,22).
Il metotrexato, come ha cercato di illustrare questa analisi, con un NNT più alto rispetto a quello dei trattamenti considerati e un costo per trattamento più basso, rappresenta il farmaco con il costo per responder PASI 90 a 12 e a 52 settimane più basso considerando entrambi i dosaggi (13,4 mg e 15 mg), pari rispettivamente a € 566,71/€ 634,37 e a € 2.464,89/€ 2.748,94. In linea teorica, i costi addizionali derivanti dalla differenza tra i costi per responder PASI 90 a 52 settimane di ciascun trattamento versus il costo per responder del metotrexato consentirebbero di trattare più pazienti; per esempio con il costo per responder PASI 90 di ustekinumab sarebbe possibile trattare con un dosaggio di metotrexato di 13,4 mg ulteriori 12 pazienti.
Conclusione
I risultati della presente analisi mostrano come, nella prospettiva del SSN, il metotrexato presenti un costo per responder PASI 90 sia a 12 che a 52 settimane inferiore rispetto ai farmaci attualmente più utilizzati (secukinumab, adalimumab, etanercept e ustekinumab) per il trattamento di pazienti adulti con psoriasi a placche da moderata a grave. Ciò fornisce un’utile indicazione per i decisori per allocare, in accordo con la determina AIFA, in modo efficiente le risorse disponibili e consentire un accesso al trattamento di prima linea a molti più pazienti affetti da psoriasi a placche moderata-severa.
Disclosures
Davide Integlia is the CEO of Isheo srl and has received grants from Abbvie, Merck Serono, Bristol Myers Squibb, Pierre Fabre, Eli Lylli, Boehringer Ingelheim, Angelini, Fidia Pharma, and AlfaSigma. Giuseppe Pompilio declares no conflict of interest.
Financial support: This study received unconditional funding from AlfaSigma Italia S.p.A.
Bibliografia
- 1. Damiani G, Bragazzi NL, Karimkhani Aksut C, et al. The Global, Regional, and National Burden of Psoriasis: Results and Insights From the Global Burden of Disease 2019 Study. Front Med (Lausanne). 2021;8:743180. CrossRef PubMed
- 2. Di Meglio P, Villanova F, Nestle FO. Psoriasis. Cold Spring Harb Perspect Med. 2014 Aug 1;4(8):a015354. CrossRef PubMed
- 3. Augustin M, Krüger K, Radtke MA, Schwippl I, Reich K. Disease severity, quality of life and health care in plaque-type psoriasis: a multicenter cross-sectional study in Germany. Dermatology. 2008;216(4):366-72. CrossRef PubMed
- 4. Augustin M, Reich K, Glaeske G, Schaefer I, Radtke M. Co-morbidity and age-related prevalence of psoriasis: analysis of health insurance data in Germany. Acta Derm Venereol. 2010;90(2):147-151. CrossRef PubMed
- 5. Prignano F, Rogai V, Cavallucci E, Bitossi A, Hammen V, Cantini F. Epidemiology of Psoriasis and Psoriatic Arthritis in Italy-a Systematic Review. Curr Rheumatol Rep. 2018 May 30;20(7):43. CrossRef
- 6. Perrone V, Losi S, Maiorino A, Antonelli S, Giovannitti M, Giacomini E, Sangiorgi D, Degli Esposti L. Treatment Patterns and Pharmacoutilization in Patients Affected by Psoriasis: An Observational Study in an Italian Real-World Setting. Drugs Real World Outcomes. 2022 Jun;9(2):243-251. CrossRef PubMed
- 7. Blauvelt A, Griffiths CEM, Lebwohl M, et al. Reaching complete or near-complete resolution of psoriasis: benefit and risk considerations. Br J Dermatol. 2017;177(2):587-590. CrossRef PubMed
- 8. Farahnik B, Beroukhim K, Zhu TH, et al. Ixekizumab for the Treatment of Psoriasis: A Review of Phase III Trials. Dermatol Ther (Heidelb). 2016;6(1):25-37. CrossRef PubMed
- 9. Thaçi D, Blauvelt A, Reich K, Tsai TF, Vanaclocha F, Kingo K, Ziv M, Pinter A, Hugot S, You R, Milutinovic M. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate to severe plaque psoriasis: CLEAR, a randomized controlled trial. J Am Acad Dermatol. 2015 Sep;73(3):400-9. CrossRef PubMed
- 10. Gazzetta Ufficiale della Repubblica Italiana. Serie Generale n. 129 del 20-5–2020. Online (Accessed July 2022)
- 11. Nast A, Smith C, Spuls PI, et al. EuroGuiDerm Guideline on the systemic treatment of Psoriasis vulgaris – Part 1: treatment and monitoring recommendations. J Eur Acad Dermatol Venereol. 2020;34(11):2461-2498. CrossRef PubMed
- 12. Gruppo di lavoro multidisciplinare sui Farmaci Biotecnologici in Dermatologia Regione Emilia-Romagna. Linee guida terapeutiche/1 Trattamento sistemico della psoriasi cronica a placche moderata-grave con particolare riferimento ai farmaci biotecnologici. Novembre 2021. Online (Accessed July 2022)
- 13. Corazza, V., Cusano, F., De Pità, O., Rossi, L., & Virno, G. G. Methotrexate in the therapeutic pathway of patients with psoriasis. Analysis of clinical practice data and comparison with guidelines. Dermatology Reports. 2021;14(1). CrossRef PubMed
- 14. AIFA. Osservatorio Nazionale sull’impiego dei Medicinali. L’uso dei farmaci in Italia. Rapporto Nazionale 2015. Roma. 2016. Online (Accessed July 2022)
- 15. Sbidian E, Chaimani A, Garcia-Doval I, Doney L, Dressler C, Hua C, Hughes C, Naldi L, Afach S, Le Cleach L. Systemic pharmacological treatments for chronic plaque psoriasis: a network meta-analysis. Cochrane Database Syst Rev. 2022 May 23;5(5):CD011535. CrossRef PubMed
- 16. Reich K, Sorbe C, Griese L, Reich JLK, Augustin M. The value of subcutaneous vs. oral methotrexate: real-world data from the German psoriasis registry PsoBest. Br J Dermatol. 2021 Apr;184(4):765-767. CrossRef PubMed
- 17. Leonardi CL, See K, Burge R, Sun Z, Zhang Y, Mallbris L, Garrelts A, Warren RB. Number Needed to Treat Network Meta-Analysis to Compare Biologic Drugs for Moderate-to-Severe Psoriasis. Adv Ther. 2022 May;39(5):2256-2269. CrossRef PubMed
- 18. Gisondi P, Altomare G, Ayala F, et al. Italian guidelines on the systemic treatments of moderate-to-severe plaque psoriasis. J Eur Acad Dermatol Venereol. 2017 May;31(5):774-790. CrossRef PubMed
- 19. Gisondi P, Loconsole F, Raimondo P, Ravasio R. Cost per responder for risankizumab vs secukinumab in patients with moderate-to-severe plaque psoriasis in Italy. Glob Reg Health Technol Assess. 2021;8(1):120-123. CrossRef
- 20. Ravasio R, Antonelli S, Maiorino A et al. Cost per responder for ixekizumab and other biologic drugs approved for the treatment of moderate-to-severe plaque psoriasis in Italy. Glob Reg Health Technol Assess. 2019;6(1). CrossRef
- 21. Attwa EM, Elkot RA, Abdelshafey AS, Hafez AR. Subcutaneous methotrexate versus oral form for the treatment and prophylaxis of chronic plaque psoriasis. Dermatol Ther. 2019 Sep;32(5):e13051. CrossRef PubMed
- 22. Dogra S, Singh N, Kumar S, Narang T, Handa S. Comparison of overall efficacy and safety of oral versus subcutaneous methotrexate in severe psoriasis. Dermatol Ther. 2022 Aug;35(8):e15656. CrossRef PubMed