 |
Glob Reg Health Technol Assess 2022; 9: 91-98 ISSN 2283-5733 | DOI: 10.33393/grhta.2022.2413 ORIGINAL RESEARCH ARTICLE |
 |
Analisi di impatto di budget di un nuovo sistema di cura in pazienti affetti da malattia di Parkinson
Budget Impact analysis of a new system of care in Parkinson’s disease patients
Objective: To estimate the economic impact of the introduction of a new care system based on apomorphine and Patient Support Program for motor fluctuations (“on-off” phenomena) in patients with Parkinson’s disease which are not sufficiently controlled by oral anti-Parkinson medication in Italy.
Method: A Budget Impact model was developed to evaluate the new care system in patients with Parkinson’s disease over a 3-years’ time horizon. The comparator treatments included in the analysis were treatments based on apomorphine and levodopa + carbidopa. The analysis was conducted from a National Health Service (NHS) perspective. Costs included in the analysis were acquisition costs and device costs. A deterministic sensitivity analysis was carried out to evaluate the uncertainty of the parameters used. A break-even analysis was conducted to identify the minimum number of subjects that would need to be treated with the new care system to obtain a positive Budget Impact (World With – World Without = 0).
Results: The analysis shows that the introduction of the new care system based on apomorphine could generate a cost saving incurred by the NHS of over € 5.7 million in 3 years. Break-even analysis shows that if it were possible to intercept with the new treatment at least 9 patients treated with apomorphine, there would not be an increase in costs for the NHS.
Conclusion: The new care system would respond to the unmet needs of patients with Parkinson’s disease by generating a reduction in the expenditure incurred by NHS.
Keywords: Apomorphine hydrochloride, Budget Impact Analysis, Economic Evaluation, Parkinson’s Disease
Received: April 14, 2022
Accepted: July 28, 2022
Published online: September 19, 2022
Global & Regional Health Technology Assessment - ISSN 2283-5733 - www.aboutscience.eu/grhta
© 2021 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
La malattia di Parkinson è una malattia cronico-degenerativa a elevata diffusione che presenta, nelle varie popolazioni del mondo, un tasso di prevalenza estremamente variabile. Ha un impatto economico molto significativo sotto diverse prospettive: per la società, per i sistemi sanitari, per i pazienti e per i loro familiari. A livello mondiale sono circa 6,2 milioni le persone affette dalla malattia di Parkinson, ma tale cifra in realtà potrebbe essere considerevolmente più alta poiché sappiamo che molte persone non vengono diagnosticate (1).
Una recente meta-analisi condotta a livello nazionale al fine di stimare la prevalenza della malattia di Parkinson in Italia ha mostrato l’esistenza di una variabilità dei tassi di prevalenza in base all’età: 37,8/100.000 abitanti nei soggetti di età compresa tra 0 e 64 anni, 578,7/100.000 nella fascia di età compresa tra 65 e 75 anni e 1.235,7/100.000 nella fascia di età pari o superiore a 75 anni (2). La stima aggregata è risultata pari a 193,7/100.000. Inoltre, sempre all’interno dello stesso studio, è risultata un’associazione tra la malattia e il sesso maschile, ma solo nei gruppi di età più avanzata (OR = 1,37 IC 95% 1,22-1,53, e OR = 1,31, IC 95% 1,21-1,42 per gruppi di età 65-74 anni e di 75 anni o più, rispettivamente).
Circa 1/3 dei pazienti totali con Parkinson “avanzato” non è adeguatamente controllato con i trattamenti abituali ma necessita della combinazione di diverse classi di trattamento tra cui apomorfina, duodopa o stimolazione cerebrale profonda.
Le recenti Linee Guida NICE indicano la terapia da seguire in funzione dello stato di malattia di Parkinson. In particolare, per la malattia di Parkinson in fase precoce la scelta dovrebbe ricadere tra gli agonisti della dopamina, la levodopa o gli inibitori delle monoamino ossidasi B (MAO-B) per tutti quei pazienti in cui i sintomi motori non impattano sulla loro qualità di vita; per i sintomi motori la scelta dovrebbe ricadere tra gli agonisti della dopamina, MAO-B inibitori o COMT inibitori, come adiuvanti della terapia con levodopa per tutti quei pazienti che hanno sviluppato discinesie o fluttuazioni motorie. Per i pazienti con Parkinson avanzato va considerato un intervento di neurostimolazione cerebrale profonda solo quando i sintomi non sono controllati con il miglior trattamento farmacologico possibile che può includere l’apomorfina sottocutanea somministrata in maniera intermittente o per infusione continua. L’apomorfina risulta inoltre efficace sui sintomi non-motori (NMS) quali apatia, umore, allucinazioni, attenzione, memoria e problemi gastrointestinali e urinari. Quando i periodi “off” sono associati a dolore intrattabile, l’apomorfina può essere considerata un’opzione importante per alleviare il disagio dei pazienti (3).
Il trattamento continuo con apomorfina è utile negli stadi avanzati di malattia di Parkinson quando falliscono i trattamenti orali e quando le iniezioni di boli di apomorfina dovrebbero essere troppo frequenti per gestire appropriatamente i troppi periodi “off” durante la giornata. Oltre alla stimolazione cerebrale profonda (DBS), le infusioni di apomorfina e le infusioni duodenali di levodopa-carbidopa (duodopa) rappresentano una concreta opzione terapeutica (4,5).
Recentemente è stata sviluppata una nuova terapia a base di apomorfina per il trattamento delle fluttuazioni motorie (fenomeno “on-off”) in pazienti affetti da malattia di Parkinson che non sono sufficientemente controllati da medicinali orali anti-Parkinson. Tale terapia, oltre a consentire nel nuovo dosaggio di apomorfina in 20 mL (concentrazione 5 mg/mL) la somministrazione di un’unica fiala/die (100 mg) tale da coprire l’intero fabbisogno giornaliero del paziente, si propone non solo come nuovo farmaco ma come nuovo “sistema di cura” poiché si avvale di un’innovativa pompa infusionale e di un Patient Support Program (PSP) “personalizzato” in grado di assicurare una semplificazione delle modalità di somministrazione e di gestione della terapia, con conseguente miglioramento della compliance e dell’aderenza e quindi dei risultati terapeutici per il paziente.
In particolare, il PSP prevede:
– la fornitura gratuita della pompa infusionale, così come informazioni sulla sua gestione e sulla logistica;
– la fornitura gratuita di tutti i materiali monouso (cateteri, reservoir), con garanzia di consegna tempestiva a casa del paziente;
– una serie di servizi “homecare” per la gestione della pompa e del materiale monouso sia al paziente che al caregiver;
– corsi di training in ospedale rivolti a infermieri, neurologi, pazienti e caregiver;
– presenza di un “Numero Verde” disponibile per il paziente e il caregiver;
– visite di follow up con gli infermieri coinvolti e call con il paziente;
– questionari per valutare l’aderenza e la qualità della vita del paziente.
Sebbene non siano ancora stati condotti studi di confronto diretto tra apomorfina e levodopa-carbidopa, guardando agli studi clinici randomizzati di entrambe le terapie infusionali, la dimensione dell’effetto del trattamento risulta simile tra le due infusioni (6-8). Rispetto ai pazienti in trattamento con le terapie sostitutive standard della dopamina, levodopa-carbidopa gel intestinale e apomorfina a infusione continua, hanno mostrato un incremento del tempo di attivazione senza discinesia fastidiosa rispettivamente pari a 1,9 h (IC 95% 0,6-3,2; FU 3 mesi) (8) e pari a 2,0 h (IC 95% 0,7-3,4; FU 3 mesi) (7).
Guardando alla modalità di somministrazione, l’infusione di apomorfina risulta facilmente reversibile e meno invasiva rispetto al gel levodopa-carbidopa poiché quest’ultimo richiede l’inserimento di un tubo gastrico. La fornitura di un PSP “personalizzato” in associazione alla somministrazione di apomorfina consentirebbe un ulteriore miglioramento della gestione della terapia.
L’obiettivo dello studio è stato quello di valutare gli impatti economici che potrebbe generare l’introduzione del nuovo trattamento a base di apomorfina e del suo servizio di PSP per il trattamento delle fluttuazioni motorie (fenomeno “on-off”) in pazienti affetti da malattia di Parkinson che non sono sufficientemente controllati da medicinali orali anti-Parkinson.
L’impatto economico derivante dall’introduzione sul mercato del nuovo trattamento a base di apomorfina verrà valutato confrontando lo scenario in cui sia presente la nuova terapia con lo scenario caratterizzato dai trattamenti attualmente disponibili sul mercato.
Metodi
L’analisi di impatto sul budget è stata condotta secondo la prospettiva del Servizio Sanitario Nazionale (SSN) e seguendo le Linee Guida suggerite dall’International Society of Pharmacoeconomics and Outcome Research (ISPOR) (9,10).
Tale analisi si basa sul confronto di due scenari alternativi: lo scenario senza il nuovo trattamento a base di apomorfina, caratterizzato dalla presenza delle terapie attualmente disponibili sul mercato per il trattamento delle fluttuazioni motorie in pazienti affetti da malattia di Parkinson (apomorfina cloridrato 50 mg/5 mL e levodopa + carbidopa 7 sacche gel intestinale 100 mL 20 mg/mL + 5 mg/mL), e lo scenario in cui viene simulata l’introduzione della nuova terapia sul mercato.
Il modello ha tenuto conto di un orizzonte temporale pari a 3 anni di analisi.
Popolazione eleggibile e scenari di analisi
Applicando la stima di prevalenza per la malattia di Parkinson ottenuta dalla letteratura nazionale più recente (Ricco et al. 2020 (2)) alla popolazione residente in Italia, è stato possibile stimare un numero di pazienti con malattia di Parkinson in Italia pari a circa 114.250 soggetti. La sottoanalisi dello studio osservazionale multi-paese OBSERVE-PD condotta da Stefani et al. nel 2022 sul gruppo di pazienti appartenenti a 9 centri italiani (su 128 centri nel mondo) ha stimato una quota di pazienti con malattia di Parkinson in stadio avanzato pari al 42,9% (11); tra i pazienti con malattia in stadio avanzato che risultavano in trattamento con terapia orale/transdermica (circa il 67%), il 97,6% non risultava adeguatamente controllato. Applicando queste stime alla popolazione con malattia di Parkinson in Italia, il numero di pazienti con malattia di Parkinson in stadio avanzato non adeguatamente controllati con farmaci orali è risultato pari a circa 32.000 pazienti (Tab. I).
La popolazione eleggibile al nuovo trattamento a base di apomorfina è stata individuata a partire dalla stima del numero di soggetti in trattamento con le terapie attualmente disponibili; tale stima è stata effettuata sulla base dei dati di dispensazione per il periodo tra gennaio e dicembre 2018 e gennaio e agosto 2019 assumendo una proiezione costante per l’ultimo quadrimestre 2019 (dati IQVIA, Tab. I).
Assumendo un numero di unità internazionali (UI) annue per paziente pari a 365 per il trattamento con levodopa + carbidopa e un numero di UI annue per paziente pari a 730 per il trattamento a base di apomorfina per il 2018 sono stati stimati rispettivamente circa 928 pazienti trattati con levodopa + carbidopa e circa 155 pazienti trattati con apomorfina cloridrato. Per il 2019 sono stati stimati un aumento dei pazienti in trattamento con levodopa + carbidopa (+990 pazienti) e una riduzione dei pazienti in trattamento con apomorfina (-133 pazienti).
Il numero di pazienti potenzialmente eleggibili al nuovo trattamento a base di apomorfina è risultato pari a 1.222, 1.282 e 1.350 in corrispondenza degli anni 1, 2 e 3 (Tab. I). Nei tre anni simulati è stato assunto un incremento del numero di pazienti trattati proporzionale rispetto a quanto registrato per il periodo 2018-2019.
Le quote di pazienti associate a ciascun trattamento per entrambi gli scenari sono state definite sulla base di stime interne Ever Pharma. Nella Tabella II sono riportate le percentuali di utilizzo delle singole opzioni di trattamento durante i 3 anni simulati.
Si prevede che il nuovo trattamento a base di apomorfina diventi, progressivamente, la principale alternativa terapeutica insieme a levodopa + carbidopa nei pazienti affetti da malattia di Parkinson interessati da fluttuazioni motorie (fenomeno “on-off”) che non sono sufficientemente controllati da medicinali orali anti-Parkinson.
Nello scenario in cui viene simulata l’introduzione del nuovo trattamento sul mercato, la percentuale di pazienti trattati con il nuovo farmaco a base di apomorfina a livello nazionale è stata considerata pari al 4%, al 10% e al 16% rispettivamente per gli anni 1, 2 e 3.
| Stima | N | Fonte | |||
|---|---|---|---|---|---|
| Popolazione residente al 1° gennaio 2022 | 58.983.122 | ISTAT (14) | |||
| Casi/100.000 abitanti | 193,7 | 114.250 | Riccò et al. 2020 (2) | ||
| Pazienti con malattia di Parkinson in stadio avanzato | 42,90% | 49.013 | Stefani et al. 2022 (11) | ||
| Pazienti con malattia di Parkinson in stadio avanzato trattati con terapia orale/transdermica | 67,0% | 32.839 | |||
| Pazienti con malattia di Parkinson in stadio avanzato non adeguatamente controllati con i farmaci orali | 97,6% | 32.051 | |||
| UI 2018 | N pazienti 2018* | UI 2019 | N pazienti 2019* | ||
| Levodopa + carbidopa (gel intestinale) | 338.795 | 928 | 361.231 | 990 | IQVIA |
| Apomorfina cloridrato (infusione sottocutanea continua) | 113.352 | 155 | 96.808 | 133 | |
| Totale | 1.083 | 1.123 | |||
| N pazienti 2020** | N pazienti 2021** | N pazienti 2022** | N pazienti 2023** | ||
| Levodopa + carbidopa (gel intestinale) | 1.055 | 1.125 | 1.200 | 1.279 | IQVIA |
| Apomorfina cloridrato (infusione sottocutanea continua) | 113 | 97 | 83 | 71 | |
| Totale | 1.168 | 1.222 | 1.283 | 1.350 |
*Stimato assumendo un numero di unità internazionali (UI) annue per paziente pari a 365 per il trattamento con levodopa + carbidopa e un numero di UI annue per paziente pari a 730 per il trattamento a base di apomorfina.
**Stimato considerando il tasso di crescita stimato tra il 2018 e il 2019 e risultato pari al 6,6% per levodopa + carbidopa e pari al -15% per apomorfina cloridrato.
| Trattamenti | Scenario Attuale | Scenario Alternativo | ||||
|---|---|---|---|---|---|---|
| Anno 1 | Anno 2 | Anno 3 | Anno 1 | Anno 2 | Anno 3 | |
| Levodopa + carbidopa | 92% | 94% | 95% | 89% | 86% | 83% |
| Apomorfina cloridrato | 8% | 6% | 5% | 7% | 4% | 1% |
| Apomorfina cloridrato emiidrato + Pompa elettronica e consumabili per l’infusione continua + PSP | 0% | 0% | 0% | 4% | 10% | 16% |
| Totale | 100% | 100% | 100% | 100% | 100% | 100% |
Parametri di costo
Nella presente analisi sono stati considerati il costo di acquisizione del trattamento e il costo dei dispositivi necessari ai fini dell’utilizzo dei singoli trattamenti (Tab. III). Il costo dei dispositivi necessari per la somministrazione dell’apomorfina (separato dal prezzo del farmaco e sostenuto dal SSN) è stato calcolato assumendo per ciascuna delle due somministrazioni giornaliere l’utilizzo di un ago verticale e di una siringa (730 unità per ciascun dispositivo) e considerando l’acquisto di un microinfusore ogni due anni (durata prevista da scheda tecnica pompa Canè).
Nella Tabella IV sono riportati i costi annui per paziente associati a ciascuna specifica voce di costo e il costo annuo totale per paziente relativamente a ciascuna opzione di trattamento in analisi. In particolare, per la somministrazione di levodopa + carbidopa è stato considerato anche il costo della chirurgia prevista per il posizionamento PEG. Per il calcolo dei costi di acquisizione sono state assunte un’aderenza e una compliance pari al 100% in corrispondenza di ciascun anno di analisi. Tale assunto potrebbe non essere verosimile ma si è reso necessario al fine di consentire un confronto diretto delle differenti strategie di trattamento.
| Prezzo Ex-Factory | Prezzo UI | Dose giornaliera | Costo Totale Annuo Terapia | |
|---|---|---|---|---|
| Apomorfina cloridrato emiidrato + Pompa elettronica e consumabili per l’infusione continua + PSP | € 56,8 | € 42,6 | 1 | € 15,562,7 |
| Levodopa + carbidopa | € 682,3 | € 97,5 | 1 | € 35,576,5 |
| Apomorfina cloridrato | € 29,5 | € 5,9 | 2 | € 4.314,3 |
| Dispositivi addizionali per apomorfina cloridrato | N° dispositivi anno | Costo unitario | Costo totale | Fonte parametro di costo |
| Aghi Verticali Singoli (2 unità giornaliere) | 730 | € 3,6 | € 2.628,0 | Listino prezzi 2018 Canè Prezzo unitario al netto degli sconti (IVA inclusa) |
| Microinfusori (durata media 2 anni) | 1 | € 1.314,0 | € 1.314,0 | |
| Siringhe (2 unità giornaliere) | 730 | € 5,1 | € 3.744,9 |
| Farmaco | Chirurgia | Pompa | Altri dispositivi¥ | Homecare | Costo Annuo Totale | |
|---|---|---|---|---|---|---|
| Levodopa + carbidopa | € 35.577 | € 1.129* | PSP | PSP | PSP | € 36.706 |
| Apomorfina cloridrato | € 4.314 | – | € 1.314 | € 6.373 | ** | € 12.001 |
| Apomorfina cloridrato emiidrato + Pompa elettronica e consumabili per l’infusione continua + PSP | € 15.056 | – | PSP | PSP | PSP | € 15.563 |
*EGD scopia (Cod.reg. 45.17 tariffa € 738,55) + Posizionamento PEG (€ 345,54).
¥Somma dei costi annui per aghi e siringhe (non compresi nel costo del Duodopa system).
**Nessuna offerta di servizi di Homecare.
Analisi di sensibilità
Al fine di identificare differenti potenziali scenari di analisi nel corso degli anni, è stata condotta un’analisi di sensibilità deterministica; tale analisi consiste nel far variare un parametro di input alla volta al fine di valutare l’impatto di tale variazione sui risultati dell’analisi. In particolare, per questo modello sono stati valutati i seguenti scenari:
- Scenario 1: riduzione del prezzo di levodopa + carbidopa secondo quanto stimato da gare regionali (–31%)
- Scenario 2: riduzione del prezzo del trattamento a base di apomorfina secondo quanto stimato da gare regionali (–13%)
- Scenario 3: variazione combinata dei prezzi di levodopa + carbidopa e apomorfina secondo quanto stimato da gare regionali
- Scenario 4: variazione della velocità di penetrazione:
Caso-base: 50, 130 e 220 pazienti rispettivamente al 2021, al 2022 e al 2023; Min 25, 65 e 110 pazienti e Max 75, 195 e 330 pazienti
- Scenario 5: variazione dei prezzi degli altri dispositivi non compresi nel prezzo del farmaco (±20% rispetto al caso-base)
I risultati dell’analisi di sensibilità deterministica sono mostrati mediante il grafico tornado.
Infine, è stata condotta una specifica analisi di break-even al fine di individuare il numero minimo di soggetti che sarebbe necessario trattare con la nuova terapia di base di apomorfina (tra quelli attualmente trattati con apomorfina) al fine di ottenere un Budget Impact positivo (Costo mondo Con – Costo mondo Senza = 0).
Risultati
Nella Tabella V sono riportati i costi diretti sanitari stimati per ciascuno scenario e per ciascun anno di analisi e la differenza di costo derivante dal confronto dei due scenari. Per entrambi gli scenari, la principale voce di spesa è risultata caratterizzata dal costo del farmaco (98% della spesa complessiva). L’introduzione del nuovo trattamento a base di apomorfina sul mercato italiano con quote di pazienti trattati crescenti nel corso degli anni consentirebbe una riduzione cumulata della spesa a carico del SSN di oltre € 5,7 milioni in 3 anni (Fig. 1). Tale riduzione di spesa risulta attribuibile a un minor numero di pazienti trattati con levodopa + carbidopa e al risparmio in termini di acquisto dei dispositivi che si otterrebbe per i pazienti trattati con la nuova terapia a base di apomorfina poiché per questo trattamento il costo dei dispositivi risulta compreso all’interno del prezzo del farmaco.
Guardando ai risultati in corrispondenza di ciascun anno di analisi, il SSN potrebbe ottenere una riduzione della spesa pari a circa € 676.726 al primo anno di analisi, pari a oltre € 1,8 milioni al secondo anno di analisi e pari a oltre € 3,2 milioni al terzo anno dall’introduzione del nuovo trattamento a base di apomorfina.
| ITALIA | Spesa | ||
|---|---|---|---|
| Risultati anno 1 | World without | World with | BUDGET IMPACT |
| Costo farmaco | € 40.444.219 | € 39.912.460 | € –531.759 |
| Costo chirurgia | € 177.846 | € 138.328 | € –39.518 |
| Costo altri dispositivi | € 679.988 | € 574.540 | € –105.448 |
| TOTALE SPESA | € 41.302.054 | € 40.625.328 | € –676.726 |
| Risultati anno 2 | World without | World with | BUDGET IMPACT |
| Costo farmaco | € 43.034.011 | € 41.526.387 | € –1.507.623 |
| Costo chirurgia | € 189.623 | € 82.360 | € –107.263 |
| Costo altri dispositivi | € 580.742 | € 334.696 | € –246.046 |
| TOTALE SPESA | € 43.804.377 | € 41.943.444 | € –1.860.933 |
| Risultati anno 3 | World without | World with | BUDGET IMPACT |
| Costo farmaco | € 45.808.229 | € 43.124.603 | € –2.683.626 |
| Costo chirurgia | € 202.181 | € 15.881 | € –186.299 |
| Costo altri dispositivi | € 495.981 | € 109.337 | €–386.644 |
| TOTALE SPESA | € 46.506.392 | € 43.249.822 | € –3.256.570 |
| Risultati a 3 anni | World without | World with | BUDGET IMPACT |
| Costo farmaco | € 129.286.460 | € 124.563.451 | € –4.723.008 |
| Costo chirurgia | € 569.651 | € 236.569 | € –333.081 |
| Costo altri dispositivi | € 1.756.713 | € 1.018.573 | € –738.139 |
| SPESA TOTALE A 3 ANNI | € 131.612.824 | € 125.818.595 | € –5.794.229 |
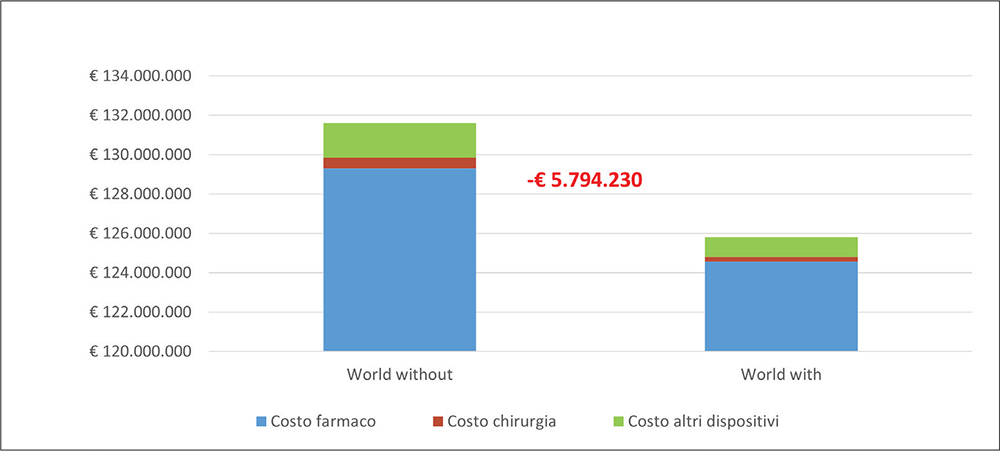
Fig. 1 - Composizione della spesa totale a tre anni – Italia.
La Figura 2 mostra come il valore di Budget Impact cumulato stimato dal modello economico sia piuttosto robusto. Infatti, in tutti gli scenari simulati nell’analisi di sensibilità deterministica, l’introduzione del nuovo trattamento a base di apomorfina consente una riduzione dei costi rispetto all’attuale gestione dei pazienti in analisi. In particolare, il parametro a cui corrisponde la maggiore riduzione della spesa è rappresentato dalla velocità di penetrazione del nuovo trattamento a base di apomorfina. Simulando un numero di pazienti trattati con il nuovo farmaco pari a 75, 195 e 330 rispettivamente in corrispondenza degli anni 1, 2 e 3, potrebbe ottenersi un risparmio cumulato della spesa a carico del SSN a 3 anni di analisi pari a circa € 11,8 milioni. Tuttavia, è possibile osservare come, in tutti gli scenari pessimistici (MIN), comunque si otterrebbero delle riduzioni di spesa.
La Figura 3 mostra la relazione tra il numero di pazienti intercettati dal nuovo trattamento a base di apomorfina e il risultato di Budget Impact a un anno dall’introduzione del nuovo trattamento a base di apomorfina. L’analisi mostra come il livello di break-even sia pari a 9 pazienti; dunque, se si riuscissero a intercettare tra i pazienti in trattamento con levodopa + carbidopa almeno 9 pazienti, il SSN inizierebbe a non sostenere costi aggiuntivi.
Discussione
Si ritiene che la proposta di un “sistema di cura” tale da garantire tecnologie e servizi “personalizzati” (farmaco + device + PSP) e non più di un “solo farmaco” possa rispondere a bisogni ancora non soddisfatti dei pazienti (difficoltà di utilizzo corretto e funzioni di monitoraggio al servizio del paziente e delle strutture), consentendo una più corretta allocazione delle risorse terapeutiche disponibili e una riduzione dei costi sanitari generati dalla mancata aderenza.
La nostra analisi ha quattro principali limitazioni che vanno considerate. L’impatto di spesa è stato stimato tenendo conto dei soli costi di acquisizione e somministrazione (in termini di device e chirurgia) dei trattamenti oggetto di studio, per cui risulta ragionevole assumere come tale impatto rappresenti una sottostima dei reali vantaggi che potrebbe generare l’introduzione del nuovo trattamento nel contesto nazionale. Inoltre, l’analisi è stata condotta secondo la prospettiva del SSN, per cui non si è tenuto conto dei costi indiretti, i quali rappresentano oltre il 30% della spesa totale associata alla malat-tia di Parkinson (12,13). Un ulteriore limite dello studio fa riferimento alla stima del numero di pazienti intercettati dal nuovo trattamento a base di apomorfina. Infatti non è semplice capire la possibilità reale di intercettazione dei pazienti nella reale pratica clinica ma l’analisi di break-even ha mostrato come tale percentuale sia sufficientemente bassa da non rappresentare una reale barriera all’accesso dell’utilizzo del nuovo trattamento a base di apomorfina. Infine, l’ipotesi del 100% di compliance costituisce una assumption del modello di simulazione affinché le tre opzioni terapeutiche in analisi possano avere le stesse condizioni di partenza per generare un risultato libero da bias. Sicuramente, considerando i soli costi del farmaco, la compliance sarebbe una sola variabile in diminuzione della spesa farmaceutica; sarebbe opportuno valutare gli effetti di medio/lungo periodo anche in termini di costi di gestione successivi. Future e più approfondite analisi potrebbero sviluppare questo filone di ricerca nell’ambito farmacoeconomico.
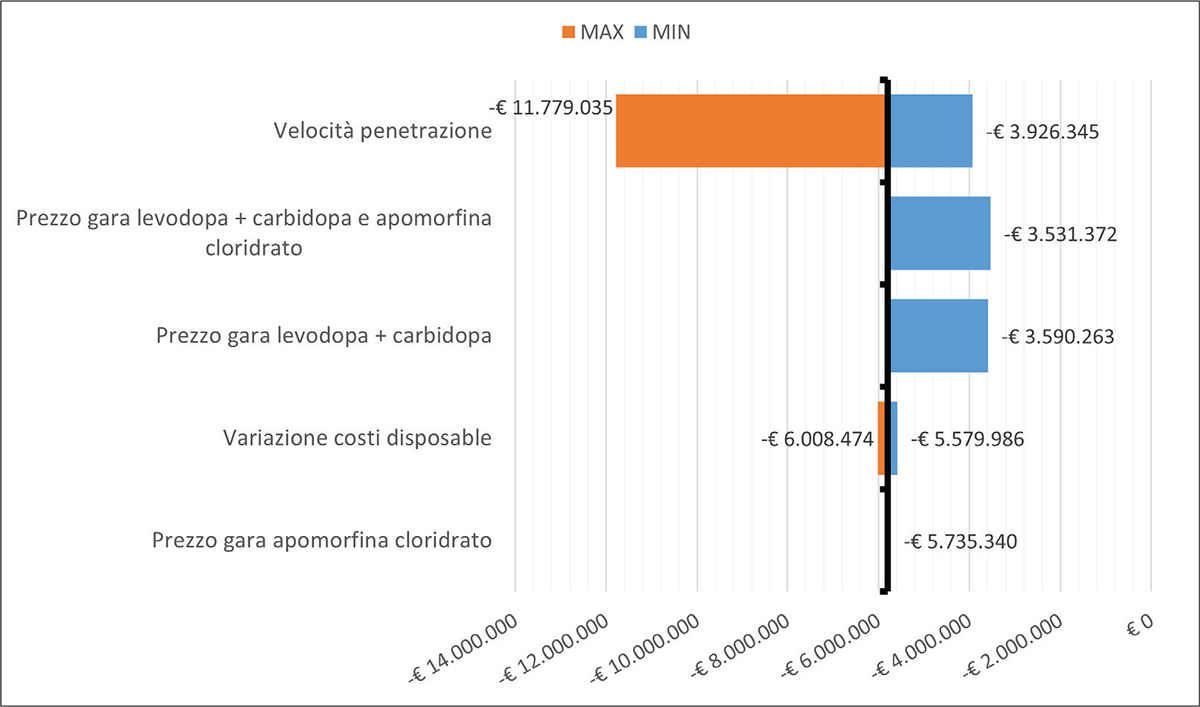
Fig. 2 - Analisi di sensitività a una via – stime cumulate anno 3.
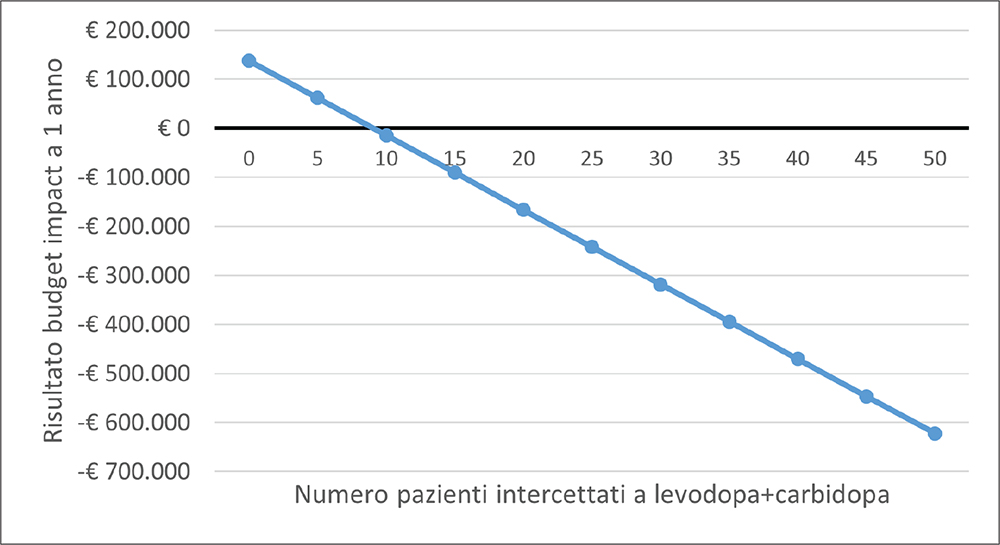
Fig. 3 - Analisi di break-even.
Tenendo conto dei limiti riportati sopra, mediante questa analisi è stato possibile osservare come l’introduzione del nuovo trattamento a base di apomorfina, inclusivo del costo del device e dei consumabili per l’infusione continua, insieme a un sistema di Patient Support Program personalizzato, potrebbe generare una riduzione cumulata della spesa a carico del SSN a 3 anni dalla sua introduzione pari a oltre € 5,7 milioni.
Il miglioramento all’accesso dei pazienti consentirebbe non solo una corretta gestione dei soggetti affetti da Malattia di Parkinson con fluttuazioni motorie (fenomeno “on-off”) che non sono sufficientemente controllati da medicinali orali anti-Parkinson, ma permetterebbe anche di rallentare la progressione della linea di trattamento con levodopa + carbidopa. Tale rallentamento consentirebbe da una parte di evitare la necessità di terapie altamente invasive e dall’altra di ridurre la spesa farmaceutica.
Conclusioni
Il nuovo trattamento a base di apomorfina, in associazione a un sistema di Patient Support Program personalizzato e a un innovativo sistema di infusione continua, all’interno delle opzioni terapeutiche per il trattamento delle fluttuazioni motorie (fenomeno “on-off”) in pazienti affetti da malattia di Parkinson che non sono sufficientemente controllati da medicinali orali anti-Parkinson, potrebbe coprire un vuoto gestionale della terapia che a oggi è particolarmente sentito da parte dei clinici e, conseguentemente, generare una riduzione di spesa da parte del SSN.
Disclosures
Conflict of interest: The Authors declare no conflict of interest.
Financial support: This study was supported by an unconditional grant from Ever Pharma Italia S.r.l.
Bibliografia
- 1. European Parkinson’s Disease Association. What is Parkinson’s disease? Online Accessed April 2022.
- 2. Riccò M, Vezzosi L, Balzarini F, et al. Prevalence of Parkinson Disease in Italy: a systematic review and meta-analysis. Acta Biomed. 2020;91(3):e2020088. PubMed
- 3. Torti M, Bravi D, Vacca L, Stocchi F. Are All Dopamine Agonists Essentially the Same? Drugs. 2019;79(7):693-703. CrossRef PubMed
- 4. Jenner P, Katzenschlager R. Apomorphine – pharmacological properties and clinical trials in Parkinson’s disease. Parkinsonism Relat Disord. 2016;33(suppl 1):S13-S21. CrossRef PubMed
- 5. Djamshidian A, Poewe W. Apomorphine and levodopa in Parkinson’s disease: two revolutionary drugs from the 1950’s. Parkinsonism Relat Disord. 2016;33(suppl 1):S9-S12. CrossRef PubMed
- 6. Ferreira JJ, Lees A, Rocha JF, Poewe W, Rascol O, Soares-da-Silva P; Bi-Park 1 investigators. Opicapone as an adjunct to levodopa in patients with Parkinson’s disease and end-of-dose motor fluctuations: a randomised, double-blind, controlled trial. Lancet Neurol. 2016;15(2):154-165. CrossRef PubMed
- 7. Katzenschlager R, Poewe W, Rascol O, et al. Apomorphine subcutaneous infusion in patients with Parkinson’s disease with persistent motor fluctuations (TOLEDO): a multicentre, double-blind, randomised, placebo-controlled trial. Lancet Neurol. 2018;17(9):749-759. CrossRef PubMed
- 8. Olanow CW, Kieburtz K, Odin P, et al; LCIG Horizon Study Group. Continuous intrajejunal infusion of levodopa-carbidopa intestinal gel for patients with advanced Parkinson’s disease: a randomised, controlled, double-blind, double-dummy study. Lancet Neurol. 2014;13(2):141-149. CrossRef PubMed
- 9. Mauskopf JA, Sullivan SD, Annemans L, et al. Principles of good practice for budget impact analysis: report of the ISPOR Task Force on good research practices--budget impact analysis. Value Health. 2007;10(5):336-347. CrossRef PubMed
- 10. Sullivan SD, Mauskopf JA, Augustovski F, et al. Budget impact analysis-principles of good practice: report of the ISPOR 2012 Budget Impact Analysis Good Practice II Task Force. Value Health. 2014;17(1):5-14. CrossRef PubMed
- 11. Stefani A, Tessitore A, Tambasco N, et al. Criteria for identification of advanced Parkinson’s disease: the results of the Italian subgroup of OBSERVE-PD observational study. BMC Neurol. 2022;22(1):41. CrossRef PubMed
- 12. von Campenhausen S, Winter Y, Rodrigues e Silva A, et al. Costs of illness and care in Parkinson’s disease: an evaluation in six countries. Eur Neuropsychopharmacol. 2011;21(2):180-191. CrossRef PubMed
- 13. Yang W, Hamilton JL, Kopil C, et al. Current and projected future economic burden of Parkinson’s disease in the U.S. NPJ Parkinsons Dis. 2020;6(1):15. CrossRef PubMed
- 14. ISTAT. Popolazione residente al 1 gennaio 2022. Online Accessed April 2022.