 |
Glob Reg Health Technol Assess 2022; 9: 58-67 ISSN 2283-5733 | DOI: 10.33393/grhta.2022.2290 ORIGINAL RESEARCH ARTICLE |
 |
Budget impact analysis sull’introduzione del dispositivo di telemonitoraggio Turbo+ nella gestione dei pazienti asmatici in Italia
Introduction of the telemonitoring device Turbo+ in the management of patients suffering from asthma in Italy: a budget impact analysis
Introduction: Adherence to long-term asthma control drugs is one of the key factors in improving disease management among patients with asthma. Poor adherence to long-term therapies significantly compromises the effectiveness of treatment and represents a problem in controlling the disease in terms of quality of life and economic impact. A budget impact analysis has been developed taking into account that Turbo+ technology (electronic monitoring device) can increase adherence to therapy in patients suffering from asthma.
Methods: Coherently with the budget impact model methodology, we developed two different scenarios. One represents the clinical practice assuming a constant market share of 0,99% for Turbo+ and the other one assumes an incremental market share of Turbo+ over the time horizon considered. An increase in adherence to therapy will likely correspond to a reduction of exacerbations and a lower rate of hospitalizations, thus generating savings in terms of use of health resources.
Results: The differential analysis shows an incremental saving in terms of resources absorbed by the National Health Service (NHS) over the time horizon considered. In the first year the savings are equal to € 795,658.64 and in the fifth year they are equal to € 3,520,636.34 for a total of resources saved in 5 years of € 10,882,028.50.
Conclusions: The model shows how the diffusion of the Turbo+ programme can lead to savings in terms of health resources consumed by the NHS. Further analyses with new real-world data on adherence in asthmatic patients could be useful in confirming the results of the present analysis.
Keywords: Adherence, Asthma, Budget impact analysis, Economic evaluation, Telemedicine
Received: July 5, 2021
Accepted: March 14, 2022
Published online: April 19, 2022
Indirizzo per la corrispondenza:
Filippo Rumi
Università Cattolica del Sacro Cuore
Alta Scuola di Economia e Management dei Sistemi Sanitari
Largo F. Vito 1
00168 Roma - Italy
filippo.rumi@unicatt.it
Global & Regional Health Technology Assessment - ISSN 2283-5733 - www.aboutscience.eu/grhta
© 2022 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
L’asma rappresenta una tra le principali cause di morbidità, mortalità e onere economico a livello mondiale. Si stima che siano circa 339 milioni le persone affette da asma a livello globale, e circa 3 milioni in Italia, di cui 300.000 con asma grave. L’Organizzazione Mondiale della Sanità (OMS) stima che le malattie respiratorie croniche rappresentino l’8,3% del carico di malattie croniche in tutto il mondo e che siano responsabili di più di 4 milioni di morti ogni anno (1). Le malattie respiratorie croniche, dunque, non solo hanno un impatto negativo sulla qualità di vita dei pazienti ma costituiscono anche un consistente onere sociale ed economico per i sistemi sanitari. Nel caso specifico dell’asma, in termini economici, questa incide da sola in misura maggiore rispetto a patologie gravi come tubercolosi e HIV in combinazione (2). L’asma è una malattia cronica, per la quale non esiste oggi alcun trattamento risolutivo. È possibile, però, controllarne il decorso, riducendo il numero e la gravità degli attacchi d’asma e migliorando la gestione dei sintomi. Al fine di mettere in atto un piano di controllo adeguato è importante che la malattia sia diagnosticata precocemente, con lo scopo di evitare gli effetti dannosi e le conseguenze a lungo termine dell’infiammazione cronica. La diagnosi di asma non è semplice, soprattutto nei primi anni di vita, e si basa essenzialmente sull’identificazione clinica dei sintomi respiratori tipici (tosse, mancanza di fiato, sibili respiratori, senso di oppressione toracica) suffragata dalla conferma funzionale tramite spirometria. In termini fisiopatologici, il processo infiammatorio bronchiale condiziona il livello di gravità dell’asma e costituisce il fattore che meglio risponde alla terapia con farmaci antinfiammatori somministrati per via inalatoria, anche in assenza di sintomi respiratori conclamati. Non esistono cure capaci di guarire definitivamente l’asma, ma è possibile gestire i sintomi garantendo a chi ne soffre una vita del tutto normale (3). Per ottenere ciò è necessario studiare delle soluzioni personalizzate per monitorare e trattare la condizione, come ridurre l’esposizione agli allergeni, eseguire test per valutare la gravità dei sintomi e ricorrere all’uso di farmaci. Il piano di trattamento deve essere elaborato e rivisto in base ai cambiamenti nei sintomi. Attualmente si ottengono ottimi risultati facendo assumere al paziente con regolarità dei farmaci in via aerosolica spray o in forma di polvere inalatoria in modo da arginare l’infiammazione cronica per evitare che degeneri e da arginare il broncospasmo, “allargando” i bronchi quando questi tenderebbero a restringersi. In ogni caso è lo specialista a decidere caso per caso quali farmaci prediligere, mentre l’asmatico deve essere sempre cosciente dei farmaci che assume e, secondo le indicazioni del medico, sapere come e quando variarne il dosaggio. In particolare, nella letteratura disponibile, la combinazione budesonide/formoterolo, tra le terapie a base di corticosteroidi inalatori raccomandati (ICS) dalle Linee Guida GINA (4), risulta possedere un profilo di costo efficacia dominante considerando la prospettiva sociale (costi diretti e indiretti) rispetto ad altre combinazioni di farmaci appartenenti alla stessa categoria. Per esempio, nel lavoro di Johansson et al. (5), partendo da dati del trial COSMOS (6), è stata valutata la costo-efficacia (CEA, Cost-Effectiveness Analysis) di budesonide-formoterolo in mantenimento e al bisogno rispetto a salmeterolo-fluticasone in mantenimento + salbutamolo al bisogno. L’analisi economica è stata condotta sulla base di dati raccolti in 246 centri in 16 paesi (Italia compresa). Come misura di efficacia è stato considerato il numero di esacerbazioni severe per paziente per anno, mentre per l’analisi dei costi sono stati considerati sia il consumo diretto di risorse che quello indiretto, rilevati nel trial.
I risultati in termini di efficacia raggiunti nei trial clinici dalle strategie farmacologiche disponibili si discostano dalla risposta dei pazienti con asma riscontrabile nella real-practice. Tale aspetto è spesso correlato a un’aderenza non ottimale alle terapie prescritte: l’incremento dell’aderenza alle terapie nell’ambito dell’asma rappresenta uno dei fattori chiave per migliorarne la gestione, in particolare tra i pazienti con malattia persistente (7). La scarsa aderenza alle terapie compromette in modo significativo l’efficacia del trattamento e rappresenta un problema importante per il raggiungimento del controllo di malattia, con un impatto sulla qualità di vita e in termini economici. L’uso regolare di corticosteroidi inalatori è associato a un minor rischio di morte per asma, mentre la non aderenza al regime terapeutico può comportare un controllo subottimale della patologia e un numero di ospedalizzazioni più elevato. A tal proposito, Williams et al. (8) hanno dimostrato come per ogni aumento del 25% dell’intervallo di tempo senza corticosteroide inalatorio, il tasso di ospedalizzazione correlato all’asma possa raddoppiare (tasso relativo 2.01; IC 95% 1,06 ± 3,79). L’aderenza subottimale ai trattamenti cronici rappresenta una problematica comune nell’asma, in pazienti sia adulti che in età pediatrica, e può arrivare fino al 50%. L’aderenza terapeutica subottimale determina uno scarso controllo della malattia, a cui consegue un più elevato rischio di esacerbazioni e, contestualmente, una maggiore spesa di gestione dei pazienti (9). Porta inoltre il paziente ad affrontare spesso un’escalation non necessaria di trattamenti, che possono essere sia dannosi per la salute che costosi (10). Dal 2017 è stato reso disponibile in Italia, dopo aver ottenuto la marcatura CE come dispositivo di Classe I, il primo e finora unico dispositivo elettronico in ambito respiratorio (Turbo+), che, grazie alla combinazione con una app per smartphone, permette il monitoraggio della terapia inalatoria nei pazienti con asma. Tramite software, infatti, è in grado di monitorare e registrare tutte le inalazioni attraverso l’app, mediante collegamento bluetooth con il dispositivo, così da offrire l’opportunità sia al paziente sia al medico curante di verificare la continuità terapeutica. Inoltre, l’app consente al paziente di impostare degli “alert” come promemoria per l’inalazione e di ricevere messaggi motivanti, supportandolo quindi nella regolarità di assunzione della terapia prescritta. Il device Turbo+ deve essere necessariamente assemblato al Turbohaler, inalatore multidose di polvere secca che contiene la combinazione fissa budesonide/formoterolo impiegata per il trattamento dell’asma sia in mantenimento che al bisogno. Tale dispositivo elettronico, attualmente disponibile per l’utilizzo esteso nella pratica clinica, è stato inizialmente testato presso centri specializzati nel trattamento delle patologie respiratorie croniche, che sono stati i primi a fare esperienza di questa innovativa tecnologia. Da un punto di vista gestionale, il medico provvede alla registrazione dei dati del paziente tramite un indirizzo mail associato con lo smartphone nel momento stesso in cui consegna l’inalatore, così da garantire una corrispondenza univoca tra device e paziente. Una volta collegato attraverso l’app, scaricabile dal paziente sul proprio smartphone, Turbo+ invia informazioni dettagliate sulla frequenza e sugli orari delle inalazioni, permettendo così al paziente un costante controllo della propria terapia. Il medico a sua volta avrà un accesso riservato attraverso un portale dedicato, in modo tale da poter verificare durante la visita di controllo se il paziente sia aderente o meno alla terapia. L’obiettivo di questo studio è stato quello di sviluppare un’analisi di budget impact, partendo dall’assunto base che la tecnologia Turbo+, grazie al monitoraggio puntuale che è in grado di fornire, sia potenzialmente in grado di implementare l’aderenza alla terapia in pazienti affetti da asma. L’ipotesi finale è che da un aumento dell’aderenza alla terapia possano verosimilmente avere origine una riduzione degli episodi di riacutizzazione e un minor tasso di ospedalizzazioni nei pazienti affetti da asma, generando così risparmi in termini di risorse sanitarie utilizzate.
Metodi
Descrizione del modello
Coerentemente con la metodologia del modello di “budget impact” sono stati sviluppati due diversi scenari: il primo dove si assume una quota costante di utilizzo del Turbo+ e un secondo dove viene assunta una quota di mercato incrementale in un orizzonte temporale di 5 anni. La prospettiva dello studio è quella del Servizio Sanitario Nazionale (SSN). Per la costruzione del modello, si è proceduto dapprima all’individuazione dei principali comparatori dell’intervento oggetto dell’analisi (ICS-LABA). In particolare, tali alternative consistono nelle combinazioni di budesonide/formoterolo, beclometasone/formoterolo, fluticasone/vilanterolo, fluticasone/salmeterolo e fluticasone/formoterolo somministrate senza l’ausilio di un dispositivo di monitoraggio dell’aderenza. In un secondo momento è stata identificata la popolazione oggetto dell’analisi. Infine, tramite una revisione della letteratura, sono state reperite evidenze al fine di popolare il modello con gli input clinici e i dati di costo. L’intervento dello studio è rappresentato dall’alternativa farmacologica budesonide/formoterolo e Turbohaler® associata all’utilizzo del dispositivo di monitoraggio Turbo+. Il comparatore dell’analisi è rappresentato dall’insieme dei farmaci corticosteroidi inalatori beta-agonisti a lunga durata d’azione (inhaled corticosteroids and long-acting β-agonists - ICS-LABA), terapia farmacologica di riferimento per la gestione dell’asma indicata dalle Linee Guida Global Initiative for Asthma (GINA) (4). Il costo medio annuale associato al ricorso a tali farmaci è stato stimato facendo riferimento al prezzo di acquisizione di ciascuna molecola così come riportato nelle Liste di Trasparenza dell’Agenzia Italiana del Farmaco (AIFA), Classe A (11), pesato per la posologia media/die indicata nel Riassunto delle Caratteristiche del Prodotto (RCP) di ciascun farmaco. In particolare, si è proceduto a calcolare la media semplice delle posologie minima e massima per ciascuna alternativa della classe ICS-LABA. I costi annuali associati alla posologia minima e massima delle terapie ICS-LABA così stimati sono stati associati ai pazienti affetti da asma intermittente o lieve e da asma moderata o severa rispettivamente. Per quanto concerne la popolazione, nella Tabella I sono mostrati i dati epidemiologici relativi alla popolazione target. In particolare, riferimento è stato fatto ai dati Istituto Italiano di Statistica (ISTAT) relativi all’anno 2021 (12). Per la stima della popolazione eleggibile negli anni successivi al primo, si tiene conto del dato di incidenza (nuovi casi per anno) aggiustato per il tasso di mortalità annuale (2020), come indicato nella seguente formula:
Pazienti eleggibili = (Pazienti asmatici in Italia+incidenza annuale asmaY) – (Pazienti asmatici in Italiay–1* tasso di mortalità popolazione generale)
Y = anno dell’analisi. Nel modello può assumere valori pari a 1,2 e 3.
Nell’analisi non vengono considerati i neonati e i bambini fino ai 6 anni, poiché, in questo sottogruppo, non c’è indicazione terapeutica all’uso di ICS-LABA. Successivamente la popolazione viene stratificata per età, sottogruppo pediatrico (6-18 anni) e sottogruppo degli adulti (>18 anni), oltre che per severità della condizione asmatica (intermittente, lieve, moderata e severa). Al fine della definizione della popolazione eleggibile, è stata considerata una percentuale di pazienti in trattamento con ICS-LABA nell’orizzonte temporale considerato pari all’85% e assumendo una graduale decrescita dell’1% annuo. Il razionale di tale assunzione deriva dall’autorizzazione all’immissione in commercio della tripla terapia in combinazione fissa per il trattamento dell’asma con ICS-LABA-LAMA (inhaled corticosteroids and long-acting β-agonists – long acting muscarinic agonists). I LAMA sono farmaci broncodilatatori a lunga durata d’azione, che agiscono su recettori diversi da quelli β2 sui quali agiscono i LABA. inoltre, è stato assunto che non vi siano elementi differenziali relativamente ai test di laboratorio, in quanto non sono state reperite evidenze di letteratura che giustificassero una variazione in tali driver associata alla maggiore aderenza. Nella Tabella I vengono, altresì, riportati le percentuali di consumo ICS-LABA utilizzate nel gruppo aderenti e non aderenti, il tasso per identificare l’aderenza media italiana (rapporto OSMED) e l’aderenza nel gruppo Turbo+ e, infine, le Market Share assunte per i due scenari. Per quanto concerne le assunzioni relative alla percentuale di consumo di ICS-LABA tra i gruppi “aderenti” (il valore soglia minimo di “medication possession ratio” con cui solitamente viene individuata l’aderenza terapeutica, 80%) e “non aderenti” (50%), le stesse sembrano essere coerenti con quanto riportato in letteratura nello studio di Jensen et al. (13). Il 50% è un’assunzione che gli Autori hanno ritenuto ragionevole per la valorizzazione del costo medio annuale associabile ai pazienti “non aderenti”, considerando un range di variazione del consumo effettivo che potrebbe variare dallo 0% al 79%.
Dapprima viene suddivisa la popolazione in adulta e pediatrica. In seguito viene calcolata la popolazione pesata con le Market Share (classe ICS-LABA e budesonide/formoterolo in combinazione con Turbo+). Successivamente viene fatta un’ulteriore suddivisione nella popolazione target andando a considerare i pazienti aderenti e non aderenti. Vengono poi associati i costi ai vari sottogruppi, assumendo che la popolazione aderente faccia in media una visita in meno durante l’anno con il medico di base o il medico specialista e facendo pesare i tassi di riduzione del rischio sulle riacutizzazioni (PS) e sulle ospedalizzazioni basati sugli odds ratio derivanti dalla metanalisi di Engelkes (9). I risultati vengono presentati sotto forma di differenziale tra gli scenari (Tab. II e di impatto sul singolo paziente stratificato per severità della condizione asmatica.
Nella Tabella III vengono riportati i driver di costo e le relative frequenze stratificate per severità della condizione utilizzate per lo sviluppo dei due scenari previsti nel modello. Gli altri elementi considerati sono:
- prezzo ICS-LABA: prezzo al netto degli sconti di legge con indicazione della posologia minima (somministrata alla popolazione con severità intermittente e lieve) e della posologia massima (somministrata alla popolazione con severità moderata e severa) (8);
- % di consumo ICS-LABA aderenti e non aderenti (assunzione): vengono assunti un consumo del farmaco pari all’80% per la popolazione aderente e un consumo pari al 50% per la popolazione non aderente;
- % di pazienti con asma intermittente, lieve, moderata e severa;
- visite dal medico di base pesate per la severità;
- visite dal medico specialista pesate per la severità;
- test di laboratorio annuali;
- % di pazienti con riacutizzazione che porta il paziente a eseguire un accesso in Pronto Soccorso (PS) o % di pazienti che eseguono un ricovero pesate per la severità dell’asma;
- costi di visite, test di laboratorio, Pronto Soccorso e ricoveri (questi ultimi pesati per i DRG di pazienti con e senza comorbidità (CC)). Nello specifico, come riportato nella Tabella III, viene assunta una quota di pazienti con comorbidità pari al 30% e senza comorbidità pari al 70%. Pertanto, le tariffe associate ai due DRG presi in considerazione vengono pesate per l’incidenza delle comorbidità (DRG 96: Bronchite e asma, età > 17 anni con CC; DRG 97: Bronchite e asma, età > 17 anni senza CC);
- riduzione percentuale del rischio nei pazienti aderenti che influiscono sui tassi di ospedalizzazione e riacutizzazione nella popolazione aderente;
- tassi di aderenza medi italiani (Rapporto OSMED) e tassi di aderenza stimati del “gruppo Turbo+”.
| Popolazione | |||||
|---|---|---|---|---|---|
| Input | Valore | Fonte | |||
| Popolazione Italiana (età maggiore di 6 anni) | 56.932.625 | (12) | |||
| Prevalenza Asma Italia | 4,50% | (4) | |||
| Incidenza della condizione asmatica | 0,26% | (14) | |||
| Pazienti asmatici in Italia | 2.561.968 | Calcolato | |||
| Nuovi casi per anno | 145.748 | Calcolato | |||
| Tasso di mortalità | 1,050% | (12) | |||
| % asma intermittente | 34,80% | (15) | |||
| % asma lieve | 26,80% | (15) | |||
| % asma moderata | 30,60% | (15) | |||
| % asma severa | 7,80% | (15) | |||
| Pazienti eleggibili/anno (popolazione asmatica) | Anno 1 | Anno 2 | Anno 3 | Anno 4 | Anno 5 |
| 2.680.815 | 2.825.315 | 2.969.545 | 3.113.778 | 3.258.011 | |
| Input di aderenza e Market Share | |||||
| % consumo di ICS-LABA aderenti | 80% | Assunzione | |||
| % di consumo ICS-LABA non aderenti | 50% | Assunzione | |||
| Tasso di aderenza (Standard of Care) | 12,6% | (10) | |||
| Tasso di aderenza (Turbo+) | 63%-54%* | Real-life | |||
| Market Share Scenario ICS-LABA (quota costante di Turbo+: 0,09%) | 0,09%-99,01% | Assunzione | |||
| Market Share/anno | |||||
| SCENARIO AS IS | |||||
| Anno 1 | Anno 2 | Anno 3 | Anno 4 | Anno 5 | |
| Turbo+ | 0,09% | 0,09% | 0,09% | 0,09% | 0,09% |
| ICS-LABA | 99,01% | 99,01% | 99,01% | 99,01% | 99,01% |
| SCENARIO AS IS | |||||
| Turbo+ | 4,00% | 8,00% | 10,00% | 13,00% | 16,00% |
| ICS-LABA | 96,00% | 92,00% | 90,00% | 87,00% | 84,00% |
| Pazienti | 2.680.815 | 2.825.315 | 2.969.545 | 3.113.778 | 3.258.011 |
(*) Al fine di stimare l’aderenza nel gruppo Turbo+ è stata analizzata una serie di esperienze in real-life in diversi contesti regionali italiani. In particolare, sono stati identificati dei gruppi di lavoro regionali composti da clinici di comprovata esperienza nella gestione di pazienti affetti da asma nel setting italiano. Tali gruppi hanno seguito un pool di pazienti asmatici per un periodo compreso tra 90 giorni e 180 giorni.
| SCENARIO AS IS | ||||||
|---|---|---|---|---|---|---|
| Anno 1 | Anno 2 | Anno 3 | Anno 4 | Anno 5 | TOTALE | |
| Popolazione asmatica (adulta) | 1.985.525 | 2.067.929 | 2.147.621 | 2.224.801 | 2.299.467 | 10.725.343 |
| Popolazione asmatica (pediatrica) | 293.168 | 305.335 | 317.101 | 328.497 | 339.522 | 1.583.623 |
| Voci di costo (adulti) | ||||||
| Costo ICS-LABA | € 528.069.014,28 | € 549.984.085,74 | € 571.169.311,32 | € 591.678.319,58 | € 611.535.583,86 | € 2.852.436.314,80 |
| Visite | € 309.179.756,83 | € 322.011.615,18 | € 334.421.843,78 | € 346.441.818,69 | € 358.068.722,23 | € 1.670.123.756,70 |
| Test di laboratorio | € 157.015.325,90 | € 163.531.860,84 | € 169.833.853,44 | € 175.937.239,56 | € 181.841.853,86 | € 848.160.133,60 |
| Pronto Soccorso | € 208.900.119,93 | € 217.570.290,81 | € 225.957.112,73 | € 234.081.779,04 | € 241.937.777,13 | € 1.128.447.079,66 |
| Ricovero | € 558.935.961,41 | € 582.133.986,86 | € 604.573.880,01 | € 626.312.346,11 | € 647.331.959,92 | € 3.019.288.134,32 |
| Voci di costo (pazienti pediatrici) | ||||||
| Costo ICS-LABA | € 77.970.676,50 | € 81.206.490,19 | € 84.334.540,36 | € 87.362.745,40 | € 90.294.718,85 | € 421.169.171,30 |
| Visite | € 45.651.144,35 | € 47.545.799,50 | € 49.378.199,99 | € 51.152.978,57 | € 52.869.719,20 | € 246.597.841,62 |
| Test di laboratorio | € 23.183.695,41 | € 24.145.877,67 | € 25.076.382,23 | € 25.977.562,06 | € 26.849.392,75 | € 125.232.910,11 |
| Pronto Soccorso | € 30.688.661,76 | € 31.962.366,59 | € 33.194.486,09 | € 34.388.133,54 | € 35.542.230,68 | € 165.775.878,66 |
| Ricovero | € 82.110.994,82 | € 85.518.936,54 | € 88.815.612,00 | € 92.009.351,10 | € 95.097.268,87 | € 443.552.163,33 |
| TOTALE | € 2.021.705.351,20 | € 2.105.611.309,93 | € 2.186.755.221,96 | € 2.265.342.273,66 | € 2.341.369.227,36 | € 10.920.783.384,11 |
| SCENARIO TO BE | ||||||
| Anno 1 | Anno 2 | Anno 3 | Anno 4 | Anno 5 | TOTALE | |
| Popolazione asmatica (adulta) | 1.985.525 | 2.067.929 | 2.147.621 | 2.224.801 | 2.299.467 | 10.725.343 |
| Popolazione asmatica (pediatrica) | 293.168 | 305.335 | 317.101 | 328.497 | 339.522 | 1.583.623 |
| Voci di costo (adulti) | ||||||
| Costo ICS-LABA | € 534.567.372,04 | € 563.576.295,20 | € 587.820.053,62 | € 611.663.519,52 | € 636.991.487,09 | € 2.934.618.727,47 |
| Visite | € 307.739.430,18 | € 318.986.803,83 | € 330.589.178,75 | € 341.516.966,29 | € 351.795.751,91 | € 1.650.628.130,96 |
| Test di laboratorio | € 157.015.325,90 | € 163.531.860,84 | € 169.833.853,44 | € 175.937.239,56 | € 181.841.853,86 | € 848.160.133,60 |
| Pronto Soccorso | € 207.360.300,03 | € 214.350.986,43 | € 222.028.457,45 | € 229.404.813,18 | € 235.980.549,24 | € 1.109.125.106,33 |
| Ricovero | € 554.815.998,65 | € 573.520.372,88 | € 594.062.317,27 | € 613.798.593,55 | € 631.392.721,11 | € 2.967.590.003,46 |
| Voci di costo (pediatrici) | ||||||
| Costo ICS-LABA | € 78.930.174,85 | € 83.213.413,03 | € 86.793.063,03 | € 90.313.608,86 | € 94.053.344,98 | € 433.303.604,76 |
| Visite | € 45.438.476,61 | € 47.099.178,74 | € 48.812.297,66 | € 50.425.812,11 | € 51.943.499,85 | € 243.719.264,98 |
| Test di laboratorio | € 23.183.695,41 | € 24.145.877,67 | € 25.076.382,23 | € 25.977.562,06 | € 26.849.392,75 | € 125.232.910,11 |
| Pronto Soccorso | € 30.432.721,43 | € 31.427.271,66 | € 32.541.486,79 | € 33.610.754,20 | € 34.552.053,28 | € 162.564.287,36 |
| Ricovero | € 81.426.197,45 | € 84.087.229,37 | € 87.068.438,31 | € 89.929.384,51 | € 92.447.936,95 | € 434.959.186,59 |
| TOTALE | € 2.020.909.692,56 | € 2.103.939.289,65 | € 2.184.625.528,55 | € 2.262.578.253,84 | € 2.337.848.591,02 | € 10.909.901.355,61 |
| Budget Impact | –€ 795.658,64 | –€ 1.672.020,28 | –€ 2.129.693,42 | –€ 2.764.019,82 | –€ 3.520.636,34 | –€ 10.882.028,50 |
| DRIVER | INTERMITTENTE | LIEVE | MODERATA | SEVERA | COSTO | FONTE | |
|---|---|---|---|---|---|---|---|
| Visite | |||||||
| Medico di base | 3,1 | 4,8 | 6,2 | 8,6 | 15,17 € | (15) | |
| Specialista | 3,5 | 4,5 | 4,3 | 4,7 | 20,66 € | (15) | |
| Test di laboratorio | Assunti uguali per tutte le severità | ||||||
| Spirometria | 37,18 € | ||||||
| Test per allergia | 23,24 € | ||||||
| Emocromo | 3,17 € | ||||||
| Raggi X | 15,49 € | ||||||
| Pronto Soccorso | 0,1 | 0,4 | 0,5 | 1,4 | 261,35 € | ||
| Ricovero | Con comorbidità (30%) | 0,03 | 0,16 | 0,12 | 0,46 | 1.832,00 € | DRG 96 |
| Senza comorbidità (70%) | 0,03 | 0,16 | 0,12 | 0,46 | 2.537,00 € | DRG 97 | |
| 100% | 2.325,50 € | 2.325,50 € | 2.325,50 € | 2.325,50 € | |||
| Con comorbidità 30%; senza comorbidità (70%); assunzione – DRG 96; DRG 97 | 30% (2.537 €) | 70% (1.832 €) | |||||
Il modello assume dunque che nel gruppo che non utilizza il dispositivo Turbo+ il tasso di aderenza medio sia pari all’11%. Ciò vuol dire che l’11% della popolazione eleggibile assume in media l’80% della dose prescritta di ICS-LABA. Al contrario l’89% (il gruppo dei non aderenti) assume in media il 50% della dose prescritta di ICS-LABA (assunzione). Al fine di stimare l’aderenza nel gruppo Turbo+ è stata analizzata una serie di esperienze in real-life in diversi contesti regionali italiani. In particolare, sono stati identificati dei gruppi di lavoro regionali composti da clinici di comprovata esperienza nella gestione di pazienti affetti da asma nel setting italiano. Tali gruppi hanno seguito un pool di pazienti asmatici per un periodo compreso tra 90 giorni e 180 giorni. Per ciascuna regione, al termine del periodo di follow-up, è stata organizzata una sessione di presentazione dei risultati emersi durante la gestione dei pazienti mediante il dispositivo di monitoraggio. Le regioni partecipanti all’analisi sono: Lazio, Calabria, Campania, Liguria, Veneto, Sicilia, Puglia, Marche, Piemonte, Lombardia e Toscana e sono stati complessivamente arruolati circa 1.500 pazienti. Il tasso di aderenza è stato monitorato per un orizzonte temporale di breve periodo (3-6 mesi) e poi esteso a 12 mesi per imputarlo nel modello. È stato poi assunto un tasso di persistenza decrescente nei 5 anni in modo tale da essere conservativi rispetto al tasso di aderenza associato al dispositivo oggetto di questa analisi. Nel caso base il modello considera un tasso di aderenza al primo anno nel gruppo Turbo+ pari al 63%, fino ad arrivare al 54% dopo 4 anni. Il modello dunque assume che, nell’orizzonte temporale considerato, circa 6 pazienti su 10 nel gruppo Turbo+ consumino almeno l’80% della terapia prescritta e vengono considerati “aderenti”. Di seguito vengono riportate le altre assunzioni del modello supportate da evidenze di letteratura disponibili o in assenza di riferimento bibliografico concordate con il gruppo di clinici coinvolto nell’analisi:
- nel modello viene assunto che i pazienti aderenti almeno all’80% alle terapie con ICS-LABA effettuino in media una visita dal medico di base o dallo specialista in meno rispetto ai pazienti meno aderenti;
- il modello prevede che i pazienti aderenti almeno all’80% alle terapie con ICS-LABA abbiano una riduzione del rischio di riacutizzazioni e ospedalizzazioni stimato con una media semplice degli odds ratio in gruppi di pazienti aderenti/non aderenti che avevano come outcome la riduzione del rischio di andare incontro a una riacutizzazione o a un’ospedalizzazione per via della condizione asmatica (15) (Tab. IV). Come si evince nella Tabella vi è una riduzione del rischio correlata all’aderenza per quanto concerne le ospedalizzazioni e gli accessi al Pronto Soccorso. Contrariamente, l’aderenza non sembra essere correlata a una riduzione nell’utilizzo di corticosteroidi orali (OCS);
- il modello non considera un tasso di persistenza variabile nell’orizzonte temporale dell’analisi;
- i tassi di riacutizzazione e ospedalizzazioni sono stati stimati da fonti scientifiche in letteratura (9,15) e sono stati correlati alla severità della condizione asmatica, valorizzando economicamente le voci con il tariffario delle prestazioni ambulatoriali specialistiche e il tariffario DRG (16,17) (Tab. III);
- infine, il modello assume, ai fini della presente analisi, che il dispositivo Turbo+ venga distribuito gratuitamente. Per esplorare in maniera più dettagliata questa assunzione è stata condotta un’analisi di sensibilità sul prezzo del dispositivo nella quale i risultati appaiono robusti nonostante gli scostamenti considerati. Tale analisi non viene riportata all’interno del seguente studio in quanto non è disponibile un benchmark di riferimento relativo al prezzo medio ipotizzabile per il dispositivo oggetto di questa valutazione.
| Odds Ratio (OR) gruppo aderenti/non aderenti (popolazione pediatrica) | ||||||
|---|---|---|---|---|---|---|
| Riferimento | Design | Partecipanti | Outcome | Aderenza | OR | Fonte |
| Rust (2013) | Cohort | 43.166 | Hosp/ED | CTR: < 0,5 or > 0,5/CTR: < 0,5 or > 0,5 | 0,59 | (9) |
| Bukstein (2007) | Cohort | 11.407 | Comb: ED/Hosp | 0,6 | (9) | |
| Camargo (2007) | Cohort | 10.976 | Comb: ED/Hosp | Prescriptions ≥ 2 versus 1 | 0,32 | (9) |
| Herndon (2012) | Cohort | 10.878 | Hosp | MPR: median (0,08) versus less | 0,96 | (9) |
| Elkout (2012) | Cohort | 3.172 | ED | MPR: > 50% versus < 19% | 0,56 | (9) |
| OCS | MPR: > 50% versus < 19% | 1,02 | (9) | |||
| MEDIA | 0,606* | |||||
| Odds Ratio (OR) gruppo aderenti/non aderenti (popolazione adulta) | ||||||
| Riferimento | Design | Partecipanti | Outcome | Aderenza | OR | Fonte |
| Stern (2006) | Cohort | 97.743 | Comb: ED/Hosp | MPR: 75th perc versus less | 0,86 | (9) |
| Delea (2008) | Cohort | 12.907 | OCS; Comb: ED/Hosp | Mean MPR: +25% | 0,97 | (9) |
| Balkrishnan (2000) | Cohort | 751 | Comb: ED/Hosp | Refills: 2 versus 0 | 0,62 | (9) |
| Williams (2004) | Cohort | 405 | OCS | Median CMA: +25% | 0,75 | (9) |
| Williams (2011) | Cohort | 298 | Comb: ED/Hosp/OCS | MPR: >75% versus <25% | 0,58 | (9) |
| McMahon (2000) | 4.535 | Hosp + OCS; Hosp | Adh: 90 versus 1-89 days | 1,02 | (9) | |
| Smith (2009) | 3.013 | Comb: ED/Hosp | MPR: >80% versus <50% | 0,47 | ||
| MEDIA | 0,65 | |||||
(*) La media tiene conto della riduzione del rischio del gruppo aderenti di incorrere in un’ospedalizzazione o a un accesso in Pronto Soccorso. Come si evince dagli Odds Ratio riportati, non si registra una variazione tra i due gruppi nel consumo di OCS.
Hosp: ricovero per asma; ED: visita al Pronto Soccorso per asma; CTR: rapporto tra controller e farmaco totale; MPR: medication possession ratio (misura dell’aderenza terapeutica); OCS: corticosteroidi orali; OR: Odds Ratio; Comb: combinato.
Risultati
I risultati sono espressi come differenziale tra lo scenario in cui si assume una quota di mercato costante di Turbo+ (AS IS) nell’orizzonte temporale considerato e lo scenario alternativo in cui viene assunta una diffusione incrementale del dispositivo nei 5 anni di analisi (TO BE). I driver considerati includono i costi della terapia farmacologica, i costi delle prestazioni generate dal diverso tasso di aderenza dei pazienti, quelli relativi alla gestione delle riacutizzazioni e delle ospedalizzazioni nonché il costo delle visite. I risultati derivanti dal differenziale tra i due scenari evidenziano un risparmio in termini di risorse assorbite dal Servizio Sanitario Nazionale incrementale nell’orizzonte temporale considerato. Al primo anno i risparmi sono pari a 795.658,64 € e al quinto anno risultano essere pari a 3.520.636,34 € per un totale di risorse risparmiate nei 5 anni di 10.882.028,50 €.
Nella Figura 1 vengono riportati i dati di impatto sul budget per paziente, stratificati per severità della patologia asmatica. Per quanto riguarda l’asma intermittente, il risparmio medio a paziente annuo derivante dal confronto dei due scenari è pari a 177,08 €. I risparmi derivano da tutti i driver considerati, a eccezione dei test di laboratorio che non generano alcun differenziale nel modello. Il risparmio per il paziente lieve è pari a 313,99 €. Anche in questo caso, i risparmi derivano dalla riduzione dei costi di ICS-LABA, dei ricoveri, degli accessi al PS e delle visite dal medico di base. Nei pazienti intermittenti e lievi, nonostante l’aumento dell’aderenza che dovrebbe comportare un aumento dei costi di ICS-LABA, si evidenzia un risparmio anche in termini di terapia farmacologica prescritta (ICS-LABA). Questo perché i costi della posologia minima di budesonide/formoterolo e Turbohaler (Turbo+) sono inferiori rispetto alla media dei costi associati alla posologia minima della classe ICS-LABA che è stata utilizzata. Discorso diverso per quanto riguarda la posologia massima; in questo caso il costo annuale di Budesonide/formoterolo e Turbohaler è superiore rispetto alla media dei costi associati alla posologia massima dei farmaci presenti nella classe ICS-LABA. Pertanto, la classe di severità moderata rappresenta l’unica nella quale non si verifica un risparmio in termini di profilo di budget impact medio per paziente. In questa classe, i maggiori costi di ICS-LABA non riescono a essere completamente compensati dalla riduzione di ospedalizzazioni, accessi al PS e visite dal medico, generando un aggravio di € 16,11/paziente. Infine, nella classe “severa” si evidenzia un risparmio di 342,95 € a paziente. In questo caso gli aumentati costi della terapia farmacologica vengono ampiamente compensati dalla riduzione sugli altri driver di costo. Per quanto riguarda i costi della terapia, vengono considerati una spesa di 733,9 € per la posologia massima di budesonide/formoterolo in associazione con il dispositivo di monitoraggio e un costo di 367,0 € per la posologia minima. Per quanto riguarda invece il costo medio della classe ICS-LABA viene considerata una spesa di 537,7 € per la posologia massima e di 474,6 € per la posologia minima. Tale posologia viene associata ai pazienti che presentano asma intermittente e lieve, mentre la posologia massima viene associata a quei pazienti che presentano asma moderata e severa.
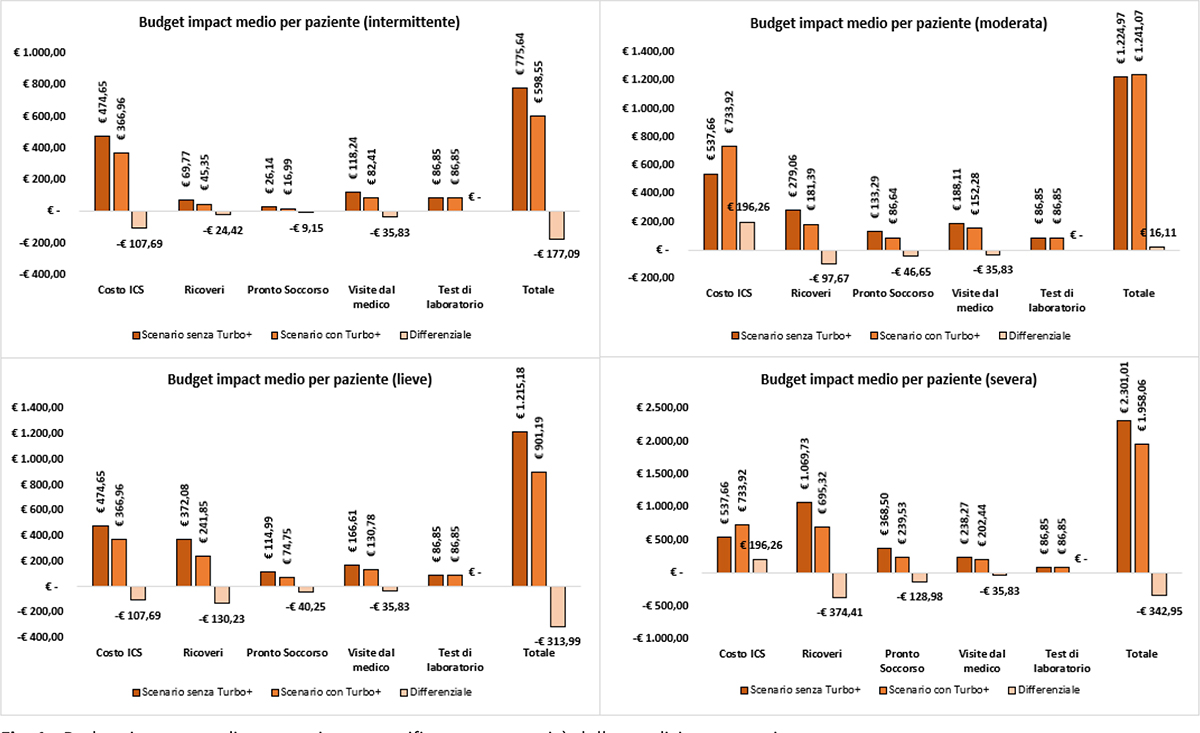
Fig. 1 - Budget impact medio per paziente stratificato per severità della condizione asmatica.
Analisi di sensibilità
È stata sviluppata un’analisi di sensibilità deterministica per caratterizzare l’incertezza dei parametri utilizzati per sviluppare il modello. Tutti i driver sono stati fatti variare in un range prestabilito (±15%) per analizzare quanto tali scostamenti possano influenzare i risultati di impatto sul budget. Il parametro caratterizzato da maggiore incertezza è rappresentato dalla quota di mercato associata all’utilizzo del dispositivo Turbo+ nel quinto anno dell’orizzonte temporale considerato, seguito dal costo medio degli ICS-LABA e dall’odds ratio delle ospedalizzazioni nel gruppo adulti. La percentuale nel gruppo di severità “severa”, il tasso di utilizzo del Turbo+ al primo anno e la percentuale nel gruppo di severità “intermittente” sono tra i parametri il cui scostamento potrebbe avere un impatto significativo sui risultati dell’analisi (Fig. 2).
Discussione
Il modello mostra come la diffusione del dispositivo Turbo+ possa portare a considerevoli risparmi in termini di risorse sanitarie consumate da parte del Servizio Sanitario Nazionale. L’assunzione di base che considera come un paziente più aderente possa andare incontro a minori complicanze in termini di riacutizzazioni, ospedalizzazioni e visite dal medico trova riscontri nella letteratura scientifica analizzata con particolare riferimento alla metanalisi condotta da Engelkes et al. (9). Come si evince dai risultati, la diffusione di un dispositivo in grado, al contempo, di monitorare l’aderenza al trattamento farmacologico del paziente e di migliorare gli esiti clinici della condizione (ospedalizzazioni, accessi in Pronto Soccorso, ecc.) permette un potenziale risparmio di risorse sanitarie in termini di costi diretti evitati. Dall’analisi si evince che i pazienti che godrebbero maggiormente dell’utilizzo del dispositivo oggetto di analisi sono i pazienti con asma lieve e grave. È importante sottolineare che, nonostante nell’analisi siano stati considerati anche i pazienti moderati per i quali non si verifica un risparmio significativo, è comunque emerso un risparmio incrementale in termini di risorse assorbite dal Servizio Sanitario Nazionale pari a 10.882.028,50 € nell’orizzonte temporale di 5 anni considerato. In tale contesto, è necessario chiarire inoltre che il modello non è in grado di prevedere se i pazienti con asma intermittente e lieve possano trarre un beneficio nell’utilizzare Turbo+ al punto di non progredire in uno stato più severo dell’asma. Pertanto, si andrebbe a configurare una situazione favorevole con una minore quota di pazienti interessati da forme severe, e questo potrebbe avere non solo un impatto in termini positivi sull’assorbimento delle risorse sanitarie ma anche determinare una riduzione dei costi indiretti, generando quindi un importante risparmio economico anche nella prospettiva dell’intera società. Con il diffondersi del dispositivo di monitoraggio elettronico Turbo+ sarebbe auspicabile avere ulteriori dati nel contesto di “real-life” nel lungo periodo al fine di confermare i risultati raggiunti da questo modello di budget impact. Va infine sottolineato che, alla luce del contesto emergenziale che stiamo affrontando a causa della pandemia globale, si è assistito a una profonda evoluzione nell’organizzazione dell’erogazione dei servizi assistenziali e a una accelerazione senza precedenti verso l’innovazione digitale. Le cure parzialmente sospese a causa dei provvedimenti urgenti adottati dal governo e le norme di distanziamento sociale hanno evidenziato alcuni limiti dell’assistenza sanitaria tradizionale e la necessità di servizi accessibili da remoto anche sotto forma di Telemedicina. È proprio in questo contesto che i dispositivi come Turbo+, in grado di monitorare da remoto l’aderenza dei pazienti asmatici, assumono ancora più rilevanza, rappresentando uno strumento innovativo e allo stesso tempo utile sia per i pazienti che per i professionisti sanitari coinvolti nei processi di cura. Un limite da considerare nel ricorso a tale dispositivo risiede nella peculiarità di essere un device utilizzabile solo in combinazione con una terapia farmacologica (confezione specifica di budesonide/formoterolo) Si può ritenere, inoltre, che tale dispositivo, in quanto device che rende possibile il monitoraggio a distanza del comportamento del paziente rispetto alla terapia, consenta di ottenere un’innovazione di processo e di prodotto in linea con le prerogative auspicate dalle recenti linee di indirizzo sulla Telemedicina (18). Un ulteriore limite dell’analisi risiede nel fatto che i dati che hanno portato a stimare il tasso di aderenza nel gruppo che utilizza il dispositivo fanno riferimento a un campione di pazienti che potrebbe non essere rappresentativo della popolazione generale in quanto tali dati fanno riferimento al pool di pazienti in gestione presso i centri coinvolti nell’ambito degli studi “real-life” che sono stati condotti durante la realizzazione della presente analisi. In tale contesto è opportuno sottolineare che i dati primari per popolare il modello sono stati ricevuti in forma aggregata e con le determinazioni di sintesi, vale a dire che non vi è stata la possibilità di disporre di dati analitici. Infine, la presente analisi non considera alcun prezzo di cessione associato al dispositivo. Qualora il dispositivo fosse invece associato a un costo di acquisizione si dovrebbe considerare l’eventuale spesa aggiuntiva a carico del Servizio Sanitario Nazionale.
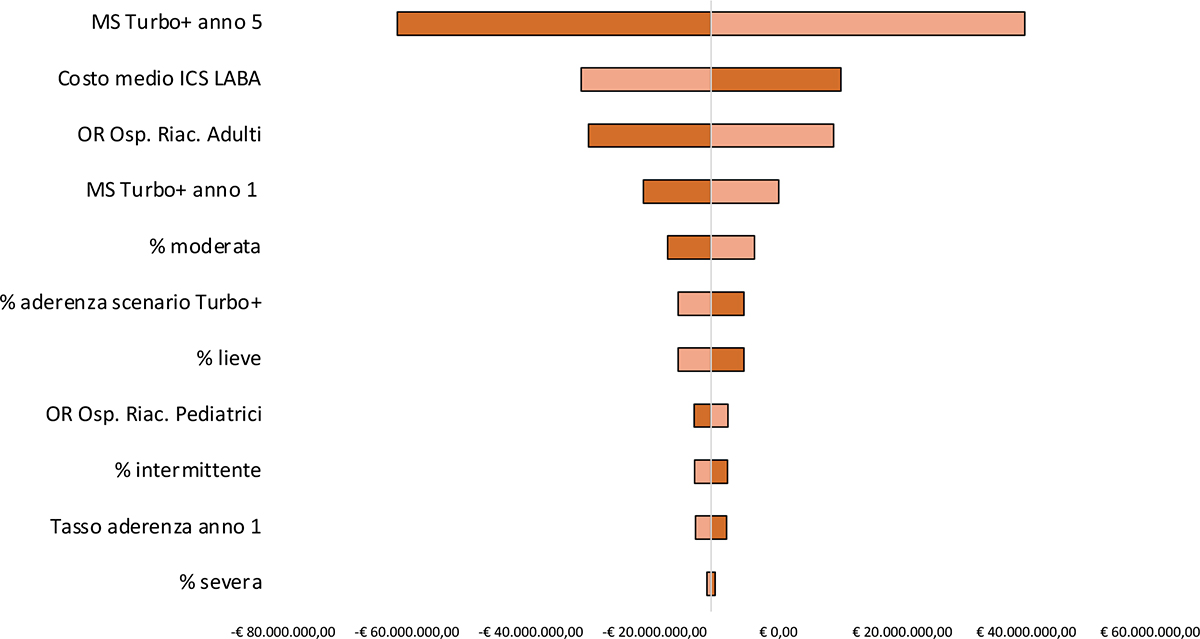
Fig. 2 - Analisi di sensibilità deterministica.
Acknowledgements
Desideriamo ringraziare i membri dei Board che hanno contribuito a questo lavoro:
Andò Filippo (AOU Azienda Policlinico Universitario, Messina); Catalano Filippo (Ospedali Riuniti Villa Sofia-Cervello, Palermo); Gammeri Enrico (AUSL 5, Messina); Viviano Vittorio (Centro Salus, Palermo); Selvaggio David (Ospedale Cristo Re, Roma); Ricci Alberto (Azienda Ospedaliero Universitaria e Policlinico Sant'Andrea, Roma); Graziani Elda (Ospedale Policlinico Umberto I, Roma); Balbo Piero Emilio (UOA Pneumologia, Ospedale Maggiore della Carità. Novara); Biglia Carlotta (Ospedale Mauriziano Umberto I, Torino); Crida Benedetta (Ospedale Infantile Regina Margherita, Torino); Malerba Mario (Ospedale S. Andrea, Vercelli); Maugeri Laura (AOU San Luigi Gonzaga, Orbassano,TO); Nicola Stefania (AUSL Valle D'Aosta); Omodeo Pinuccia (Ospedale SS. Antonio e Biagio e C. Arrigo, Alessandria); Ricciardolo Fabio (AOU San Luigi Gonzaga, Orbassano, TO); Caminati Marco (Azienda Ospedaliera Universitaria Integrata, Verona); Carobene Loredana (Azienda Ospedaliera Universitaria Senese, Siena); Corsi Lorenzo (Azienda Provinciale per i Servizi Sanitari, APSS, Trento); Buzzulini Francesca (Ospedale Santa Maria degli Angeli, Pordenone); De Carli Marco (Azienda Sanitaria Universitaria Integrata, Udine); Ferraro Valentina Agnese (Azienda Ospedaliera, Padova); Battistella Laura (ULSS 3 Serenissima, Venezia-Mestre e ULSS 6 Euganea, Padova); Chizzolini Maddalena (Ospedale Riabilitativo ad Alta Specializzazione Oras, Motta di Livenza, Treviso – ULSS 2 Marca Trevigiana); Romagnoli Micaela (Ospedale Cà Foncello, AULSS 2 Marca Trevigiana, Treviso); Nordio Beatrice (ULSS 6 Euganea, Padova); Salvador Vittorino (Azienda ULSS 8 Asolo, Treviso); Mincarini Marcello (Ospedale Policlinico San Martino, Genova); Castagneto Corrado (ASL 4 Chiavarese, Chiavari, GE); Nicolini Antonello (ASL 4 Chiavarese, Chiavari, GE); Serra Maria (ASL 3 Genovese, Genova); Fascie Clara (ASL 3 Genovese, Genova); Milanese Manlio (ASL 2 Savonese, Savona); Franceschi Paolo (Ospedale San Paolo, Savona); Bancalari Lorenza (ASL 5 Spezzino, Ospedale San Bartolomeo, Sarzana, La Spezia); Fumagalli Federica (Presidio Ospedaliero San Filippo Neri, ASL Roma 1, Roma); Macchia Luigi (Azienda Ospedaliero-Universitaria Policlinico, Bari); Arezzo Cesare (Ospedale San Paolo, Bari); Schino Pietro (Ospedale Miulli ,Acquaviva Delle Fonti, Bari); Satriano Francesco (Poliambulatorio Ex Vito Fazzi, Lecce); Loconte Filomena (Presidio Ospedaliero, Ostuni Fasano, Brindisi); Carbonara Anna Maria (Ospedale Di Venere, Carbonara, Bari).
Disclosures
Conflict of interest: The Authors declare no conflict of interest.
Financial support: This article was produced with unconditional support from AstraZeneca.
Bibliografia
- 1. Global Asthma Network. The Global Asthma Report 2018. Online (Accessed June 2021)
- 2. Vos T, Lim SS, Abbafati C, et al; GBD 2019 Diseases and Injuries Collaborators. Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2020;396(10258):1204-1222. CrossRef PubMed
- 3. Brian C. Leutholtz, Ignacio Ripoll, Exercise and disease management, 2nd. CRC Press; 2011:100.
- 4. Global Initiative for Asthma (GINA) – Global Strategy for Asthma Management and Prevention; Online (Accessed May 2021)
- 5. Johansson G, Andreasson EB, Larsson PE, Vogelmeier CF. Cost effectiveness of budesonide/formoterol for maintenance and reliever therapy versus salmeterol/fluticasone plus salbutamol in the treatment of asthma. Pharmacoeconomics. 2006;24(7):695-708. CrossRef PubMed
- 6. Vogelmeier C, D’Urzo A, Pauwels R, et al. Budesonide/formoterol maintenance and reliever therapy: an effective asthma treatment option? Eur Respir J. 2005;26(5):819-828. CrossRef PubMed
- 7. Assessing national capacity for the prevention and control of noncommunicable diseases: report of the 2019 global survey. Geneva: World Health Organization; 2020. Licence: CC BY-NC-SA 3.0 IGO; Online (Accessed May 2021)
- 8. Williams LK, Pladevall M, Xi H, et al. Relationship between adherence to inhaled corticosteroids and poor outcomes among adults with asthma. J Allergy Clin Immunol. 2004;114(6):1288-1293. CrossRef PubMed
- 9. Engelkes M, Janssens HM, de Jongste JC, Sturkenboom MC, Verhamme KM. Medication adherence and the risk of severe asthma exacerbations: a systematic review. Eur Respir J. 2015;45(2):396-407. CrossRef PubMed
- 10. L’uso dei farmaci in Italia – Rapporto nazionale anno 2019; Online (Accessed May 2021)
- 11. Agenzia Italiana del Farmaco (AIFA); Online (Accessed May 2021)
- 12. Istituto Nazionale di Statistica – Popolazione residente al 1° gennaio – Online (Accessed May 2021)
- 13. Jensen, F.F., Håkansson, K.E.J., Overgaard Nielsen, B. et al. Self-reported vs. objectively assessed adherence to inhaled corticosteroids in asthma. Asthma Res Pract. 2021 May 31;7(1):7. CrossRef PubMed
- 14. Pesce G, Locatelli F, Cerveri I, et al. Seventy Years of Asthma in Italy: Age, Period and Cohort Effects on Incidence and Remission of Self-Reported Asthma from 1940 to 2010. PLoS One. 2015;10(10):e0138570. CrossRef PubMed
- 15. Antonicelli L, Bucca C, Neri M, et al. Asthma severity and medical resource utilisation. Eur Respir J. 2004;23(5):723-729. CrossRef PubMed
- 16. Ministero della Salute – Tariffario delle prestazioni di assistenza specialistica per acuti (DRG); Online (Accessed May 2021)
- 17. Prestazioni Di Assistenza Specialistica Ambulatoriale – Allegato III – Online (Accessed May 2021)
- 18. Ministero della Salute – Telemedicina – Linee di indirizzo Nazionali. Online (Accessed May 2021)