 |
AboutOpen | 2021; 8: 92-98 ISSN 2465-2628 | DOI: 10.33393/ao.2021.2285 ORIGINAL RESEARCH ARTICLE |
 |
Sorveglianza delle infezioni correlate all’assistenza e monitoraggio degli antibiotici in terapia empirica in un reparto di medicina interna
ABSTRACT
Surveillance of hospital-acquired infections and monitoring of empiric antibiotic therapy in an internal medicine department
Introduction: Hospital-acquired infections (HAIs) are the most serious and frequent complication of healthcare systems. In 2019 the Marche Region has introduced a project to check HAIs and also the use of antibiotics in empirical therapy. The aim of this analysis was to conduct a periodic descriptive prevalence study according to the regional plan.
Materials and Methods: In the quarter January-March 2020, the Internal Medicine Department of the Mazzoni Hospital of Ascoli Piceno has been considered, enrolling patients with HAIs to whom has been prescribed at least one antibiotic in empirical therapy. To assess the prevalence of multi-drug resistant organisms (MDRO), microbiological isolates were examined and laboratory response times were measured as a quality indicator. Besides, the incidence of HAIs from medical device, the clinical outcomes and the average length of stay have been analyzed.
Results: The results show: high incidence of HAIs and high percentage of MDRO. The response time of the laboratory analysis is on average over 48-72 hours after sampling. The data show a widespread use of broad-spectrum antibiotics and low adherence to the new regional empiric therapy guidelines.
Conclusions: The high incidence of HAIs implies the urgent need of an active surveillance of an Antimicrobial Stewardship team. This would represent a strategic solution to prevent and limit antimicrobial resistance and reduce morbidity, mortality and costs.
Keywords: Alert Organism, Antimicrobial Resistance, Antimicrobial Stewardship, Empirical Antibiotic Therapy, Hospital-Acquired Infections
Received: June 14, 2021
Accepted: November 11, 2021
Published online: December 8, 2021
AboutOpen - ISSN 2465-2628 - www.aboutscience.eu/aboutopen
© 2021 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0).
Commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
Negli ultimi anni, il tema della sorveglianza delle Infezioni Correlate all’Assistenza (ICA) e del contenimento della diffusione dei microrganismi multiresistenti è sempre più all’attenzione delle Strutture Sanitarie (1,2).
Il Piano Nazionale di Contrasto dell’Antimicrobico-Resistenza (PNCAR) 2017-2020 ha individuato come obiettivo “il rafforzamento della sorveglianza dell’Antimicrobico-Resistenza (AMR) come attività stabile e rappresentativa della realtà del nostro paese” (3).
La Regione Marche ha recepito il PNCAR con la Delibera di Giunta n. 518 del 2019, stilando un protocollo per la sorveglianza dei multiresistenti e delle ICA e per l’uso degli antibiotici. A tal proposito, nel medesimo documento, sono riportate le Linee Guida (LG) di terapia antimicrobica empirica per favorire un approccio prescrittivo standardizzato (3,4).
L’Azienda Sanitaria Unica Regionale (ASUR) è composta da 5 Presidi Unici Ospedalieri e tale complessità ha presupposto una strategia di controllo a più livelli. È stato, quindi, istituito un Comitato Centrale con compiti di pianificazione e coordinamento e 5 Comitati, uno per Area Vasta (AV), con responsabilità di attuazione della sorveglianza.
Nell’ambito dell’AV n. 5, è stato condotto uno studio di prevalenza periodico a carattere descrittivo, con l’obiettivo di rilevare l’andamento degli indicatori definiti nel protocollo regionale. Per tale ragione, non è stata eseguita un’analisi statistica.
L’indagine ha riguardato il trimestre gennaio-marzo 2020 nel reparto di Medicina Interna dell’Ospedale Mazzoni di Ascoli Piceno, scelto in virtù della proporzione elevata della popolazione in termini di dimissioni e di giornate di degenza.
Sono state identificate le caratteristiche epidemiologiche delle ICA, le procedure invasive impiegate, la tempestività del laboratorio analisi nel fornire risposte agli esami colturali richiesti e i microrganismi responsabili (alert e non). Sono stati, inoltre, monitorati i consumi di antibiotici in terapia empirica nei pazienti con ICA ed è stata misurata l’aderenza rispetto alle LG regionali. Da ultimo, sono stati analizzati gli esiti clinici dei pazienti in esame.
Metodi
Per l’indagine sono state impiegate le cartelle cliniche informatizzate del sistema Network Sanitario; la raccolta dati è avvenuta in forma anonima, elaborando i dati con Microsoft Excel.
Sono stati monitorati tutti i pazienti degenti in Medicina Interna da gennaio a marzo 2020 e non dimessi al momento della rilevazione; sono stati inclusi nello studio solo coloro nei quali è insorta un’infezione dopo almeno 48 ore di permanenza in ospedale. A tal proposito, sono state analizzate le terapie antibiotiche empiriche impiegate per trattare le infezioni correlate all’assistenza.
Le ICA sono state classificate sulla base del sito e dell’apparato di interesse; sono state descritte la tipologia di pazienti (sesso; età) e la prevalenza delle infezioni rispetto al trimestre in esame. I microrganismi rilevati (multiresistenti e non) sono stati distinti per i siti/apparati di infezione.
È stata, poi, valutata la qualità del laboratorio analisi in relazione alla capacità nel fornire referti tempestivi in seguito alla ricezione del campione (inferiore/uguale o superiore a 48/72 ore dal prelievo).
Negli ultimi anni, infatti, l’evoluzione epidemiologica dei MDRO ha richiesto investimenti sulla diagnostica microbiologica rapida per perfezionare la terapia empirica con scelte mirate sul microrganismo e sulle sue caratteristiche di antibiotico-sensibilità.
A oggi, in Italia, le tempistiche per la refertazione dei campioni microbiologici sono variabili, in quanto le risorse, in termini di strumentazione e tecnologia, sono distribuite in modo disomogeneo in ambito nazionale, regionale e locale.
Di seguito, sono stati descritti le tipologie, il numero e la frequenza d’uso di device invasivi. I dati ottenuti sono stati correlati alle ICA poiché molte di queste sono associate al loro impiego.
Per le analisi di farmaco-utilizzazione, sono stati considerati i consumi di antibiotici in terapia empirica nei pazienti con infezioni correlate all’assistenza. Per gli antimicrobici sono stati utilizzati il codice della classificazione anatomica terapeutica chimica (ATC) e la dose definita giornaliera (DDD) (5). Nella rilevazione sono stati compresi tutti gli antibiotici ATC J01. L’appropriatezza prescrittiva è stata misurata in termini di prevalenza d’uso e di DDD/100 giornate di degenza (DDD/100 bd); sono stati, inoltre, misurati il numero di schemi di terapia antibiotica empirica e la media del numero di molecole prescritte per paziente. I dati di consumo degli antimicrobici sono stati correlati al sito di infezione per i quali sono stati impiegati. È stata, poi, determinata la spesa associata alle principali classi antimicrobiche e alle singole molecole. Altri indicatori di appropriatezza sono stati la durata media della terapia antibiotica e la frequenza della de-escalation therapy.
È stata, infine, determinata l’aderenza dei trattamenti antibiotici rispetto alle LG regionali. Il valore è stato misurato come percentuale tra il numero di trattamenti che hanno seguito accuratamente il protocollo regionale rispetto al numero totale di trattamenti.
Gli esiti clinici dei pazienti con ICA sono stati valutati in termini di durata media della degenza, dimissioni e decessi nell’arco dei 30 giorni dalla dimissione.
Risultati
Epidemiologia delle Infezioni Correlate all’Assistenza
Dall’analisi delle cartelle cliniche informatizzate è stato rilevato che, su 344 pazienti (57% femmine e 43% maschi), 50 hanno acquisito un’infezione ospedaliera per una prevalenza pari al 15,53%. Il numero di ICA è stato complessivamente pari a 64, con un rapporto infezioni/paziente pari a 1,28.
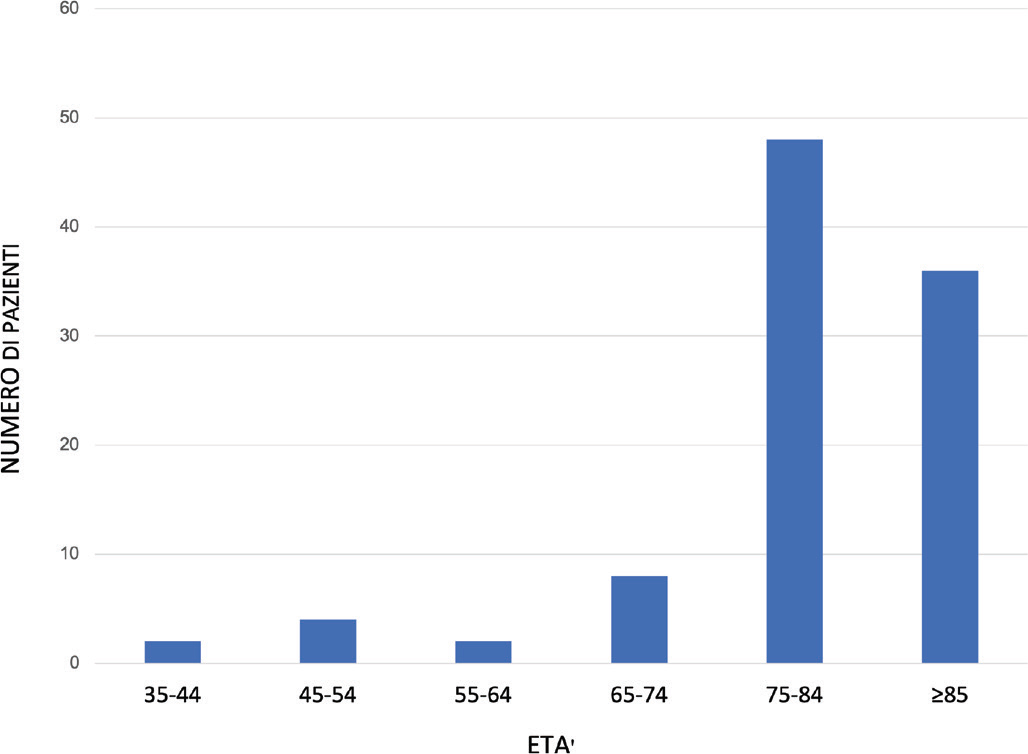
Dalla distribuzione per età riportata nella Figura 1, risulta che la maggioranza dei pazienti appartiene alla fascia di età over 65 (46 pazienti, 92%), con un’età media pari a 81 anni. Di questi, il 64% di sesso femminile e il 36% di sesso maschile.
Le infezioni più frequenti sono state le batteriemie/sepsi (46,88%), le infezioni delle vie urinarie (29,69%) e le infezioni delle basse vie respiratorie (10,94%). Le infezioni delle ferite e altre ICA sono state registrate nel 4,69% e nel 7,81% dei casi, rispettivamente (Tab. I).
| Sito di infezione | N. ICA | % sul totale | Prevalenza di ICA/100 pazienti |
|---|---|---|---|
| Batteriemie/sepsi | 30 | 46,88 | 8,72 |
| Infezioni delle vie urinarie | 19 | 29,69 | 5,52 |
| Infezioni delle basse vie respiratorie | 7 | 10,94 | 2,03 |
| Altre ICA | 5 | 7,81 | 1,45 |
| Infezioni delle ferite | 3 | 4,69 | 0,87 |
| Totale | 64 | 100,00 | 18,59 |
Tra le infezioni del sangue, quelle correlate al catetere venoso centrale confermate microbiologicamente sono state le più frequenti, rappresentando il 34,38% di tutte le ICA. Le infezioni delle vie urinarie (IVU), con esame colturale positivo, sono state maggiori rispetto a quelle con isolato negativo, 28,13% e 3,13%, rispettivamente. La diagnosi delle IVU negative all’esame colturale è stata condotta su base clinica, valutando i tipici sintomi di infezione urinaria, come la difficoltà e l’urgenza nell’urinare.
Tra le infezioni respiratorie, le polmoniti sono state le più frequenti (4,69%), seguite da altre infezioni delle basse vie respiratorie, esclusa la polmonite (3,13%). Le infezioni delle ferite si sono equamente distribuite tra infezioni profonde, infezioni superficiali e infezioni dei tessuti molli (1,56%). Relativamente ad altre ICA, la colite indotta da Clostridium Difficile è stata la più frequente (4,69%); il tasso di infezioni del tratto gastrointestinale non correlate a questo patogeno e di infezioni intra-addominali è stato dell’1,56%.
Dispositivi medici invasivi
Nel periodo dello studio, tutti i pazienti con ICA sono stati portatori di almeno un dispositivo invasivo.
La proporzione dei pazienti esposti a due device è stata la più elevata (70%); per il 16% dei pazienti è stato utilizzato un unico dispositivo invasivo, per il 14% ne sono stati usati tre.
Il catetere vescicale (CV) è stato il device più utilizzato nei pazienti con ICA (86%); il catetere venoso centrale (CVC) è stato utilizzato con una frequenza più elevata (72%) rispetto al catetere venoso periferico (CVP) (24%). La proporzione dei pazienti intubati è stata pari al 2%; altri device quali protesi, stent e così via sono stati utilizzati nel 16% dei casi.
Valutando la proporzione di impiego di ciascun dispositivo nei pazienti con ICA, il maggiore utilizzo ha interessato il CV, pari al 43%. Il CVC è stato utilizzato nel 36% dei casi; la frequenza di utilizzo del CVP è stata più bassa (12%). L’intubazione ha riguardato solo l’1% dei casi; per l’8% dei casi, sono stati impiegati altri presidi (p. es., protesi, stent, ecc.).
Dall’analisi emerge che, dei 36 pazienti portatori di CVC e dei 12 con CVP, il 69% e il 33% rispettivamente hanno contratto una batteriemia/sepsi; 19 dei pazienti portatori di CV hanno avuto un’infezione delle vie urinarie (44%). L’unico paziente intubato ha avuto un’infezione delle basse vie respiratorie.
Attività del laboratorio analisi
Durante lo studio, sono state analizzate 64 ICA; di queste, il 92,18% era corredato da un esame microbiologico positivo. Gli esami colturali eseguiti complessivamente, con refertazione sia positiva che negativa, sono stati 59; quelli con refertazione entro le 48/72 h dal prelievo sono stati pari al 37,28%.
Microrganismi e sorveglianza degli alert
Durante lo studio sono stati isolati 60 microrganismi. I batteri Gram-negativi sono stati i patogeni isolati con maggiore frequenza (56,67%). I Gram-positivi sono stati rilevati nel 40,00% dei casi; i miceti hanno rappresentato solo il 3,33% dei patogeni (Fig. 2).
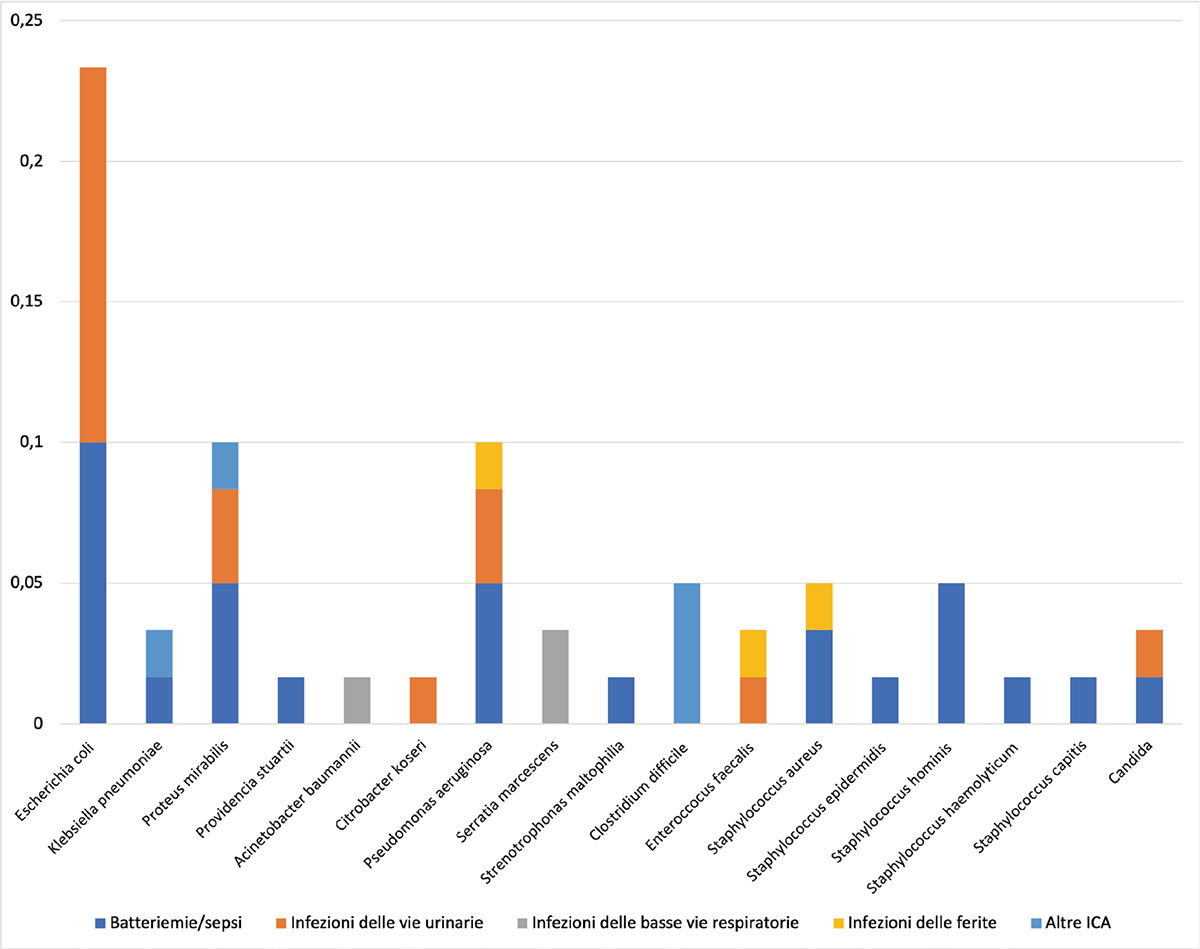
La maggior parte dei pazienti (78%) ha avuto una o più infezioni causate da patogeni alert, definiti tali a causa della loro elevata patogenicità e dell’elevata diffusibilità.
Tali microrganismi hanno rappresentato la maggioranza degli isolati (68,33%), con una frequenza elevata nelle batteriemie/sepsi (38,33%) e nelle IVU (16,67%).
Le ICA per le quali i microrganismi alert sono stati responsabili hanno rappresentato il 61,00% di tutte le ICA in esame. Le batteriemie/sepsi e le infezioni delle vie urinarie sono le patologie dove sono stati più frequentemente isolati, 37,70% e 13,11%, rispettivamente.
Il report conferma l’elevata percentuale di batteri multiresistenti (61,00% di tutte le ICA in esame). Lo sviluppo di resistenza multipla è preoccupante per i batteri Gram-negativi, isolati con maggiore frequenza (60,98% dei microrganismi alert). Escherichia coli ESBL (Extended-Spectrum Beta-Lactamase) e Pseudomonas aeruginosa sono stati i microrganismi più isolati nelle infezioni del sangue e delle vie urinarie.
La frequenza di Gram-positivi (34,15%) ha interessato soprattutto Staphylococcus epidermidis MDR (Multi-Drug Resistant), con isolamenti riguardanti principalmente il torrente ematico e la punta del CVC, a indicare come l’impiego di materiali plastici sia una fonte ideale per la proliferazione della flora cutanea. Sono state rilevate anche infezioni da miceti, con una frequenza del 4,88%, rispetto al totale degli alert (Tab. II).
| Microrganismi Alert | n | % |
|---|---|---|
| Escherichia coli ESBL | 11 | 26,83 |
| Staphylococcus epidermidis MDR | 6 | 14,63 |
| Pseudomonas spp panresistente | 5 | 12,20 |
| Proteus ESBL | 3 | 7,32 |
| Clostridium difficile produttore di tossine | 3 | 7,32 |
| Enteroccocus faecalis vancomicina-resistente | 2 | 4,88 |
| Staphylococcus hominis meticillina-resistente | 2 | 4,88 |
| Klebsiella spp produttore di carbapenemasi | 2 | 4,88 |
| Candida | 2 | 4,88 |
| Acinetobacter spp panresistente | 2 | 4,88 |
| Staphylococcus haemolyticum MDR | 1 | 2,44 |
| Serratia ESBL | 1 | 2,43 |
| Providencia ESBL | 1 | 2,43 |
| Totale | 41 | 100,00 |
I germi per i quali non sono stati rilevati fenomeni di multiresistenza hanno rappresentato il 32% degli isolati; il tasso di Gram-positivi e di Gram-negativi si può considerare equivalente, 47,37% e 52,63%, rispettivamente.
Il batterio più frequente è stato Staphylococcus epidermidis (21,05%), seguito da Escherichia coli, Proteus mirabilis e Staphylococcus aureus (entrambi 5,79%). Altri microrganismi sono stati osservati in percentuale minore (5,26%).
I microrganismi Gram-negativi (52,63%) isolati appartengono alla famiglia delle Enterobacteriaceae (31,58%) e dei Bacilli Gram-negativi (21,05%). Escherichia coli e Proteus mirabilis sono stati i microrganismi maggiormente riscontrati nelle IVU, 15,79% e 10,53%, rispettivamente.
Relativamente alle infezioni da Gram-positivi, sono stati isolati Cocchi Gram-positivi (47,37%). Staphylococcus epidermidis e aureus sono stati i patogeni isolati con maggiore frequenza, 21,05% e 10,53% rispettivamente, principalmente nelle batteriemie/sepsi.
Consumo e spesa degli antibiotici in terapia empirica
Durante lo studio, 48 dei 50 pazienti con un’ICA sono stati trattati con almeno un antibiotico in terapia empirica; la prevalenza d’uso è stata del 96%. Sono stati somministrati in totale 133 cicli di antibiotici, pari a 2,7 trattamenti ogni 100 degenti. Sono stati prescritti tutti per via parenterale.
Per i dati consumo e di spesa sono stati considerati i farmaci equivalenti aggiudicati al prezzo più basso nel bando di gara ASUR e utilizzati in AV n. 5.
Le classi antibiotiche più usate sono state le penicilline (J01C), 35,34%, altri antibiotici β-lattamici (J01D), 32,33%, e “altri antibiotici”, quali glicopeptidi e ossazolidinoni, (J01X), 17,29%. Altri antimicrobici sono stati impiegati con una minore frequenza: chinoloni (J01M), 5,26%, tetracicline (J01A) e macrolidi, lincosamidi e streptogrammine (J01F), 4,51%, aminoglicosidi (J01G), 0,75%.
Le molecole maggiormente usate sono state Piperacillina/Tazobactam (33,83%), Meropenem (23,31%) e Teicoplanina (10,53%) (Tab. III).
Esprimendo il consumo di antimicrobici con il sistema di classificazione ATC/DDD, è emerso che gli antibiotici più utilizzati sono gli antibiotici β-lattamici (60,09 DDD/100 bd); a tal proposito, Piperacillina/Tazobactam è la molecola più impiegata (59,62 DDD/100 bd). Nell’ambito degli altri β-lattamici, il Meropenem è risultato quello maggiormente utilizzato (12,54 DDD/100 bd). Il consumo di “altri antibiotici” (J01X) ha riguardato soprattutto Linezolid (0,91 DDD/100 bd) e Teicoplanina (0,62 DDD/100 bd). Relativamente ai fluorochinoloni, si è osservato un consumo equivalente di Levofloxacina (0,16 DDD/100 bd) e di Ciprofloxacina (0,11 DDD/100 bd). Le tetracicline e gli aminoglicosidi sono stati impiegati con una minore frequenza (0,08 e 0,01 DDD/100 bd, rispettivamente) (Tab. III).
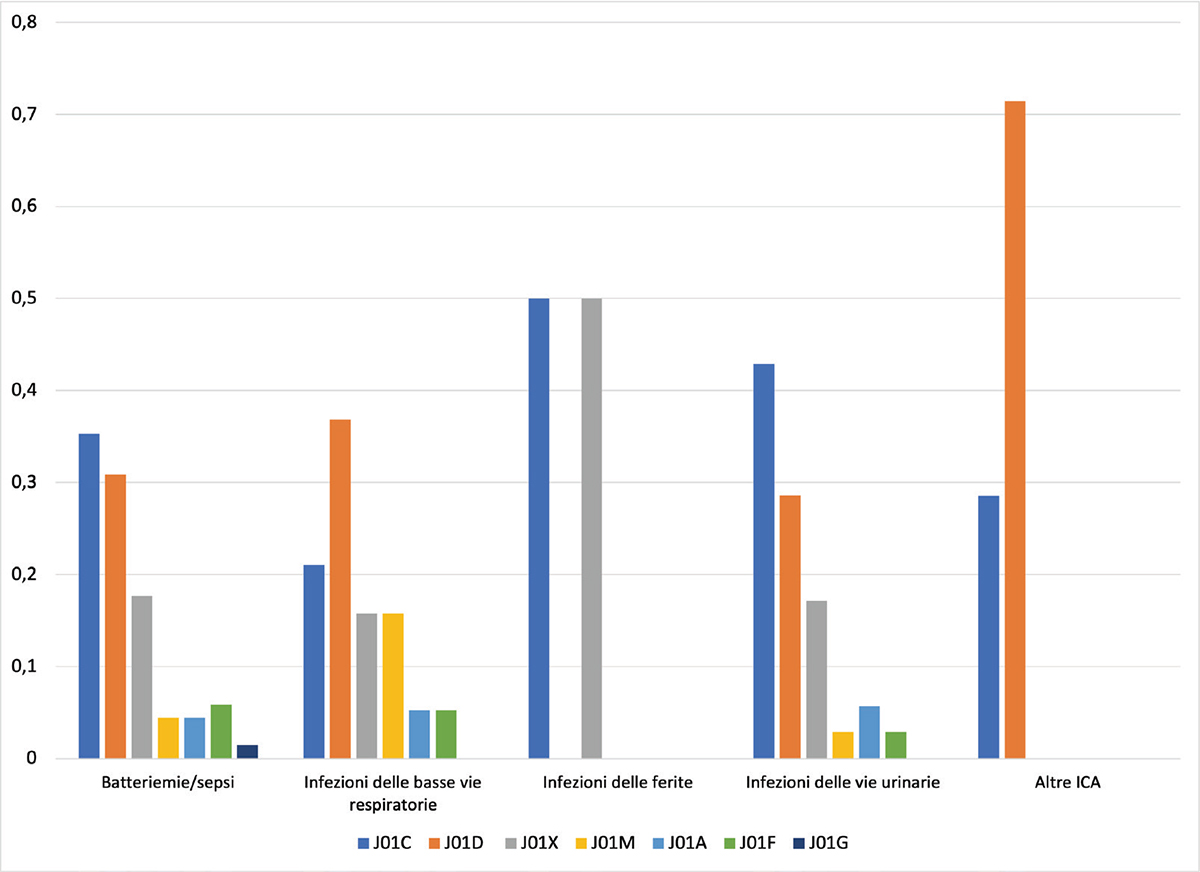
Prendendo in esame i principali siti di infezione (Fig. 3), si osserva che le penicilline (35,29%), altri antibiotici β-lattamici (30,88%) e “altri antibiotici” (J01X) (17,65%) sono le classi più utilizzate per il trattamento delle batteriemie/sepsi. Per le IVU, il trend è simile, 42,86% e 28,57%, rispettivamente. Anche per le infezioni delle basse vie respiratorie, altri antibiotici β-lattamici sono le molecole maggiormente somministrate (36,84%), seguite dalle penicilline (21,05%). Le infezioni delle ferite sono state trattate in egual misura (50%) con le penicilline e con “altri antibiotici” (J01X). Relativamente ad altre ICA, per il 71,43% sono state curate con altri antibiotici β-lattamici e per il 28,57% con penicilline.
| ATCV Livello | Batteriemie/
sepsi |
Infezioni delle basse vie respiratorie | Infezioni delle ferite | Infezioni delle vie urinarie | Altre ICA | Totale | DDD | DDD/
100 bd |
||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| n | % | n | % | n | % | n | % | n | % | n | % | n | n | |
| J01CR05 Piperacillina/Tazobactam | 23 | 17,29 | 4 | 3,01 | 2 | 1,50 | 14 | 10,53 | 2 | 1,50 | 45 | 33,83 | 3052,00 | 59,62 |
| J01DH02 Meropenem | 16 | 12,03 | 5 | 3,76 | 0 | 0,00 | 7 | 5,26 | 3 | 2,26 | 31 | 23,31 | 642,00 | 12,54 |
| J01XA02 Teicoplanina | 9 | 6,77 | 1 | 0,75 | 1 | 0,75 | 3 | 2,26 | 0 | 0,00 | 14 | 10,53 | 31,60 | 0,62 |
| J01DD04 Ceftriaxone | 4 | 3,01 | 2 | 1,50 | 0 | 0,00 | 2 | 1,50 | 2 | 1,50 | 10 | 7,52 | 102,00 | 1,99 |
| J01XX08 Linezolid | 2 | 1,50 | 1 | 0,75 | 1 | 0,75 | 3 | 2,26 | 0 | 0,00 | 7 | 5,26 | 46,80 | 0,91 |
| J01AA12 Tigeciclina | 3 | 2,26 | 1 | 0,75 | 0 | 0,00 | 2 | 1,50 | 0 | 0,00 | 6 | 4,51 | 4,10 | 0,08 |
| J01FA10 Azitromicina | 3 | 2,26 | 1 | 0,75 | 0 | 0,00 | 1 | 0,75 | 0 | 0,00 | 5 | 3,76 | 11,00 | 0,21 |
| J01MA12 Levofloxacina | 2 | 1,50 | 2 | 1,50 | 0 | 0,00 | 1 | 0,75 | 0 | 0,00 | 5 | 3,76 | 8,00 | 0,16 |
| J01CR02 Amoxicillina/Acido Clavulanico | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 1 | 0,75 | 0 | 0,00 | 2 | 1,50 | 24,00 | 0,47 |
| J01MA12 Ciprofloxacina | 1 | 0,75 | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 2 | 1,50 | 5,60 | 0,11 |
| J01DH51 Imipenem | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 1 | 0,75 | 0 | 0,00 | 2 | 1,50 | 6,00 | 0,12 |
| J01XA01 Vancomicina | 1 | 0,75 | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 2 | 1,50 | 12,00 | 0,23 |
| J01FA09 Claritromicina | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 1 | 0,75 | 2,00 | 0,04 |
| J01GB03 Gentamicina | 1 | 0,75 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 0 | 0,00 | 1 | 0,75 | 0,72 | 0,01 |
| Totale | 68 | 51,12 | 19 | 14,27 | 4 | 3 | 35 | 26,31 | 7 | 5,26 | 133 | 100,00 | 3947,82 | 77,11 |
Rispetto alle terapie analizzate, il numero totale di cambiamenti di schemi di terapia antibiotica empirica per paziente è stato pari a 34, vale a dire che, nella maggioranza dei casi in esame (75%), sono state utilizzate almeno due linee di terapia empirica. Sono stati prescritti mediamente tre antibiotici per paziente.
La durata media delle terapie empiriche antimicrobiche è stata di circa 13 giorni; tale continuità è stata determinata, in alcuni casi, dai lunghi tempi di refertazione microbiologica, in altri casi non si è passati da una terapia empirica a una terapia antibiotica mirata. A tal proposito, è monitorata la de-escalation therapy; dallo studio emerge che solo nel 13% dei pazienti è avvenuto il passaggio da una terapia antibiotica empirica a largo spettro a una a spettro più ristretto, sulla base dei risultati microbiologici, o c’è stata una riduzione del numero degli antibiotici.
È stata, infine, misurata l’aderenza delle terapie antibiotiche empiriche per il trattamento delle ICA rispetto alle LG ASUR; è stata corrispondente al 34% rispetto al totale delle terapie empiriche analizzate.
Gli scostamenti più comuni hanno riguardato i carbapenemici (49%), nonostante il protocollo ne raccomandasse una limitazione d’uso in quanto ultima risorsa per i Gram-negativi ESBL.
Altre non conformità hanno riguardato l’utilizzo di cosiddette molecole “di nicchia”, quali Teicoplanina (14%) e Linezolid (9%), che andrebbero usate preferibilmente in pazienti con un’infezione documentata microbiologicamente, e l’impiego di un antibiotico lipofilo, quale la Tigeciclina (20%), per le IVU.
Come misura indiretta dei consumi di antibiotici è stata, poi, misurata la spesa, pari a € 7.732,24. Per il 37,99% è stata determinata dall’impiego di antibiotici β-lattamici. Piperacillina/Tazobactam è stata la molecola che ha inciso maggiormente (€ 2.907,66). Il consumo di “altri antibiotici” (J01X) è stato altrettanto elevato (€ 2.098,28) e relativo all’impego di Teicoplanina (€ 1.848,61) e Linezolid (€ 237,67). Nell’ambito degli altri β-lattamici, il Meropenem è risultato quello con un maggiore impatto sulla spesa (€ 1.528,11). Le tetracicline hanno a loro volta inciso sui consumi (€ 858,00). Per la classe J01F sono stati spesi € 120,54. Le classi J01M e J01G hanno rappresentato solo lo 0,29% e lo 0,12% della spesa totale, rispettivamente.
Esiti clinici
Analizzando i pazienti con ICA rispetto a tutti i degenti nel medesimo periodo, è emerso che le persone assistite con più di 65 anni potrebbero essere più soggette a contrarre infezioni ospedaliere (età media dei pazienti con ICA, 81 anni; altri assistiti, 59 anni).
Confrontando le due popolazioni, il sesso femminile sembrerebbe essere il più rappresentativo per entrambe (64%, assistiti con ICA; 57%, altri assistiti).
I pazienti con un’infezione correlata all’assistenza hanno rappresentato il 27,88% delle giornate di degenza del periodo di riferimento e il 14,53% delle dimissioni totali.
Sono stati, quindi, valutati gli esiti in questo gruppo di assistiti.
Nonostante le dimissioni abbiano rappresentato la maggioranza (74%), il 26% dei degenti è deceduto nell’arco dei 30 giorni dalla data di dimissione ospedaliera. La durata media dei giorni di degenza nel periodo dello studio è stata pari a 28,54 giorni. Confrontando la frequenza di questi due indicatori con l’intera popolazione del trimestre in esame (decessi:18,90%; durata media della degenza:14,88 giorni), si può concludere che le ICA e le AMR potrebbero essere delle complicanze che aumentano il tempo di convalescenza e la mortalità.
Bisogna, tuttavia, tenere conto del fatto che, nel presente studio, non sono stati considerati fattori di rischio intrinseci per l’insorgenza delle ICA, quali deficit immunitari, malnutrizione e gravi patologie concomitanti. Inoltre, per quanto riguarda l’analisi di farmaco-utilizzazione, la DDD utilizzata come indicatore per il consumo degli antibiotici è un paramento teorico di dose giornaliera che non rappresenta la dose effettivamente prescritta in terapia (PDD, Prescribed Daily Dose).
Sarebbe, dunque, interessante valutare in un prossimo lavoro come questi paramenti aggiuntivi potrebbero influenzare l’interpretazione dei risultati.
Conclusioni
Per concludere, le ICA hanno un costo, sia in termini di salute che economici.
L’istituzione di protocolli per il controllo delle infezioni e il corretto uso degli antibiotici sono sicuramente degli strumenti utili, ma, comunque, non sufficienti per il raggiungimento degli obiettivi.
Occorrono azioni concrete attraverso l’istituzione di un team di Antimicrobial Stewardship che sia impegnato quotidianamente nell’applicazione di strategie condivise.
Sarebbe determinante la realizzazione di un network aziendale che preveda interventi coordinati tra il clinico prescrittore, l’infettivologo, il microbiologo, il farmacista ospedaliero e l’infermiere.
A tal proposito, il medico dovrebbe essere supportato nella scelta dell’antimicrobico più idoneo, accedendo in tempo reale alle LG. Ai fini della sorveglianza dei MDRO, sarebbe utile inserire un segnale grafico accanto al nominativo del paziente sulla cartella elettronica, in caso di positività laboratoristica, sia per ottimizzare la gestione del paziente che per ridurre il rischio di potenziali trasmissioni.
L’informatizzazione assicurerebbe, quindi, una maggiore sicurezza per i pazienti, in quanto verrebbe garantita la tracciabilità di tutto il percorso, migliorando la performance della terapia, prevenendo eventuali rischi e razionalizzando le risorse economiche.
Per concludere, l’impegno dedicato a questo studio vuole rappresentare un momento di riflessione e di sensibilizzazione per mettere in atto dei cambiamenti.
In un periodo di estrema emergenza sanitaria, dove l’infezione da sindrome respiratoria grave Coronavirus-2 (SARS-CoV-2) ha reso vulnerabili anche i Paesi più solidi, è urgente la necessità di contrastare le resistenze antimicrobiche e di preservare i pazienti da possibili infezioni.
La pandemia deve rappresentare, quindi, un’opportunità di miglioramento, iniziando da un approccio di cura multidisciplinare.
Disclosures
Conflict of interest: The authors declare no conflict of interest.
Financial support: This research received no specific grant from any funding agency in the public, commercial, or not-for-profit sectors.
Authors contribution: All authors contributed equally to this manuscript.
Bibliografia
- 1. Iacchini S, Sabbatucci M, Gagliotti C, et al. Bloodstream infections due to carbapenemase-producing Enterobacteriaceae in Italy: results from nationwide surveillance, 2014 to 2017. Euro Surveill. 2019;24(5):pii=1800159. CrossRef PubMed
- 2. Report on the burden of endemic health care-associated infection worldwide. World Health Organization, 2011. Online. (Accessed June 2021)
- 3. Piano Nazionale di Contrasto dell’Antimicrobico-Resistenza, PNCAR, 2017-2020. Online. (Accessed June 2021)
- 4. ASUR DG 518/19: “Controllo delle Infezioni Correlate all’Assistenza ed appropriato uso degli antibiotici: linee di indirizzo ASUR Marche”: Online. (Accessed June 2021)
- 5. WHO Collaborating Centre for Drug Statistics Methodology. Guidelines for ATC classification and DDD assignment; Oslo, 2021. Online (Accessed November 2021)