 |
AboutOpen | 2020; 7(1): 95-102
ORIGINAL RESEARCH ARTICLE |
 |
Modello di stima dei costi sanitari e della capacity delle terapie intensive in Italia nel trattamento di pazienti affetti da COVID-19: valutazione dell’impatto di remdesivir
Model for estimating healthcare costs and capacity of intensive care units in the treatment of Italian patients with COVID-19, and relative evaluation of a new therapeutic strategy
Introduction: Coronavirus disease 2019 (COVID-19) is caused by a severe acute respiratory syndrome coronavirus 2, which is a human coronavirus responsible for a pandemic. Direct interventions, i.e. physical distancing and use of protective devices, can prevent or limit contagions, however, it is also required to evaluate the optimization of limited resources, such as the Intensive Care Unit (ICU). For this purpose, it is relevant to estimate the impact of therapeutic solutions that reduce the probability that the patient transits to ICU in symptomatic subjects and in need of hospitalization. The therapeutic solutions allow a more rapid recovery of the patient and save scarce resources that can be used in the treatment of other patients.
Methods: A forecasting model is designed to estimate the impact of one therapeutic solution, i.e. the antiretroviral Remdesivir, on both the capacity of intensive care and the healthcare costs for hospitals when managing the current emergency. A base case is presented as well as a best and a worst case scenario deriving from the sensitivity analyses.
Results: The introduction of Remdesivir in patients receiving low-flow oxygen therapy with the purpose of reducing ICU accesses and deaths leads to 431 million euros cost savings and avoids 17,150 hospitalizations in intensive care and 6,923 deaths. In the best case, 294 million euros savings are estimated, whilst in the worst case the model estimates a saving of 512 million euros.
Conclusions: Remdesivir has the potential to reduce the negative effects of the Coronavirus disease, improving patient conditions and reducing death tolls, and can also save scarce healthcare resources during this pandemic, resulting in a shorter hospital stay and fewer ICU admissions.
Keywords: COVID-19, Intensive Care Units, Remdesivir
Received: November 24, 2020
Accepted: December 4, 2020
Published online: December 17, 2020
© 2020 The Authors. This article is published by AboutScience and licensed under Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0). Any commercial use is not permitted and is subject to Publisher’s permissions. Full information is available at www.aboutscience.eu
Introduzione
La malattia da coronavirus 2019 (COVID-19) è causata dal coronavirus 2 da sindrome respiratoria acuta grave (SARS-CoV-2), un coronavirus umano che si è diffuso rapidamente in tutto il mondo, portando l’Organizzazione Mondiale della Sanità a dichiarare una pandemia.
Dall’inizio dell’epidemia di COVID-19 in Europa, l’Italia è stata tra i primi paesi colpiti e il numero di casi segnalati è ancora fra i più alti del continente. Nei primi mesi del 2020 l’Italia si è trovata a essere il paese più colpito sia in termini di contagi, che di decessi e di ricoveri. A oggi sono stati identificati oltre 1.600.000 casi dall’inizio della pandemia e, purtroppo, oltre 55.000 decessi (dato aggiornato al 2 dicembre) (1).
Prescindendo dall’inevitabile riflesso che la pandemia ha avuto e sta avendo sulla salute dei cittadini, in particolare gli anziani e i fragili e dall’importante impatto economico, con una contrazione del prodotto interno lordo (PIL) che si stima, a fine anno, intorno al 14,8% (2), l’epidemia ha avuto una ricaduta notevole nel settore acuto del sistema sanitario nazionale (SSN), soprattutto per i reparti di emergenza e per le unità di terapia intensiva (ICU), che hanno sperimentato una pressione crescente.
Le ICU, dedicate a trattare i pazienti più gravi con bisogno di ventilazione automatica, sono, da una parte, tradizionalmente annoverate fra i servizi più complessi e con un numero molto limitato sul territorio italiano e, dall’altra, estremamente costose. Il costo giornaliero di un paziente in ICU si attesta su una media di circa € 1600 (3) ed è molto sensibile ai trattamenti che vengono somministrati.
Per quanto riguarda il burden economico della malattia, tenendo in considerazione in maniera del tutto conservativa soltanto le prestazioni ospedaliere, nel periodo dall’1 marzo al 21 luglio 2020, il costo per il SSN è stato quantificato, a tariffe DRG, in circa 657 milioni di euro e il costo delle giornate di degenza in ICU in oltre 265 milioni di euro (4).
Appare chiaro che, oltre a una serie di interventi a monte e volti essenzialmente a prevenire o, almeno, a limitare i contagi (distanziamento fisico, utilizzo dei dispositivi di protezione), è necessario ragionare in termini di ottimizzazione dell’utilizzo di risorse così limitate come le ICU, soprattutto a causa di una recrudescenza della pandemia che, nel confermare le previsioni che già erano state fatte, sta colpendo il nostro territorio con particolare vigore. Come confermato dall’Agenzia Nazionale per i Servizi Sanitari Regionali (AGENAS), si stimano, al 13 novembre 2020, 3230 ricoverati in ICU, su un totale di 8423 posti letto (38,3% dei posti letto totali, considerando un sovraccarico per le terapie intensive superata la soglia del 30%, come individuato dal decreto del Ministro della Salute del 30/4/2020) (5).
In questo senso, assume particolare importanza stimare l’impatto di eventuali soluzioni terapeutiche che, nei soggetti sintomatici e con bisogno di essere ospedalizzati, riducano la probabilità che il paziente transiti in ICU, da un lato consentendo un più rapido recupero del paziente e, dall’altro, risparmiando risorse scarse che potrebbero essere impiegate per trattare altri pazienti, non necessariamente affetti da COVID-19.
Remdesivir, primo medicinale approvato in Usa per il trattamento dei pazienti affetti da COVID-19 e, da luglio, 2020 anche nell’Unione Europea per i pazienti adulti e adolescenti (di età pari o superiore ai 12 anni e con un peso pari ad almeno 40 kg) con polmonite che richiede ossigenoterapia supplementare, è oggi disponibile in Italia nell’ambito di un accordo europeo congiunto (Joint Procurement Agreement, JPA) con modalità di accesso al farmaco tramite registro dell’Agenzia Italiana del Farmaco (AIFA) (6). Il registro consente l’accesso al medicinale solo ai pazienti con condizione clinica corrispondente all’indicazione autorizzata dall’Agenzia Europea per i Medicinali (EMA) e conformi ai criteri definiti dalla Commissione Tecnico-Scientifica (CTS) dell’AIFA, per un ciclo di trattamento pari a 5 giorni (7). Tali criteri sono:
- diagnosi di polmonite documentata radiologicamente;
- esordio dei sintomi da meno di 10 giorni;
- in ossigenoterapia;
- non in ventilazione meccanica non invasiva, ossigenoterapia ad alto flusso, ventilazione meccanica invasiva o ECMO;
- funzionalità renale: stima della velocità di filtrazione glomerulare (eGFR), da 30 mL/min a 90 mL/min compreso;
- funzionalità epatica: alanina aminotransferasi (ALT), normale o inferiore 5 volte al limite superiore della norma al basale.
Dati clinici da un trial indipendente randomizzato, controllato in doppio cieco verso placebo su oltre 1000 pazienti ospedalizzati per COVID-19 hanno dimostrato che remdesivir migliora significativamente il tempo di recupero del paziente di 5 giorni (di 7 nei pazienti in ossigenoterapia al basale) e riduce la durata dell’ospedalizzazione di una mediana di 5 giorni (8). Dallo stesso studio clinico è emerso che la terapia con remdesivir riduce la progressione della malattia, misurata come minore incidenza di nuova ventilazione meccanica o di ossigenazione extracorporea a membrana (ECMO) (rispetto al placebo, il 43% in meno di pazienti veniva avviato alla ventilazione meccanica); questo passaggio coincide tipicamente con il ricovero del paziente in un’unità di terapia intensiva ed è quindi di particolare importanza dal punto di vista dell’organizzazione delle strutture ospedaliere. Nella popolazione in ossigenoterapia a basso flusso al basale, remdesivir è, inoltre, in grado di ridurre il rischio di mortalità del 70% rispetto a placebo (8). È, quindi, evidente che la terapia con remdesivir può generare un valore significativo per i pazienti, un risparmio per il SSN e, più in generale, un beneficio per la società nel suo complesso. I benefici clinici di remdesivir, infatti, si traducono in una riduzione del tempo di permanenza del paziente in ospedale e possono tradursi anche in una minore necessità di ricorso alla terapia intensiva.
In questa ottica, è stato costruito un modello previsionale volto a stimare l’impatto di una soluzione terapeutica come remdesivir sulla capacity delle ICU e, in ultima istanza, sui costi sanitari diretti per gli ospedali nella gestione dell’attuale emergenza.
Metodi
Struttura del modello
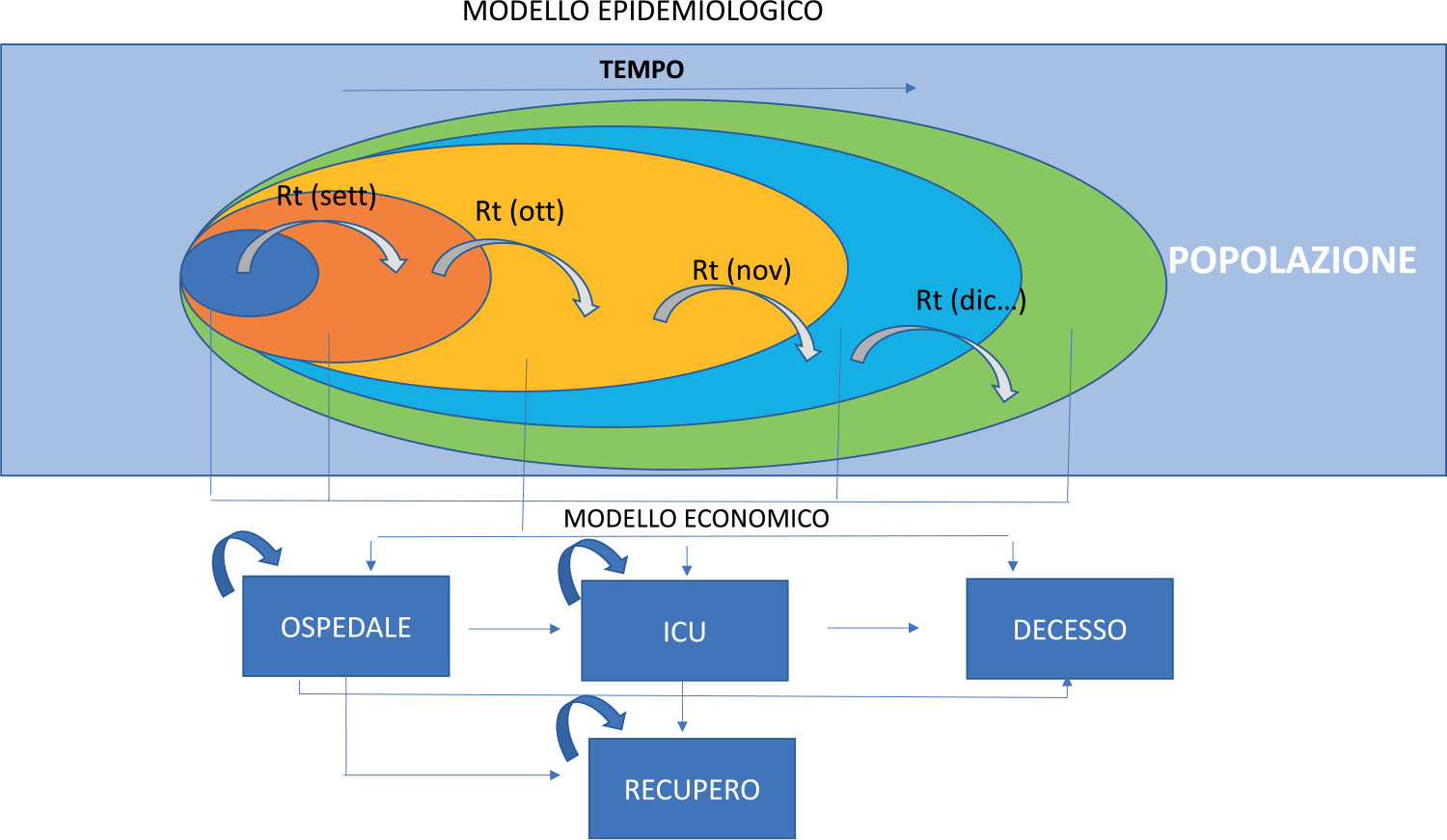
Il modello è strutturato in due fasi (Fig. 1), i cui obiettivi sono:
- stimare il numero di contagiati totali sulla base della popolazione italiana;
- stimare i costi sanitari diretti associati al trattamento dei pazienti ospedalizzati e in terapia intensiva sia in assenza di ricorso alla terapia con remdesivir sia laddove venga, invece, impiegato remdesivir nei pazienti in ossigenoterapia a basso flusso.
Nella prima fase di stima, a partire dai dati epidemiologici osservati e relativi alla contagiosità (l’indice Rt) e ai dati aggiornati con cadenza quotidiana rispetto agli ospedalizzati, ai ricoverati in terapia intensiva e ai decessi, è stata simulata, su un orizzonte temporale di 20 settimane, l’evoluzione della pandemia in termini di contagiati, accessi in terapia intensiva e decessi. In considerazione della peculiarità epidemiologica e clinica dell’infezione da coronavirus e dell’incertezza nel poter formulare ipotesi sulla sua evoluzione in termini di contagi e di virulenza nel medio-lungo periodo, si è deciso di limitare l’orizzonte temporale a un’unica ondata pandemica.
La simulazione che porta alla prima fase di stima ha ipotizzato un’evoluzione della contagiosità basata sulle variazioni negli Rt osservati di settimana in settimana nel mese di ottobre. Le diminuzioni di Rt conseguenti a ulteriori provvedimenti restrittivi hanno fatto riferimento al decreto del Presidente del Consiglio dei Ministri (DPCM) emanato in data 25 ottobre 2020. Si è ipotizzato che gli effetti di tali provvedimenti sulla contagiosità fossero osservabili a partire dalla terza settimana (ossia settimana 5 del modello) e che avessero un impatto quantificabile in una riduzione dell’indice Rt, secondo l’andamento descritto nella Tabella I. Ulteriori scenari sono stati simulati successivamente (vedi analisi di scenario qui di seguito).
Questa simulazione è servita ad alimentare la seconda fase di stima costituita da un modello markoviano a coorte aperta che consentisse di ricostruire il percorso del paziente ospedalizzato, considerando, quindi, sia la probabilità di accesso direttamente in terapia intensiva che l’ospedalizzazione e la probabilità di successiva evoluzione in termini di decesso o aumento dell’intensità delle cure necessarie (Fig. 1).
Coerentemente con il modello epidemiologico strutturato nella prima fase di stima, il modello markoviano è costituito da 20 cicli, ciascuno della durata di una settimana.
Ciò ha consentito di stimare i costi ospedalieri valorizzando il numero di giornate di degenza caratterizzato a seconda del livello di intensità di cura.
Stando ai dati attualmente disponibili e pubblicati con cadenza quotidiana, la frequenza dei pazienti ospedalizzati è pari al 6,6% mentre quella dei ricoverati in terapia intensiva è pari allo 0,6% sul totale degli infetti, mentre la letalità si attesta all’interno di un range compreso fra lo 0,6% e il 2,4% (9,10) (Tab. I).
Dati di efficacia
Per valutare lo scenario con l’adozione di remdesivir è stato considerato il trial randomizzato controllato e in doppio cieco condotto da Beigel et al. (8), che hanno constatato che l’adozione di remdesivir nei pazienti in ossigenoterapia a basso flusso, vale a dire nei pazienti candidabili al trattamento con remdesivir in Italia, riduce il time-to-recovery dei pazienti ospedalizzati (hazard ratio: 1,45; 95% CI, 1,18-1,79) e la mortalità (hazard ratio: 0,3; 95% CI, 0,14-0,64). La riduzione della probabilità di accesso in terapia intensiva a seguito del trattamento è stata estrapolata calcolando la Relative Risk Reduction (RRR) risultante dai dati dello studio clinico che riportano una frequenza di nuova ventilazione meccanica o ECMO più bassa nel gruppo trattato con (13%) vs placebo (23%) (Tab. II).
Si è ipotizzato che una percentuale tra il 50% e il 60% fra tutti gli ospedalizzati per COVID-19 abbia bisogno di ossigenoterapia a basso flusso e sia, quindi, eleggibile al trattamento con remdesivir. L’utilizzo della strategia terapeutica non è stato ipotizzato in pazienti ospedalizzati in terapia intensiva, coerentemente con l’eleggibilità dei pazienti alla terapia secondo i criteri AIFA.
La Tabella I riporta nel dettaglio i dati clinici utilizzati insieme ai valori degli Rt utilizzati per ogni settimana.
Dati economici
Dal momento che la prospettiva di analisi considerata è quella dell’ospedale, il modello considera, quale driver principale della stima dei costi, la durata della degenza. Di conseguenza, sulla base del time to recovery indicato nello studio clinico, è stata stimata la riduzione della degenza ospedaliera a seguito del trattamento con remdesivir, rispetto a una media di 19 giorni di ospedalizzazione, come indicato dai dati del Ministero della Salute.
I dati relativi alla durata delle degenze e dei ricoveri in terapia intensiva, sia per i pazienti guariti che nei pazienti deceduti, sono stati ricavati dallo studio di Grasselli et al. (11) e dagli “Instant report” di analisi dei modelli organizzativi di risposta al COVID-19, pubblicati sul sito di Altems dell’Università Cattolica di Roma (4).
Per quanto riguarda la valorizzazione delle giornate di degenza è stata utilizzata la stima della Ragioneria Generale dello Stato, che riporta un valore medio per giornata di degenza pari a € 674 (12). Per la valorizzazione delle terapie intensive sono stati utilizzati dati ricavati dal progetto Mattoni del Ministero della Salute, che stima una tariffa minima per giornata di degenza in terapia intensiva pari a € 1.654 (13).
Per quanto riguarda la valorizzazione dell’alternativa terapeutica di riferimento, è stato considerato il prezzo, identico in tutti i paesi industrializzati e pari a 390 dollari a fiala. Coerentemente con i criteri AIFA, è stata ipotizzata una durata della terapia di 5 giorni (6 fiale).
| Parametri | Valore | Fonte |
|---|---|---|
| Letalità popolazione italiana | 0,6%-2,4% | Bassi et al. (9) |
| Hazard ratio time-to-recovery nei pazienti in ossigenoterapia a basso flusso | 1,45 | Beigel et al. (8) |
| Riduzione relativa del rischio a progressione a terapia intensiva con remdesivir | 36% | Beigel et al. (8) |
| Hazard Ratio mortalità nei pazienti in ossigenoterapia a basso flusso | 0,3 | Beigel et al. (8) |
| Rt sett 1
Rt sett 2 Rt sett 3 Rt sett 4 Rt sett 5 Rt sett 6 Rt sett 7 Rt sett 8 Rt sett 9 Rt sett 10 Rt sett 11 Rt sett 12 Rt sett 13 Rt sett 14 Rt sett 15 Rt sett 16 Rt sett 17 Rt sett 18-20 |
1,1
1,3 1,7 1,7 1,5 1,3 1,2 1,1 1,1 1 0,8 0,8 0,8 0,8 0,8 0,8 0,8 0,75 |
ISS (dato medio nazionale 5-11 ottobre 2020)
ISS (dato medio nazionale 12-18 ottobre 2020) ISS (dato medio nazionale 19-26 ottobre 2020) ISS (dato medio nazionale 19-26 ottobre 2020 ) Ipotesi su dati ISS |
| Parametro | Valore | Fonte |
|---|---|---|
| Costo giornata degenza | 674,00 € | Rag. Gen. Stato (12) |
| Durata ospedalizzazione | 19 g | Estrapolato da Grasselli et al. (11) |
| Costo giornata ICU | 1.654,00 € | ALTEMS (13) |
| Durata ricovero in ICU | 9 g | Grasselli et al. (11) |
| Durata degenza (deceduti) | 8 g | Grasselli et al. (11) |
| Durata ospedalizzazione (pazienti RDV) | 14 g | Ipotesi da Beigel et al.* (8) |
| Costo giornata degenza (pazienti RDV) | 807,00 € | Ipotesi** |
| Durata terapia con RDV | 5 g | Beigel et al. (8) |
ICU: unità di terapia intensiva; RDV: remdesivir.
*I risultati di Beigel et al. stimano una riduzione del tempo di recupero pari a 5 giorni (p < 0,001). È stata, quindi, ipotizzata una riduzione della durata di degenza pari agli stessi giorni, a partire dal valore medio italiano pari a 19 giorni. Nell’analisi di sensibilità si è considerata anche l’ipotesi che la riduzione del tempo di recupero non avesse un impatto sulla durata della degenza totale. **Il costo di una giornata di degenza in pazienti trattati con remdesivir è stato calcolato moltiplicando il prezzo a fiala del farmaco per il numero di fiale (6). Il risultato è stato distribuito sulla durata di degenza ipotizzata (15,58 giorni) e sommato al costo per giornata di degenza senza remdesivir (pari a 674 €).
Analisi di sensibilità
Al fine di testare la sensibilità del modello alle variazioni dei parametri inclusi sono state condotte delle analisi di sensibilità probabilistiche su tutti i parametri inclusi sia nella prima fase che nella seconda fase di stima previste dal modello.
I valori degli Rt sono stati fatti variare applicando ai valori previsti la stessa variazione osservata dagli intervalli di confidenza degli Rt dei mesi precedenti. A tali valori sono state applicate delle distribuzioni casuali di tipo beta.
I valori relativi alla riduzione della probabilità di accesso in terapia intensiva e alla riduzione della mortalità sono stati fatti variare coerentemente con una distribuzione beta, ipotizzando una deviazione standard coerente con i dati clinici pubblicati (8). È da notare che la scelta in merito all’utilizzo di tale dato è stata dettata dalla disponibilità limitata di altre informazioni che consentissero di adottare un approccio di tipo probabilistico nell’analisi di sensibilità.
I valori relativi al numero di giornate di degenza in regime ordinario e in terapia intensiva, così come il time to recovery conseguente al trattamento, sono stati fatti variare coerentemente con una distribuzione di tipo gamma, ipotizzando una deviazione standard pari al 20% del valore basale.
Analisi di scenario
Sono stati, inoltre, ipotizzati due scenari alternativi a quello basale, dipendenti dall’evoluzione della curva epidemiologica. Più in dettaglio, sono stati simulati diversi tassi di riduzione degli Rt a seguito di misure più o meno restrittive.
Il primo scenario alternativo, definito “ottimistico”, ha ipotizzato una riduzione degli Rt pari a 0,2 punti a settimana a partire dalla quarta settimana, per, poi, attestarsi a 0,9 dall’ottava settimana in poi.
Il secondo scenario alternativo, definito “pessimistico”, ha, invece, ipotizzato che il valore degli Rt rimanesse a 1,1 fino alla settimana 12 e che, successivamente, scendesse a 1 dalla settimana 12 alla settimana 20.
Risultati
La Tabella III riporta i risultati della prima fase di stima. Su un orizzonte temporale di 20 settimane, sono stimati, a fronte di circa 2.750.000 contagiati, oltre 57.000 accessi in terapia intensiva e 16.586 decessi. L’adozione di remdesivir nei pazienti che necessitano di ossigenoterapia a basso flusso sarebbe in grado di ridurre gli accessi in terapia intensiva di oltre 17.000 unità e di evitare quasi 7000 decessi.
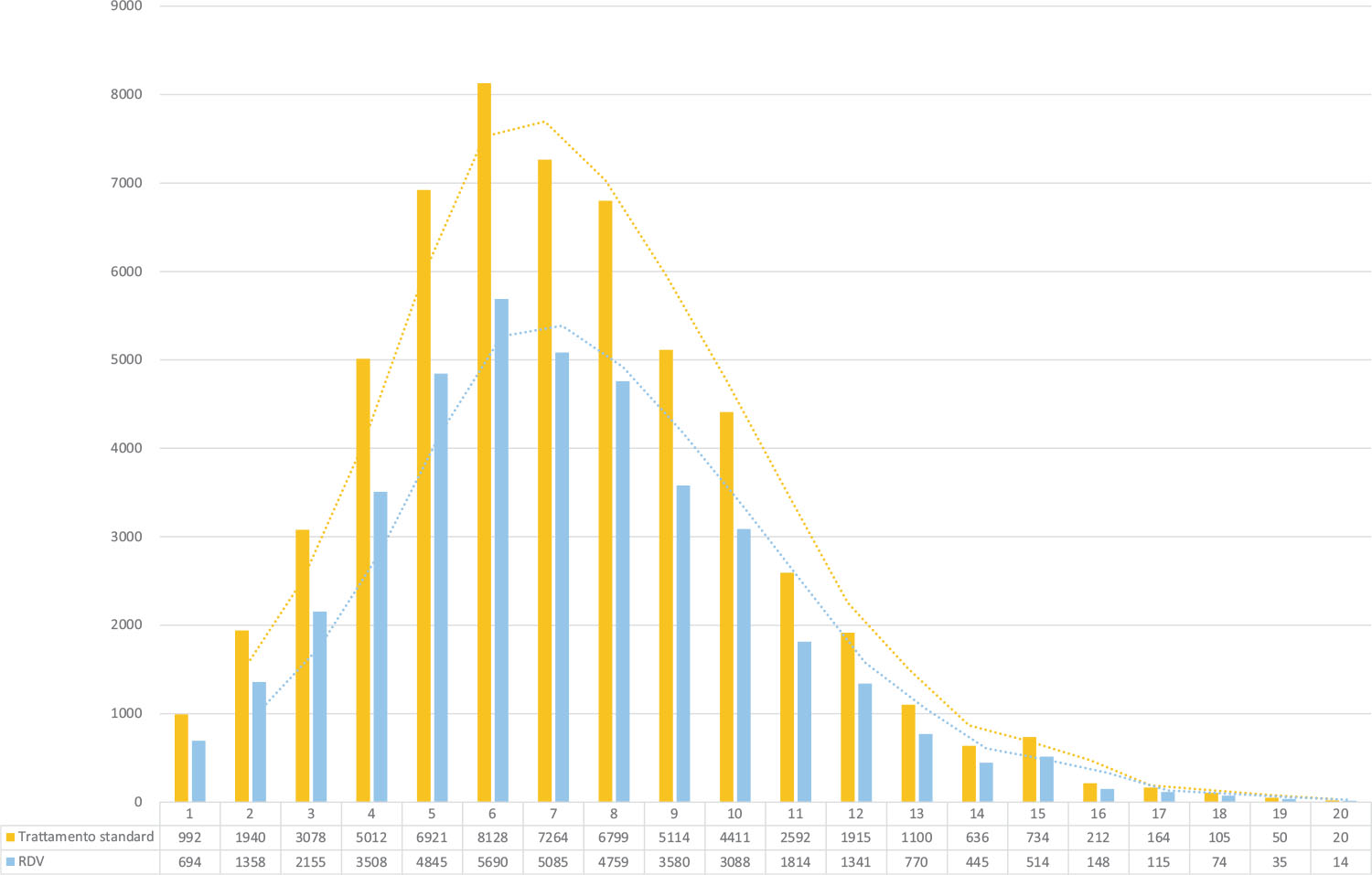
La Figura 2 riporta la distribuzione del numero di accessi in terapia intensiva per settimana senza e con la terapia a base di remdesivir e mette in evidenza come la terapia con remdesivir possa contribuire a ridurre il tasso di saturazione delle unità di terapia intensiva.
La Tabella IV riporta i costi delle due alternative di confronto ripartiti per ospedalizzati, ricoverati in terapia intensiva e deceduti. Dal modello emerge che la terapia con remdesivir può determinare un risparmio per il SSN di oltre 430 milioni di euro, principalmente grazie all’effetto della riduzione del ricorso alle cure in terapia intensiva.
| Trattamento standard | Con remdesivir | ||
|---|---|---|---|
| Contagiati | 2.748.950 | 2.748.950 | |
| Accessi in terapia intensiva | 57.166 | 40.016 | –17.150 |
| Morti | 16.586 | 9663 | –6923 |
| Trattamento standard | Con remdesivir | ||
|---|---|---|---|
| Costi ospedalizzati | 865.641.240 € | 733.050.312 € | –132.590.928 € |
| Costi terapie intensive | 915.698.493 € | 668.643.983 € | –247.054.509 € |
| Costi decessi | 151.527.522 € | 100.323.867 € | –51.203.654 € |
| Totale costi | 1.932.867.255 € | 1.502.018.162 € | –430.849.093 € |
Analisi di sensibilità
La Tabella V mostra i risultati delle analisi di sensibilità condotte. I parametri ai quali le stime sono maggiormente sensibili risultano essere in ordine:
– il valore degli Rt;
– il tasso di riduzione degli accessi in terapia intensiva;
– il tasso di riduzione della mortalità;
– la durata dei ricoveri;
– il numero di giornate in terapia intensiva;
– il time to recovery.
L’analisi di sensibilità multivariata mostra che, al variare simultaneo di tutti i parametri del modello, i risultati, ordinati dal venticinquesimo al settantacinquesimo percentile della distribuzione congiunta, restituiscono risultati dominanti con risparmi variabili fra i 251 e i 534 milioni di euro. La riduzione dei ricoveri in terapia intensiva risulta variabile tra 9400 e 24.100, mentre la riduzione dei decessi è variabile tra 4430 e 12.101.
Analisi di scenario
Best case
Lo scenario ottimistico, che ha ipotizzato una riduzione degli Rt pari a 0,2 punti a settimana a partire dalla quinta, stima 1,3 milioni di contagiati, circa 25 mila ricoveri in terapia intensiva e 8670 decessi. In questo scenario, l’introduzione di remdesivir comporterebbe una riduzione di 12.500 ricoveri in terapia intensiva e di 4800 decessi. Dal punto di vista economico, ciò si tradurrebbe in un risparmio di circa 294 milioni di euro.
Worst case
Lo scenario pessimistico ipotizza il valore degli indici Rt costante a 1,1 fino alla settimana 12 e, poi, pari a 1 dalla settimana 12 alla settimana 20. Dai risultati emerge una stima di circa 5,4 milioni di contagiati, 62.500 ricoveri totali in terapia intensiva e 27.159 decessi. A fronte di questo, l’introduzione di remdesivir comporterebbe una riduzione di 25.750 accessi in terapia intensiva e di 15.047 decessi. Dal punto di vista economico, ciò si tradurrebbe in un risparmio di circa 512 milioni di euro.
Discussione
I risultati di questo studio evidenziano che l’introduzione di remdesivir nei pazienti in ossigenoterapia a basso flusso può comportare, nell’arco di un’ondata pandemica di 20 settimane, un risparmio pari a 431 milioni di euro a fronte di 17.150 ricoveri in ICU e 6923 decessi evitati. In altre parole, il trattamento con remdesivir può non solo ridurre il burden della malattia, migliorando la salute dei pazienti e riducendo i decessi, ma può anche consentire un risparmio delle risorse sanitarie durante questa pandemia, comportando una minore durata della degenza ospedaliera e un minore accesso ai ricoveri in terapia intensiva. Dal punto di vista ospedaliero, l’utilizzo di remdesivir nei pazienti in ossigenoterapia a basso flusso libererebbe, dunque, sia posti letto in ospedale, permettendo, così, la gestione di più pazienti, sia posti letto in terapia intensiva, con relativo risparmio nell’impiego di mezzi respiratori invasivi e ottimizzazione nella gestione delle unità di terapia intensiva, unità che, durante questa pandemia, risultano oltremodo congestionate.
| Parametro | Differenza costi | Differenza terapie intensive | Differenza morti | |||
|---|---|---|---|---|---|---|
| 25esimo percentile | 75esimo percentile | 25esimo percentile | 75esimo percentile | 25esimo percentile | 75esimo percentile | |
| Rt | –152.498.724 € | –677.516.201 € | –10.594 | –22.358 | –965 | –12.780 |
| Riduzione accessi in terapia intensiva | –178.264.513 € | –598.415.678 € | –9851 | –20.561 | –5831 | –12.250 |
| Riduzione mortalità | –152.321.489 € | –554.897.632 € | –9542 | –21.549 | –4247 | –12.364 |
| Durata ricoveri | –148.326.124 € | –535.497.801 € | –12.564 | –21.006 | –4111 | –12.201 |
| Numero gg terapia intensiva | –195.231.476 € | –512.990.223 € | –13.428 | –22.056 | –3964 | –12.165 |
| Time to recovery | –192.316.473 € | –539.248.100 € | –13.894 | –22.561 | –3221 | –12.327 |
Diversi studi evidenziano, infatti, la preoccupazione crescente relativamente alla capacità del sistema sanitario nazionale italiano di rispondere efficacemente ai bisogni dei pazienti che necessitano di cure intensive per il COVID-19. (11,14) Le misure di razionalizzazione delle risorse ospedaliere devono essere attuate con urgenza, in caso contrario diventerà inevitabile un aumento considerevole di decessi. Il SSN dovrebbe prepararsi per un massiccio aumento della domanda di terapie intensive durante focolai incontrollati di COVID-19, garantendo un posto letto ad ogni paziente che necessitasse di un ricovero in ICU. Anche lo stesso Comitato Nazionale per la Bioetica si è espresso sulla questione dell’accesso alle cure in condizioni di risorse limitate nel contesto dell’attuale emergenza sanitaria, definendo il criterio clinico come l’unico criterio eticamente accettabile per l’assunzione di decisioni cliniche e affermando che la Costituzione riconosce il diritto di ogni individuo a ricevere tutte le cure sanitarie necessarie.
I dati utilizzati per alimentare il modello del presente articolo derivano dallo studio di Beigel et al. (8), studio randomizzato, in doppio cieco, controllato verso placebo, non sponsorizzato e condotto dall’Istituto nazionale per le allergie e le malattie infettive degli Stati Uniti. A oggi, lo studio di Beigel è l’unico che fornisce dati utilizzabili in un modello che stimi gli effetti derivanti dall’impiego di remdesivir nella popolazione oggetto di analisi. I risultati di questo studio dimostrano che l’utilizzo di remdesivir è in grado di ridurre significativamente il tempo del recupero clinico del paziente e la probabilità di progredire a stadi della malattia più gravi, che richiedono cure in unità di terapia intensiva e, in particolare per i pazienti in ossigenoterapia a basso flusso, ossia i pazienti candidabili al trattamento con remdesivir in Italia secondo le indicazioni dell’AIFA, lo studio ha dimostrato che remdesivir è in grado di ridurre il rischio di mortalità del 70%.
Ulteriori studi sono stati condotti su remdesivir con lo scopo di valutare il trattamento sui pazienti con COVID-19 (15,16,17-18), tuttavia non si prestano a essere inclusi in questo modello per alcune caratteristiche, come, per esempio, l’interruzione precoce dello studio per difficoltà nell’arruolamento, la scelta di condurre lo studio in aperto e senza avere come confronto lo standard of care o placebo, la mancanza di dati specifici a disposizione sui pazienti in ossigenoterapia a basso flusso.
Punti di forza e limitazioni dello studio
Il modello utilizzato presenta dei punti di forza e dei limiti. In generale, il punto di forza è rappresentato dal fatto che, a oggi, questo è l’unico modello, adattabile a scenari diversi, che consenta di collegare l’andamento epidemiologico e l’introduzione di strategie terapeutiche come remdesivir a variabili di tipo organizzativo, come, per esempio, il ricorso alle unità di terapia intensiva che rappresentano il punto più critico associato alla gestione dell’attuale crisi. Per questo, tale strumento potrebbe risultare utile ai decisori che si trovino a gestire anche eventuali altre ondate o, con gli opportuni adattamenti, pandemie derivanti da diversi virus.
Il modello si presta anche ad adattamenti di tipo regionale/locale (per esempio utilizzando i relativi Rt o, anche, dati real-world sui tempi di recupero provenienti da diverse realtà), permettendo, quindi, di condurre stime che potrebbero essere utili a prendere decisioni a vari livelli.
Il limite principale è costituito dal fatto che la base epidemiologica è rappresentata da dati sugli Rt osservati fino alla fine del mese di ottobre e, successivamente, ipotizzati tenendo conto anche delle misure restrittive messe in atto dal Governo a seguito dell’aggravarsi dell’ondata pandemica. Il modello, quindi, potrebbe non essere rappresentativo delle reali condizioni epidemiologiche, anche se poi, nella sua struttura, può essere comunque riadattato e popolato con nuovi dati reali che si rendano disponibili.
Il secondo limite è costituito dal fatto che i dati si basano sui risultati dell’unico studio (8) per il quale è possibile fare questo tipo di analisi e potrebbero cambiare in funzione delle nuove evidenze disponibili dagli studi in corso.
Conclusioni
In conclusione, la nostra analisi mostra che, in aggiunta alle misure volte a ridurre la trasmissione del virus, l’utilizzo di remdesivir nei pazienti ospedalizzati in ossigenoterapia a basso flusso, sulla base dei dati attualmente disponibili, sarebbe in grado di garantire, da un lato, una migliore gestione dell’emergenza e un migliore decorso clinico per i pazienti e, dall’altro, un notevole risparmio per il SSN. La presente analisi può contribuire a supportare le decisioni più opportune da parte dei leader politici e delle autorità sanitarie, per garantire che ci siano risorse sufficienti, inclusi personale, letti ospedalieri e strutture di terapia intensiva, per fronteggiare eventuali ulteriori ondate pandemiche.
Acknowledgements
The authors thank Claudio Ripellino for medical writing assistance on behalf of Health Publishing & Services Srl. The authors would like to extend their gratitude also to Dr. Elisa Martelli (Gilead Sciences) for the precious clarifications concerning the trial design and the population involved.
Disclosures
Conflict of interest: The authors declare no conflict of interest.
Financial support: This research received no specific grant from any funding agency in the public, commercial, or not-for-profit sectors.
The view expressed by authors does not represent - and has not to be interpreted - as the view of the Institutions they are affiliated to.
Bibliografia
- 1. Istituto Superiore di Sanità, Epidemia COVID-19, aggiornamento nazionale, 2 dicembre 2020. Online
- 2. Istituto Nazionale di Statistica, Conti Economici Trimestrali, 2 ottobre 2020. (Accessed November 2020). Online
- 3. Healthcare Datascience Lab, Centro sull’Economia e sul Management nella Sanità e nel Sociale, assorbimento di risorse economiche correlato alla gestione ospedaliera dei pazienti COVID-19 (Accessed November 2020). Online
- 4. ALTEMS, Alta Scuola di Economia e Management dei Sistemi Sanitari, COVID-19, Instant REPORT#18: 03 settembre 2020. Online
- 5. Agenzia Nazionale per i Servizi Sanitari Regionali (AGENAS), Rapporto COVID-19 (Accessed November 2020). Online
- 6. Summary of product characteristics (SMPC), Remdesivir. (Accessed November 2020). Online
- 7. Agenzia Italiana del Farmaco (AIFA). Emergenza COVID-19, Procedura di richiesta per il farmaco Veklury® (remdesivir). (Accessed November, 2020). Online
- 8. Beigel JH, Tomashek KM, Dodd LE, et al; ACTT-1 Study Group Members. Remdesivir for the Treatment of COVID-19 - Final Report. N Engl J Med. 2020;383(19):1813-1826. CrossRef Medline
- 9. Bassi F, Arbia G, Falorsi PD. Observed and estimated prevalence of COVID-19 in Italy: how to estimate the total cases from medical swabs data. Sci Total Environ. 2020;142799:142799; Epub ahead of print. CrossRef Medline
- 10. ISTAT. Indagine di sieroprevalenza sul SARS-CoV-2. (Accessed November 2020). Online
- 11. Grasselli G, Zangrillo A, Zanella A. Baseline characteristics and outcomes of 1591 patients infected with SARS-CoV-2 admitted for ICUs of the Lombardy Region, Italy. JAMA. 2020;323(16):1574-1581. CrossRef Medline
- 12. Ministero dell’Economia e delle Finanze – Commissione Tecnica per la Finanza Pubblica. Libro verde sulla spesa pubblica (2007). Online
- 13. ALTEMS, Alta Scuola di Economia e Management dei Sistemi Sanitari, COVID-19, Instant REPORT#28: 12 novembre 2020. Online
- 14. Remuzzi A, Remuzzi G. COVID-19 and Italy: what next? Lancet. 2020;395(10231):1225-1228. CrossRef Medline
- 15. Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. [published correction appears in Lancet. 2020 May 30;395(10238):1694]. Lancet. 2020;395(10236):1569-1578. CrossRef Medline
- 16. Spinner CD, Gottlieb RL, Criner GJ, et al; GS-US-540-5774 Investigators. Effect of Remdesivir vs Standard Care on Clinical Status at 11 Days in Patients With Moderate COVID-19: A Randomized Clinical Trial. JAMA. 2020;324(11):1048-1057. CrossRef Medline
- 17. Goldman JD, Lye DCB, Hui DS, et al. Remdesivir for 5 or 10 Days in Patients with Severe COVID-19. N Engl J Med. 2020;383:1827-1837. CrossRef Medline
- 18. World Health Organization. “Solidarity” clinical trial for COVID-19 treatments. (Accessed November 2020). Online